Капілярних явищ, сукупність явищ, обумовлених поверхневий натяг на межі розділу змішуються середовищ (в системах рідина - рідина, рідина - газ або пар) при наявності викривлення поверхні. Окремий випадок поверхневих явищ.
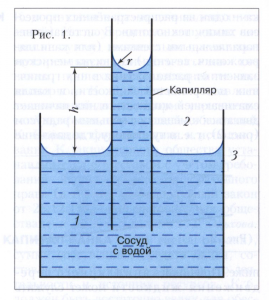
При відсутності сили тяжіння рідина обмеженою маси під впливом поверхневого натягу прагне зайняти обсяг з мінімальною поверхнею, т. Е. Приймає форму кулі. В умовах дії сили тяжіння не дуже в'язка рідина достатньої маси приймає форму судини, в який налита, і її вільна поверхня при відносно великій площі (далеко від стінок посудини) стає плоскою, так як роль поверхневого натягу менш істотна, ніж сили тяжіння. При взаємодії з поверхнею іншої рідини або твердого тіла (наприклад, зі стінками посудини) поверхню даної рідини викривляється в залежності від наявності або відсутності змочування. Якщо має місце змочування, т. Е. Молекули рідини 1 (рис. 1) сильніше взаємодіють з молекулами поверхні 3, ніж з молекулами іншої рідини (або газу) 2, то під впливом різниці сил міжмолекулярної взаємодії рідина 1 піднімається по стінці судини - ділянку рідини, що примикає до стінки, викривляється. Тиск, що викликається підйомом рідини, врівноважується капілярним тиском? Р - різницею тисків над і під викривленої поверхнею розділу. Величина капілярного тиску залежить від середнього радіуса r кривизни поверхні і визначається формулою Лапласа:? Р = 2σ / r, де σ - поверхневий натяг. Якщо межа розділу фаз плоска (r = ∞), то в умовах механічної рівноваги системи тиску по обидва боки кордону розділу рівні і? Р = 0. У разі увігнутої поверхні рідини (r <0) давление в жидкости ниже, чем давление в граничащей с ней фазе и ∆р <0; для выпуклой поверхности (r> 0)? Р> 0.
Викривлення поверхні впливає на умови рівноваги між рідиною і її насиченим паром: згідно Кельвіна рівнянням, тиск парів над краплею рідини підвищується зі зменшенням її радіусу, що пояснює, наприклад, зростання великих крапель в хмарах за рахунок малих.
До характерних капілярних явищ відносяться капілярне всмоктування, поява і поширення капілярних хвиль, капілярний пересування рідини, капілярна конденсація, процеси випаровування і розчинення при наявності викривленої поверхні. Капілярний всмоктування характеризується швидкістю, яка залежить від капілярного тиску і в'язкості рідини. Воно відіграє істотну роль у водопостачанні рослин, русі води в грунтах та інших процесах, пов'язаних з рухом рідин в пористих середовищах. Капілярна просочення - один з поширених процесів хімічної технології. У системах з непаралельними стінками (або капілярах конічного перетину) кривизна менісків залежить від розташування в них граничних поверхонь рідини, і крапля смачивающей рідини в них починає рухатися до меніска з меншим радіусом (рис. 2), т. Е. В ту сторону, де тиск нижче. Причиною капілярного пересування рідини може служити і різниця сил поверхневого натягу в меніска, наприклад при існуванні градієнта температури або при адсорбції поверхнево-активних речовин, що знижують поверхневий натяг.

Викривлення поверхні рідини може істотно впливати на процеси випаровування, кипіння, розчинення, зародкоутворення при конденсації пари і кристалізації. Так, властивості систем, що містять велику кількість крапель або бульбашок газу (емульсій, аерозолів, пен), і їх формування багато в чому визначаються капілярними явищами. Вони лежать також в основі багатьох технологічних процесів: флотації, спікання порошків, витіснення нафти з пластів водними розчинами поверхнево-активних речовин, адсорбційного розділення і очищення газових і рідких сумішей і т. П.
Вперше капілярні явища були досліджені Леонардо да Вінчі. Систематичного спостереження і опису капілярні явища в тонких трубках і між плоскими, близько розташованими скляними пластинами провів в 1709 Ф. Хоксби, демонстратор Лондонського королівського товариства. Основи теорії капілярних явищ закладені в працях Т. Юнга, П. Лапласа, а їх термодинамічне розгляд здійснив Дж. Гіббс (1876).
Літ. Адамсон А. Фізична хімія поверхонь. М. 1979; Роулінсон Дж. Уідом Б. Молекулярна теорія капілярності. М. 1986.
А. М. Ємельяненко, Н.В. Чураев.