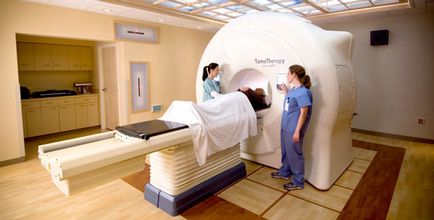

Слідом за змінами стандартів хірургічного та системного лікування різко зросли вимоги до променевої терапії. Поряд з максимальною ефективністю обов'язковою умовою сучасного радіаційного лікування є його безпеку, а саме прецизійне опромінення тільки пухлинної тканини, зниження дозового навантаження на розташовані поруч критичні органи і зменшення ступеня проявів ранньої та пізньої токсичності.
Найбільш досконалим технологічним втіленням сучасної променевої терапії, що відповідає вимогам сьогоднішньої онкологічної практики, є томотерапія (TomoTherapy).

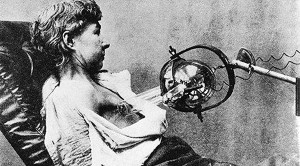
Еміль Груббе вже в 1896 р провів опромінення молочної залози при неоперабельний карциномі (ім'я першої пацієнтки Rose Lee), а Віктор Деспень, лікар з Ліона, через 5 місяців після відкриття Х-променів використовував катодний трубку Крукса (рис. 2) для опромінення хворий з величезною пухлиною в шлунку.
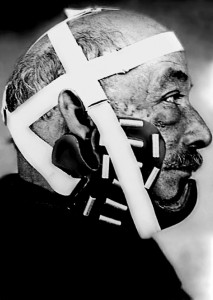
Цей метод лікування полягав у введенні зерен з джерелами випромінювання всередину ураженого органу. Брахітерапії застосовували для лікування раку шкіри, передміхурової залози, молочної залози, стравоходу, піхви, тіла і шийки матки, бронхів, жовчних проток, мови.
На жаль, повальне захоплення солями радіоактивного радію і віра в його зцілюють сили привели до того, що в лікарнях почали пропонувати нові анекдотичні методи терапії, які мали найсерйозніші негативні наслідки для хворих: інгаляції радієм, застосування радієвих мазей і внутрішньовенних ін'єкцій розчинами, що містять солі радіоактивного радію, вживання радієвої води і навіть шоколаду з радієм (рис. 4).

Про те, що крім лікувального ефекту радій найчастіше призводить до утворення численних злоякісних пухлин, стало відомо тільки на початку 1930-х рр. Шоком для суспільства стала смерть Ебена Макберні Байєрса (1880-1932), багатого американського промисловця і спортсмена, який помер від численних метастазів радіаційно-індукованого раку внаслідок вживання популярного патентованого ліки, приготованого з радію і розчиненого у воді.
На згадку про жертви застосування Х-променів в госпіталі St. Georg в Гамбурзі (Німеччина) був відкритий меморіал, на якому в 1936 році було вигравірувано 169, а в 1959 р - вже 359 імен людей, смерть яких безпосередньо була пов'язана з «лікувальним» використанням радію.
Проте паралельно з неперевіреними і небезпечними методами лікування активно розвивалося інший напрямок променевої терапії, відбувалося вдосконалення нових технологій. Першу половину ХХ століття можна назвати «епохою кіловольт», оскільки для зовнішнього опромінення пухлин використовували катодні трубки Х-променів - технологію, яку розробив Вільям Кулідж.
З 1946 р почалася «епоха МегаВольт». Їй передувало відкриття Ірен і Фредеріком Жоліо-Кюрі в 1934 р явища штучної радіоактивності. Перша радіологічна революція пов'язана з іменами Гарольда E. Джонсона і Джона Куннінгама, які в 1951 р створили «бомбу для раку» на основі нового джерела гамма-променів - радіоактивного кобальту-60. Технологія дозволяла досягати енергії пучка фотонів в 1,2 МеВ і доставляти дозу опромінення 45-60 Гр до глибоко розташованих пухлин. Вперше кобальт-60 для терапії раку був використаний в м Саскатун (Саскачеван, Канада). У західних клініках у вигляді комерційної технології цей метод використовували протягом 20-30 років.
Друга радіологічна революція ХХ століття пов'язана з розробкою лінійного прискорювача. Ідея його створення належить Ернесту Томасу Уолтону (1929 г.). У Західній півкулі «батьком» лінійного прискорювача прийнято вважати Едварда Леонарда Гінзтона, який був Співзасновник компанії Varian (1948) і співзасновником Силіконової долини.
У лінійному прискорювачі завдяки мікрохвильової технології харчування потужність рентгенівських променів зростає від 6 до 20 МеВ, а енергія в тканинах пухлини може бути підвищена до 70 Гр.
У новій технології змінилися планують системи (2D) і з'явилася дозиметрія. Це змінило позиції променевої терапії в ті роки. Радіаційні онкологи стали повноправними членами мультидисциплінарної онкологічної команди.
Радіочутливість і радіорезистентність пухлинних клітин
Паралельно з вдосконаленням технологій променевої терапії активно розвивалися фундаментальні напрямки радіобіології. Були отримані унікальні дані, що дозволили зрозуміти молекулярні механізми радиорезистентности ракових клітин, а також вивчити шляхи індукції канцерогенезу в біологічних тканинах після впливу іонізуючої радіації.
Ще в 1906 р Клаудіус Рего, який працював в інституті Кюрі, виявив, що Х-промені викликають безпліддя. На підставі цього спостереження було зроблено висновок, що Х-промені можна використовувати для впливу на швидкорослі клітини, якими є клітини раку.
Надалі Дж. Бергоньє і Л. Трибондо показали, що клітини біологічного організму дійсно володіють різною радіочутливість. В організмі людини радіочутливим є гамети, еритробласти, епідермальні стовбурові клітини і стовбурові клітини шлунково-кишкового тракту, ооцити, лімфоцити. Мінімальною чутливістю володіють нейрони і м'язові клітини.
Закон Бергоньє - Трибондо говорить, що клітини то чутливіші до опромінення, ніж вони швидше розмножуються, чим триваліше фаза мітозу і чим вони менш диференційовані. У міру накопичення даних по радіобіології були внесені доповнення в закон: найбільш чутливими є недиференційовані клітини, які добре кровоснабжаются і мають активний метаболізм. Останнім часом доведено, що на радіочутливість впливають також молекулярно-біологічні особливості клітини (зокрема, мутації KRAS і EGFR).
Трохи пізніше австралійський радіобіолог Хуберт Родні Уітерс узагальнив теоретичні дані і сформулював закон радіобіології, який отримав назву 4R (рис. 5).
Вплив радіотерапії на пухлинне микроокружение - судинну систему і строму
Іонізуюча радіація призводить до пошкодження не тільки ракових клітин, але також клітин пухлинного мікрооточення.
Біологічний ефект іонізуючого випромінювання триває не хвилини і години, а місяці і роки. При цьому ранній біологічний ефект, що складається з запальної і проліферативної фази, змінюється пізнім біологічним ефектом, під час якого відбувається ремоделювання опромінених тканин.
У реалізацію як раннього, так і пізнього радіобіологічного ефекту залучені судини і строма пухлини.
Ранніми наслідками впливу іонізуючої радіації на судинну систему є дисфункція ендотеліальних клітин (підвищена проникність, відділення від базальної мембрани, апоптоз), агрегація тромбоцитів, претромботіческіе стану, мікротромби, диапедез, адгезія клітин запалення, руйнування кровоносних судин, зниження їх щільності, порушення перфузії тканин, гіпоксія, збільшення виробництва цитокінів, хемокінів, гіпоксичного фактора HIF-1α.
Пізніми наслідками є пошкодження ангиоархитектоники - потовщення інтими судин, тромбози, медіонекроз, облітеруючий ендартеріїт, атеросклероз, погіршення доставки кисню до тканин і гіпоксія.
Постлучевая пошкодження сполучної тканини ведуть до розвитку радіаційного фіброзу. Цьому стану передують хронічне запалення, імунні реакції і ремоделирование тканин. У механізмах розвитку радіаційного фіброзу беруть участь пухлина-асоційовані фібробласти, прозапальні цитокіни, інтерлейкіни IL-1, IL-6, IL-8, гранулоцити-макрофаги, колониестимулирующие фактори (GM-CSF), циклооксигеназа 2 (ЦОГ-2), трансформують фактори зростання (TGF-β), протеолітичні ферменти, компоненти позаклітинного матриксу.
Важливим механізмом є підвищення активності гепаранази, що створює умови для інвазії ракових клітин в тканини микроокружения під час проведення променевої терапії.
В цілому механізми формування фіброзу при загоєнні ран (операція, травма) та фіброзу при опроміненні (променева терапія) різко відрізняються: активність формування радіаційно-індукованого фіброзу зберігається протягом багатьох років і ніколи не припиняється.
Ранні та пізні ускладнення радіотерапії
До численних ранніх ускладнень радіотерапії відносять мукозити, радіодерматіти, діарею, алопецію, цистит, проктит, пневмоніт, супрессию кісткового мозку.
Ці ускладнення, зважаючи на наявність маніфестних клінічних проявів, легко розпізнаються і піддаються активної терапії.
Не меншу, а можливо, і більшу проблему представляють пізні ускладнення променевої терапії, які рідко реєструються в практиці онколога через тривале субклинического асимптомного течії. До таких належать, наприклад, ущільнення і зменшення в обсязі тканин молочної залози (поганий естетичний ефект терапії), фіброз і ригідність легких, мальабсорбція і стриктури тонкої кишки, пізня ішемія і перфорації кишечника, гематурія, телеангіоектазії шкіри, ендокринна недостатність, безпліддя, а також розвиток радіаційно-індукованого вторинного раку.
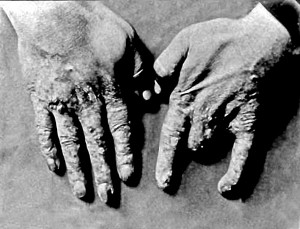
Жертвами численних ускладнень, викликаних опроміненням, на початку ери радіотерапії ставали і самі лікарі-радіологи (рис. 6).
Рецидив раку і метастазування як ускладнення радіотерапії
Ще в 1927 р Герман Джозеф Мюллер вивчав генетичні ефекти опромінення, в тому числі вплив Х-променів на ризик розвитку раку. У 1946 р за свої роботи в області радіогенетікі він був удостоєний Нобелівської премії з фізіології і медицині.
До теперішнього часу накопичені переконливі докази того, що опромінення здорових тканин мікрооточення пухлини сприяє інвазії і метастазування ракових клітин, а опромінена строма здорових тканин сприяє ініціації канцерогенезу.
Відомі результати експериментів, коли після опромінення здорових тканин молочних залоз у щурів з подальшою трансплантацією в зони розвиненого радіаційного фіброзу нормальних міоепітеліоціти останні трансформувалися в ракові клітини.
Радіаційно-індуковані пухлини щитовидної залози, шийки матки, прямої кишки, молочної залози, що розвинулися через кілька років після опромінення здорових тканин відповідної анатомічної області, - відомі факти в практиці онкологів.
Біологічні ефекти впливу радіотерапії на микроокружение пухлини, як причини онкологічних рецидивів і метастазування, реалізуються через запалення, модуляцію канцер-асоційованих макрофагів, імунну модуляцію, ремоделирование мікрооточення і формування фіброзу в зоні опромінених тканин.
При опроміненні нормальних тканин, розташованих поряд з пухлиною, відбувається активація фібробластів, дисфункція ендотелію судин, запалення, ремоделирование тканин, розвивається необоротне ушкодження строми і радіаційний фіброз, який згодом сприяє виникненню раку de novo.
СТАТТІ за темою Онкологія та гематологія
Це було недавно, це було давно ... 1963 рік. Київ. Рання весна. Чудова погода, неповторна атмосфера рідного міста, насолоджуючись якими, я не міг передбачити уготованную долею зустріч з видатним вченим, академіком АН УРСР Ростиславом Євгеновичем Кавецьким. На ці пам'ятні хвилини спілкування з ним я, звичайно ж, анітрохи не розраховував.