Порівняльна характеристика сучасних кокцидіостатиків
Кузьмін А.А. канд.вет.н.

Кокцидіостатики - речовини, призначені для профілактики і / або лікування кокцидіозів (еймеріозов) у тварин. Більшість сучасних кокцидіостатиків володіють не тільки кокцідіостатіческім дією, тобто здатністю запобігати розмноженню і розвиток кокцидий, але і кокцидіоцидна дією, тобто здатністю вбивати кокцидии на різних стадіях їх розвитку. Тільки деякі кокцидіостатики придатні для лікування кокцидіозів, оскільки при клінічно вираженому кокцидіоз, до моменту появи клінічних ознак, розвиваються серйозні порушення в уражених органах.

Таблиця 1. Послідовність впровадження кокцидіостатиків в ветеринарну практику
Кокцідіостатіческой або кокцидіоцидна активністю володіють тетрациклін, сульфаніламіди, нітрофурани та деякі інші препарати. Їх не відносять до «кокцидіостатик», оскільки основним їх дією є протимікробну дію.
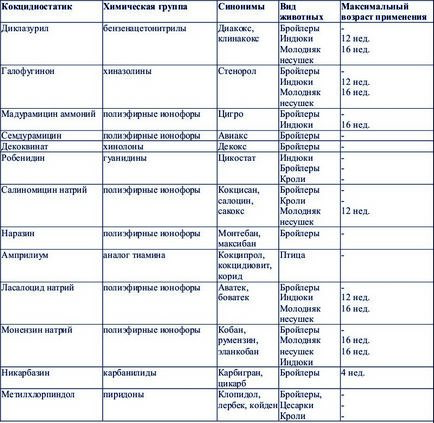
Для класифікації кокцидіостатиків використовують зазвичай змішану класифікацію, засновану на схожості структури і / або механізму дії препарату (табл.2)
Таблиця 2. Кокцидіостатики, дозволені до застосування в ЄС
Бензенацетонітріли. До бензенацетонітрілам відноситься діклазуріл - хімічний кокцидіостатик, що володіє найвищою протівококцідіозной активністю. Механізм його дії остаточно не з'ясований. Діє на ранні ендогенні стадії розвитку кокцидій. Ефективний проти дуже широкого спектру найпростіших у різних видів тварин. Нетоксичний.
Тріазінтріони. До тріазінтріонам відноситься толтразурилу - хімічний кокцидіостатик, застосовуваний. головним чином, для лікування кокцидіозу у птиці і свиней. Діє на внутрішньоклітинні стадії розвитку кокцидій. Володіє широким спектром дії. Малотоксичний.
Сульфаніламіди і етопабат. До цієї групи відносять сульфахлорпіразін, сульфадиметоксин, сульфаметазин, сульфахіноксалін (сульфаніламіди) і етопабат (похідне бензойної кислоти). Механізм їх дії заснований на конкурентному антагонізмі з пара-амінобензойної кислотою, яка необхідна кокцид для синтезу фолієвої кислоти. Ефективність дії сульфаніламідів різко збільшується при їх поєднанні з інгібітором дигідрофолатредуктази - триметопримом. Найбільш чутливі до них пізні вегетативні стадії розвитку кокцидій. Тому препарати цієї групи не перешкоджають виробленню імунітету до кокцид. У той же час, до сульфаніламідів досить легко виробляється стійкість.
Аналоги тіаміну. До них відноситься ампроліум. Оскільки ампроліум структурно нагадує тіамін, він викликає у кокцидий дефіцит цього вітаміну. Коефіцієнт безпеки ампроліума дорівнює приблизно 8: 1. При передозуванні він здатний викликати В1 -гіповітаміноз у тварин. Ампроліум не ефективний або має слабку ефективність проти деяких видів кокцидий.
Ионофорного антибіотики є продуктами Streptomyces spp. і Actinomadura spp. До цієї групи належать моненсину, ласалоцід, саліноміцин, наразін, мадураміцін, семдураміцін. Іонофори утворюють з іонами натрію, калію, магнію і кальцію ліпофільні комплекси, легко проникають через клітинні мембрани. Внаслідок цього всередину клітини проникають іони хлору, вода. Відбувається набухання клітин, порушуються функції мітохондрій у кокцидий. У тварин ионофорного антибіотики здатні викликати порушення обміну електролітів при введенні в субтоксических або токсичних дозах, а також при використанні тваринам, для яких вони мають особливу токсичність (коні).
Іонофори впливають на ранні позаклітинні і внутрішньоклітинні стадії кокцидий. В даний час, внаслідок масового застосування, широко поширені стійкі до іонофори штами кокцидий, причому стійкість розвивається до всіх представників даної групи препаратів.
Антибіотики, що відносяться до цієї групи, також ефективні проти аеробних і анаеробних грампозитивних бактерій, таких як Lactobacillus spp. Clostridium perfringens, Eubacterium spp. Peptococcus spp. Peptostreptococcus spp. Streptococcus bovis, Acholeplasma spp. Mycoplasma spp. Придушення грампозитивних бактерій в шлунково-кишковому тракті зменшує споживання ними поживних речовин, які дістаються господареві, а не паразита або комменсали, а також профилактирует некротичний ентерит, викликаний Clostridium perfringens. Це, як вважають, є причиною того, що застосування іонофоров в помірних дозах до деякої міри збільшує добові прирости і оплату корму.
Карбаніліди. Нікарбазін впливає на енергетичний обмін через трансгідрогеназу і АТФ. Цей препарат небезпечний тим, що сприяє розвитку теплового стресу у птахів.
Хінолони (буквінолат, декоквінат, неквінат) діють на спорозоїти, блокуючи перенос електронів в мітохондріях паразитів. Блокують синтез ДНК шляхом пригнічення ДНК-гірази. Це малотоксичні препарати, до яких, однак, досить швидко виробляється стійкість.
Похідні гуанідину. Робенідін запобігає формуванню зрілих шизонтів, діє як кокцідіостатіческі, так і кокцидіоцидна. До робенідіну у кокцидий досить швидко виробляється стійкість.
Основним методом застосування кокцидіостатиків є профілактичний метод, коли препарат або суміш препаратів вводиться в організм тварин, що не мають клінічних ознак кокцидиоза. Кокцидіостатики застосовують профілактично тваринам певних видів (в основному - птиці), визначеного віку (в основному - молодняку), визначеного способу утримання (в основному - групового, підлогового). Вимушене застосування кокцидіостатиків з лікувальною метою менш ефективно, ніж профілактичне застосування.
Кокцидіостатики застосовують зазвичай груповим методом з кормом або водою. Тривалість застосування залежить від паразитологічної ситуації, виду тварин, застосовуваного препарату і використовуваних доз. Низькі дози кокцидіостатиків застосовують більш тривалий час, ніж високі, часто довічно. Від виду препарату і доз залежить вироблення імунітету до кокцид у тварин. Високоефективні препарати у високих дозах повністю пригнічують розвиток кокцидий в організмі тварин і, як наслідок, - перешкоджають виробленню природного імунітету до кокцидіозу, оскільки різко зменшують контакт з кокцідіознимі антигенами. Для бройлерів така проблема не актуальна з-за нетривалого періоду їх життя, а для інших тварин більш обґрунтованим є або дозоване застосування препаратів, які не перешкоджають виробленню імунітету, або / та використання вакцин проти кокцидіозу.
Оскільки у кокцидий поступово виробляється стійкість (резистентність) до кокцидіостатик, необхідна періодична заміна препаратів. Зазвичай таку заміну здійснюють за допомогою "човникових" програма, коли послідовно на одному поголів'я застосовують більш одного кокцидіостатик, а також в "ротаційних" програмах шляхом періодичної заміни 1 раз в 4-6-12 місяців. У човникових програмах зміна кокцидіостатик відбувається при плановій зміні комбікорми.
У бройлерів за 3-7 днів перед забоєм зазвичай припиняють давати кокцидіостатик. Це пояснюється необхідністю знизити концентрацію препарату в м'ясі до мінімального допустимого рівня (МДР).
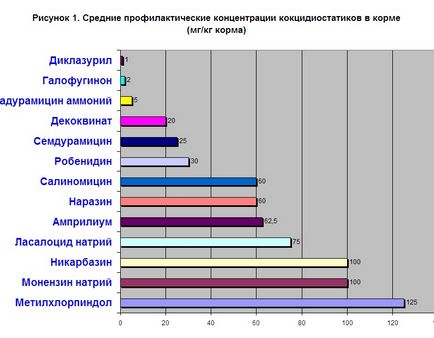
Ефективність більшості сучасних кокцидіостатиків достатня для запобігання клінічно вираженого кокцидиоза у тварин. У малюнку 1 наведені середні терапевтичні концентрації кокцидіостатиків для птиці. З цих даних видно, що найбільшою антікокцідіозной ефективністю володіють діклазуріл (діакокс), галофугінон і мадураміцін. Однак галофугінон і мадураміцін досить токсичні, галофугінон небезпечний при тепловому стресі, а до мадураміціну резистентні багато ізоляти кокцидий. Ефективність інших препаратів набагато нижче. Їх ізоеффектівних дози (концентрації) перевищують ефективну профілактичну концентрацію в кормі діклазуріла в 20-100 разів. Тобто для досягнення такого ж профілактичного або лікувального ефекту, що і у діклазуріла (діакокса), необхідно в 20-100 разів більше іншого препарату.
Слід враховувати, що не всі кокцидіостатики володіють ефективністю проти всіх видів кокцидий. До препаратів, ефективним проти всіх видів кокцидий, відноситься діклазуріл (діакокс) [3].
Токсичність і негативну дію
Сучасні кокцидіостатики в рекомендованих дозах або концентраціях, як правило, малотоксичні. Разом з тим у деяких препаратів дуже маленький індекс безпеки. Інші ж препарати, наприклад діклазуріл, практично зовсім не токсичні (табл. 3).
Таблиця 3. Смертельні дози (ЛД50) деяких кокцидіостатиків (мг / кг)
Випадки отруєння мають місце при використанні кокцидіостатиків у тварин, яким вони не рекомендовані, при завищенні дози або концентрації, а також при застосуванні їх для слабких і виснажених тварин. В даний час більшість повідомлень про негативну дію кокцидіостатиків доводиться на частку ионофорного антибіотиків.
Ионофорного антибіотики. Є численні повідомлення про токсичну дію ионофорного антибіотиків на ссавців і, особливо, на птахів [4,5]. Механізм їх токсичної дії пов'язаний, головним чином, з порушенням функціонування серцевої і скелетної мускулатури внаслідок порушення обміну кальцію і натрію. Ставлення терапевтичної дози до ЛД50 складає всього 2-3. Навіть незначне перевищення терапевтичної дози або концентрації в кормі призводить до негативних наслідків: знижується середньодобовий приріст, з'являється анорексія (втрата апетиту). У більш високих дозах вони викликають м'язову слабкість, порушення координації рухів, сонливість, депресію, діарею, зниження несучості. Випадки інтоксикації іонофори описані практично у всіх видів тварин, але найбільш чутливі тварини - коні та інші непарнокопиті, а також індики і кішки. На розтині і гістологічно виявляються ознаки міокардіодистрофії, м'язового некрозу, розширення шлуночків серця, виснаження, асцит. У разі припинення надходження ионофорного кокцидіостатиків в організм, досить швидко настає зникнення клінічних ознак і відновлення продуктивності.
Неіонофорние кокцидіостатики. Галофугінон виявив здатність знижувати міцність шкіри у птахів через порушення синтезу колагену. Він особливо токсичний для гусей, качок і риб. Робенідін і галофугінон проявили ембріотоксичну дію у курей. Галофугінон здатний викликати підвищення температури тіла у птахів. Нікарбазін токсичний для несучок, особливо для несучих пігментовані яйця, а також небезпечний при тепловому стресі [6].
Вплив на здоров'я людей. Як і будь-які інші ксенобіотики (чужорідні речовини), кокцидіостатики здатні чинити негативний вплив на здоров'я людей. В організм людини кокцидіостатики можуть потрапляти безпосередньо, наприклад, в процесі виготовлення комбікорму з кокцидіостатик, а також через тваринницьку продукцію. При безпосередньому контакті з іонофори відзначені випадки дратівної впливу на шкіру, а також алергічні реакції. Подразнюючу дію на шкіру та слизову оболонку очей також відзначено для аерозолів ампроліума, метілхлорпіндола, робенідіна і галофугінона. При роботі з кокцидіостатиками необхідно дотримуватися звичайних методів безпеки - використовувати захисний одяг, рукавички, респіратори.
Все кокцидіостатики всмоктуються в шлунково-кишковому тракті тварин і потрапляють в їстівні органи і тканини. Для більшості кокцидіостатиків встановлені періоди очікування (каренції), протягом яких м'ясопродукти, молоко, яйця непридатні в їжу людини. При плановому застосуванні кокцидіостатиків їх вилучають з корми за кілька днів перед забоєм. Ці терміни різні для різних речовин і видів тварин. Для деяких з них, внаслідок малої токсичності і незначного вмісту в тваринницькій продукції, терміни очікування не встановлені (діакокс).
Вплив на навколишнє середовище. Залишки кокцидіостатиків, як і інших хіміотерапевтичних засобів, з послідом, сечею, залишками кормів, потрапляють в навколишнє середовище, головним чином в гноєсховища. Там відбувається їх биодеградация. Наприклад, моненсину Біодеградуючі в посліді птахів протягом близько 30 діб, ампроліум - протягом 80 діб. В анаеробних умовах биодеградация кокцидіостатиків протікає повільніше, ніж в аеробних.
Кокцидіостатики, зокрема іонофори, впливають на мікробний склад посліду. Це може призводити до зміни його властивостей. Так моненсину на 20% зменшує продуктивності установок з виробництва біогазу з гною за рахунок пригнічення грамположительной мікрофлори посліду.
Деякі кокцидіостатики можуть заподіювати шкоду макроорганізму. Наприклад галофугінон, як згадувалося вище, токсичний для риб в концентрації вище 0,7 частин на мільйон.
- Кокцидіостатики в доступному для огляду майбутньому залишаться основним засобом для профілактики і лікування кокцидіозу тварин, особливо птахів.
- Сучасні кокцидіостатики дозволяють повністю профілактувати кокцидіоз у тварин за умови дотримання регламенту застосування, спектра дії і обліку можливої резистентності кокцидий до кокцидіостатик.
- Слід дотримуватися обережності і не перевищувати профілактичних (терапевтичних) концентрацій для препаратів, що володіють невисоким коефіцієнтом безпеки (ионофорного антибіотики, галофугінон, нікарбазін).
- В даний час найбільшою антікокцідіозной активністю і найменшою токсичністю володіє кокцидіостатик з групи бензенацетонітрілов - діклазуріл (діакокс).
- Діакокс можна застосовувати в будь-яких протівококцідіозних програмах в поєднанні з будь-якими іншими кокцидіостатиками, медикаментами і кормовими добавками.
4. Howell J. Hansson J. Onderka D. et al. Monensin toxicity inchickens.- Avian Diseases.- 1980.-24.- p.1050-1053.
6. Long P. L. The Biology of the Coccidia.- N.Y ..- 1982.