Пряма дія фтору на органічні речовини призводить до бурхливої реакції, що супроводжується спалахами і вибухами. В результаті виходять фторид водню і продукти розлив-вання органічних молекул (вуглець, тетрафторметан). Такий напрям реакції обумовлено її високою зекзотермічностью, яка перевершує енергію розриву вуглець-вуглецевих зв'язків.
Спокійніше реакція протікає при розведенні фтору (і парів органічної речовини) інертним в даних умовах газом, що сприймає частину тепла, що виділяється і виводячи-щим систему з дуже широких меж вибуховості. Таким газом-розріджувачем на практиці зазвичай служить азот. При фто-рірованіі в рідкій фазі можна застосовувати стійкі до дію-вию фтору розчинники (фторуглероди, при низькій темпера-туре- Тетрахлорметан). При найбільш поширеною газо-фазної реакції крім розведення азотом позитивне впливав-ня надає теплопроводящая насадка (наприклад, з мідного дроту).
Механізм реакцій фторування сильно відрізняється від хло-рірованія. Причина цього полягає в дуже слабкою електрофільності молекули фтору, внаслідок чого відбуваються тільки ра-дікально-ланцюгові реакції. Для них не потрібно сторонніх ініціаторів, а ланцюг зароджується спонтанно за рахунок взаи-модействие фтору з вуглеводнем; подальший розвиток ланцюга протікає звичайним чином:
Інша особливість полягає у високій активності і пов'язаної з цим малої вибірковості фтору при його атаці органічної молекули. Так, на відміну від хлорування, при фторування йдуть одночасно реакції заміщення і приєднання, причому заміщуються майже з однаковою ймовірністю різні атоми водо-роду, в тому числі в уже утворилися фторпохідні. Крім того, істотний розвиток отримує розщеплення по С-С-зв'язків; ці перетворення можна обмежити, пом'якшуючи умови реакції.
По викладеним причин фторування ведуть в промисло-вості головним чином для отримання перфторпроізводних вуглеводнів (перфторуглероди), що відрізняються дуже високо-кой термічної і хімічної стабільністю. З них продукти фторування середніх фракцій нафти застосовують як термо-стійкі мастила і гідравлічні рідини, а вироб-водні фракції С7 -С10 - як розчинники.
У промисловості існує не-скільки способів фторування.
Каталітичне фторування здійснюють в апараті з мідною стружкою, покритої шаром срібла: у аппа-рат подають фтор і вуглеводень, розбавлені азотом. Роль міді обумовлена її високою теплопровідністю і складається в акумулюванні тепла, що виділяється. Срібло, мабуть, пе-реходит під дією фтору в AgF2. який досить м'яко фторує вуглеводень. Однак відбувається і пряме взаємо-дія останнього з фтором, внаслідок чого вихід цільового продукту відносно малий-від 40 до 80-90%.
Металлофторідний процес набув найбільшого поширення. Він заснований на застосуванні вищих фторидів металів (CoF3. MnF3), взаємодіючих з вуглеводнями порівняно м'яко і з не настільки великим виділенням тепла. Відпрацьовану сіль знову регенерують під дією фтору:
Цим загальна теплота реак-ції F2 з ГH, складова 460 кДж / моль, розподіляє-ся на дві стадії, з яких вуглеводень приймає навчаючи-стіе тільки в одній, що має помірний тепловий ефект. Внаслідок цього виходить більший вихід продукту.
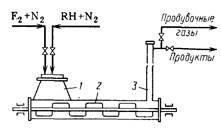
Реакційний апарат (рис. 53) являє собою горизон-тальне сталеву трубу з лопатевою мішалкою, що обертається зі швидкістю
20 об / хв. Труба приблизно наполовину заповнені-нена фторидами кобальту. У ліву її частину, де знаходиться за-грузочно люк, надходять пари органічного реагенту, разбана-лені 5-10-кратним надлишком азоту. З іншого кінця реак-тора відводять утворюються продукти, які спочатку по-падають в вивідну трубу, де звільняються від захоплених частинок фториду кобальту, і потім направляються на охолодження і поділ.
Реакцію ведуть до тих пір, поки 50% трифторида кобальту чи не перетвориться в дифторид. Температуру підтримують неодим-кові по довжині труби: 150-200 ° С на вході і 300-380 ° С на виході. Це пояснюється тим, що вуглеводень фторується до статочно швидко і щоб уникнути деструкції бажана низька температура. У той же час заміщення останніх атомів по-огрядний протікає зі значною працею, і для цього тре-буется більш висока температура. Оптимальний час контакту становить 2-3 хв. Після того як 50% трифторида кобальту витратиться, припиняють подачу вуглеводню і продувають реактор азотом. Потім регенерують трифторид кобальту, про-пускаючи при 250 ° С вільний фтор, розбавлений азотом, знову продувають апарат азотом з метою витіснення залишків фтору і знову починають реакцію. Таким чином, робота реактора є періодичною і складається з двох основних стадій (соб-ственно реакції і регенерації) і двох операцій продувки. Це - істотний недолік даного методу.
Електрохімічне фторування початок раз-виваться лише останнім часом, але воно має ряд переваж-вин в порівнянні з тільки що описаними методами. Сущ-ність його полягає в наступному: при електролізі безводного фто-ріда водню (з додаванням фторидів металів для вище-ня електричної провідності) виділяється на аноді фтор негайно реагує з розчиненим або емульгованих в рідини органічною речовиною. Завдяки протіканню ре-акцій в рідкій фазі при перемішуванні досягається хороший тепловідвід і існують широкі можливості регулювання процесу. При цьому не доводиться попередньо отримувати і очищати молекулярний фтор, який все одно справляють в промисловості методом електролізу. Найкращі результати електрохімічне фторування дає при синтезі перфторзамещенних карбонових кислот, простих і складних ефірів, амінів, сульфідів та інших з'єднань, розчинних в рідкому фториді водню.