Дефект аортолегочного перегородки - внутрішньоперикардіальний сполучення між висхідною аортою і легеневою артерією (ЛА). Порок рідкісний - 0,2-0,3% випадків всіх вроджених вад серця (ВПС). Вперше дана аномалія описана Elliotson в 1830 р
Ембріологія. У виникненні дефекту аортолегочного перегородки провідна роль належить зупинки росту і відсутності розвитку аортолегочного перегородки. Поділ примітивного, або ембріонального, артеріального стовбура на висхідну аорту і легеневий стовбур здійснюється за рахунок утворення первинної артеріальної перегородки, яка виникає дистально, і проксимально - за рахунок зростання трункальной перегородки (між 6-7 тижнями внутрішньоутробного життя). У разі порушення цього процесу виникає дефект аортолегочного перегородки.
Патолого-анатомічними критеріями цього пороку є наявність повідомлення междусмежнимі відділами висхідної аорти і легеневого стовбура; присутність двох відокремлених фіброзних кілець аортального та легеневого клапанів зі сформованими вивідними відділами відповідних шлуночків. Форма, розташування і розміри дефектів можуть бути різні.
У НЦССХ ім. А. Н. Бакулєва РАМН прийнята така класифікація пороку:
1. Дефект знаходиться в середній частині аортолегочного перегородки на достатній відстані від синусів Вальсальви і має виражені краю. ПЛА і лла відходять нормально і дистальніше верхнього краю дефекту.
2. Власне аортолегочного вікно, распололсепное безпосередньо над синусами Вальсальви.
3. Дефект розташований в дистальної частини аортолегочного перегородки, далеко від синусів Вальсальви. Проксимальна частина перегородки частково сформована. Гілки ЛА відходять в області вершини дефекту.
4. Дефект розташований дистально і захоплює область відходження ПЛА так, що висхідна аорта повідомляється як з ЛА, так і з ПЛА.
5. Повністю відсутня аортолегочного перегородка, гілки ЛА відходять від задньої стінки загального судини, але клапани аорти і ЛА розвинені нормально. Наявність останнього фактора і відсутність ДМШП дозволяє диференціювати даний порок від загального артеріального стовбура.
Зазвичай зустрічається один, рідше два дефекту, може зустрічатися комбінація з іншими ВПС: відкритою артеріальною протокою (ОАП), транспозицией магістральних судин (ТМС), подклапанного стенозом аорти та ін.
Гемодинаміка. Порушення гемодинаміки схожі з такими при ОАП. Великий скидання крові з аорти в ЛА веде до МКК і перевантаження лівих відділів серця, а при ЛГ - і ПЖ. Величина а / в скидання крові визначається розмірами дефекту і співвідношенням судинних опорів обох кіл кровообігу. При великому діаметрі дефекту Л Г спостерігається з народження дитини, і пов'язано це з передачею високого тиску з аорти, а при низькому розташуванні дефекту - з передачею сили вигнання лівого шлуночка на судини легенів.
При цьому пороці спостерігається три типи реакцій судин МКК на масивний а / в скидання крові:
I тип-нормальна або кілька уповільнена фізіологічна інволюція легеневих судин після народження дитини з поступовим зниженням ОЛС і збільшенням а / в скидання крові. При цьому виявляється гіперволемічна форма ЛГ.
II тип - з розвитком рефлекторного спазму легеневих судин виявляється змішана форма ЛГ.
III тип - відсутність фізіологічної інволюції легеневих судин після народження -вроджені склеротична форма ЛГ.
Кожен тип реакції легеневих судин залежить від індивідуальних особливостей організму. При I типі можна очікувати порівняно пізній розвиток поширених склеротичних змін (в юнацькому і більш пізньому віці). При II типі зміни в легеневих судинах розвиваються раніше, тому навіть у дітей молодше двох років можна спостерігати залишкову Л Г після корекції вади, обумовлену наявністю склеротичних змін в частині легеневих судин.
Діагностика пороку важка і вимагає застосування спеціальних методів дослідження, так як при невеликих розмірах аортолегочного повідомлення клініка його подібна до клінікою ОАП, а при великих - ДМШП, ускладненого високою ЛГ.
Клініка. Діти відстають у фізичному розвитку, бліді, часто хворіють на ГРЗ і пневмоніями, швидко втомлюються. Іноді при плачі у немовляти виявляється ціаноз носогубного трикутника за рахунок зворотного скидання крові. Виражені явища НК.
У зв'язку з наявністю ЛГ рано розвивається гіпертрофія серця, що призводить до утворення «серцевого горба». При невеликому а / в скиданні крові в другому-третьому міжребер'ї зліва від грудини може пальпувати систолічний тремтіння.
А у с кул'таті в на я картина залежить від величини скидання крові. При невеликих розмірах повідомлення вислуховується сістолодіастоліческій шум в третьому-четвер-тому межреберьях, який виявляється лише в 9-15% випадків.
Найчастіше вислуховується неголосний систолічний шум у другому-третьому, рідше в четвертому міжребер'ї зліва від грудини. На ФКГ він займає 1 / 3-2 / 3 систоли. I тон нормальний або кілька посилений на верхівці. II тон великий, нерасщеплен-ний. Може бути систолічний тон вигнання. Іноді на ЛА фіксується низькоамплітудних регресний протодиастолический шум Грехема Стілла відносної недостатності клапана ЛА.
У хворих з високою ЛГ склеротичній форми, частіше в 3-й декаді життя, в різній мірі виражений ціаноз, що з'являється при найменшому фізичному навантаженні, що пояснюється зростанням ОЛС і розвитком перехресного або зворотного скидання крові; «Серцевий горб». Вислуховується звукова тріада ЛГ: 1) великий іерасщепленний II тон; 2) систолічний тон вигнання; 3) шум Грехема Стілла.
ЕКГ. Електрична вісь нормальна або відхилена вправо. У немовлят з великим скиданням крові в ЛА переважають ознаки гіпертрофії ЛШ, а ознаки гіпертрофії ПЖ мінімальні або відсутні. Це може служити непрямою ознакою, що дозволяє диференціювати дану патологію з ДМШП. У старших дітей виражена диаст-вої перевантаження ЛШ і систолічна - ПЖ.
При зменшенні а / в скидання крові відзначається гіпертрофія обох шлуночків, більшою мірою правого. Однак збереження глибоких зубців Qv6 є показником хорошого легеневого кровотоку.
Рентгенологічна картина неспецифічна: посилений легеневий малюнок за рахунок артеріального, рідше венозного русла, серце збільшене за рахунок обох шлуночків і Л П. Судинний пучок завжди розширено, вибухає дуга ЛА, нерідко стовбур і гілки ЛА різко розширені. Висхідна аорта може бути нормальною, але у 50% хворих розширена, пульсація її посилена. Посилено пульсація стовбура ЛА, нерідко пульсують і коріння легенів.
У старших дітей і дорослих зі збільшенням ОЛС відзначається збіднення легеневого малюнка на периферії поряд з розширеними корінням легких. Серце невелике. При розвитку НК серце значно збільшено в розмірах, більше за рахунок правих відділів.
На Ехо КГ в проекції довгої осі видно дефект аортолегочпой перегородки. Даний метод дозволяє встановити локалізацію дефекту, його розміри, виключити супутні вади серця.
Катетеризація серця дозволяє встановити величину і напрямок скидання крові, ступінь ЛГ
Для діагностики цінну інформацію дасть проведення катетера з ЛА в висхідну аорту і далі в праву сонну артерію. При виведенні катетера з аорти в ЛА не реєструється тиск ПЖ. Цим виключається проходження катетера через ДМШП.
Найбільш точним діагностичним методом є аортография. На апгіограммах контрастну речовину з висхідної аорти безпосередньо потрапляє в стовбур ЛА над півмісяцевими клапанами аорти (рис. 2).
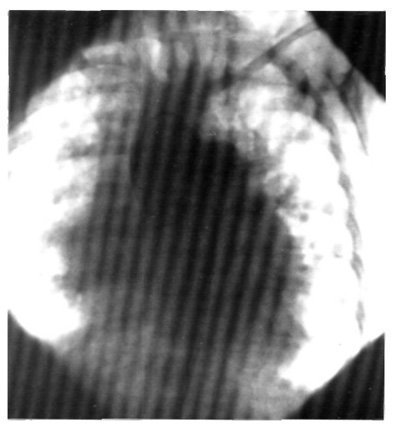
Мал. 2. аортограмме хворий з діагнозом: дефект аортолегочного перегородки.
Прогноз залежить від розмірів повідомлення. При діаметрі повідомлення більше 10 мм прогноз серйозний. Приблизно 25-30% хворих помирають протягом перших 6-ти місяців життя, близько 15% - в шкільному віці. У літературі є лише поодинокі повідомлення про пацієнтів, що дожили до 40 років (Yeatner R. et al. 1962). Середня тривалість життя - 14 років.
Єдиний засіб порятунку хворого -Хірургічне лікування, так як випадків спонтанного закриття дефекту аортолегочного перегородки не описано.
Показання до операції будуються тільки з урахуванням ступеня порушення гемодинаміки. Операцію слід виконувати при великому дефекті в ранні терміни - до одного року, в більш старшому віці операція протипоказана лише при склеротичній формі ЛГ.
Хірургічне лікування. Закриті методи корекції вад (перев'язка і розсічення соустя з подальшим ушиванням стінок) в даний час залишені, як і ушивання дефекту в умовах гіпотермії.
У 1957 р II. Shumachcr запропонував виконувати операцію в умовах штучного кровообігу (ІК). В СРСР першу успішну операцію виконав В. І. Буракопскій в 1965 р
Закриття дефекту в умовах ІК здійснюється шляхом ушивання або пластики дефекту доступами через просвіт ЛЛ або аорти, або з обох сторін. В даний час операція проводиться в умовах ІК, гіпотермії - 20-24 ° С і фармакохолодового кардіоплсгіі (ФХКП) з використанням трансаортального доступу, який дозволяє чітко бачити краю дефекту, гирла коронарних артерій і стулки аортального клапана. Після серединної стернотомии і підключення апарату ІК з введенням артеріальної канюлі вище соустя виділяють праву і ліву ЛА і беруть їх в турнікети.
Після початку охолодження перетискають їх турнікетами щоб уникнути переповнення легенів кров'ю. Кардіоплегії проводять в корінь аорти або окремо в коронарні артерії. Невеликі дефекти вшивають безперервним дворядним швом, а великі закривають ксеноперікардіальной або синтетичної латкою, що фіксується безперервним швом.
Після операційна летальність залишається високою - 15-20%.
Віддалені результати залежать від ступеня ЛГ. За даними НЦССХ ім. А. Н. Бакулєва РАМН, операція призводить до поліпшення стану і практичного одужання 65,2% пацієнтів. Зниження тиску в Лау хворих з високою Л Г настає лише у хворих з ОЛС до операції не вище 10 од.