До групи легких металів, що мають щільність менше 5 г / см, входять Al, Mg, Ti, Be, Ca, В, Zn, К та ін. Найбільше промислове застосування з них мають алюміній, магній, титан.
Алюміній є найпоширенішим металом в земній корі. Він переважно зустрічається у вигляді сполук з киснем і кремнієм алюмосиликатов. Для отримання алюмінію використовують руди, багаті глиноземом AI2O3. Найчастіше застосовують боксити, в яких міститься,%: Аl2 О3 40-60, Fе2 О3 15-30, SiO2 5-15, ТiO2 2-4 і гідратної вологи 10-15.
Технологічний процес виробництва алюмінію складається з трьох етапів: вилучення глинозему з алюмінієвих руд, електроліз розплавленого глинозему з отриманням первинного алюмінію та його рафінування. Витяг глинозему зазвичай виробляють лужним способом, застосовуваним в двох варіантах: мокрому (метод Байєра) і сухому.
При мокрому методі боксити сушать, подрібнюють і завантажують в герметичні автоклави з концентрованою лугом, де витримують протягом 2-3 год при температурі 150 ... 250 ° С і тиску до 3 МПа. При цьому протікають реакції взаємодії гідроксиду алюмінію з їдким натром:
Розчин алюмінату натрію Nа2 Про • А12 Про у вигляді гарячої пульпи йде на подальшу переробку. Оксиди заліза, титану та інші домішки, які не розчиняються в лугах, випадають в осад-шлам.
Кремнезем також взаємодіє з лугом і утворює силікат натрію: SiO2 + 2NaOH = Na2 O • SiO2 + 4Н2 О, який, в свою чергу, взаємодіючи з алюмінатом натрію, випадає в осад, утворюючи нерозчинний з'єднання Na2 O · AI2 O3 · 2SiO2 · 2Н2 Про .
Пульпа після фільтрації і розведення водою зливається у відстійник, де з алюмінатного розчину випадає в осад гідроксид алюмінію:
Гідроксид алюмінію фільтрують і прожарюють при температурі до 1200 ° С в трубчастих обертових печах. В результаті виходить глинозем:
Сухий лужний спосіб або спосіб спікання складається в спільному прожаренні при температурі 1200 ... 1300 ° С суміші бокситу, соди і вапна, що приводить до утворення спека, в якому міститься водорозчинний алюмінат натрію:
Вапно витрачається на освіту нерозчинного у воді силікату кальцію СаО • SiO2. Алюмінат натрію витравлюють з спека гарячою водою і отриманий розчин продувають вуглекислотою:
Осад промивають і прожарюють, отримуючи глинозем, як і в попередньому способі.
Алюміній отримують електролізом глинозему, розчиненого в розплавленому кріоліті Na3 AlF6. Цей метод був запропонований в 1886 р одночасно Ч.Холлом в США і П.Еру у Франції і застосовується до цих пір майже без змін. Криоліт отримують в результаті взаємодії-дії плавикової кислоти HF з гідроксидом алюмінію з подальші-щей нейтралізації содою: 6HF + А1 (ОН) 3 = Н3 АlF6 + ЗН2 Про;
Електроліз здійснюють в алюмінієвій ванні-електролізері, схема якого наведена на рис. 2.5.
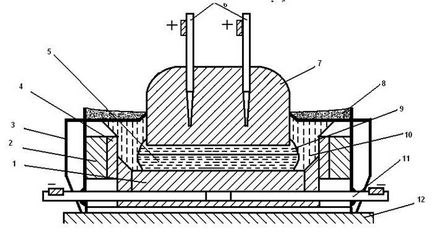
Мал. 2.5. Схема електролізера для виробництва алюмінію:
1 - катодні вугільні бло-ки; 2 - вогнетривка футеровка; 3 - сталевий кожух; 4 - вугільні плити; 5 - рідкий алюми-ний; 6 - металеві стрижні з шинами; 7 - вугільний анод; 8 - глинозем; 9 - рідкий елект-Роліт; 10 - кірка затверділої електроліту; 11 - катодна токо-підводить шина; 12 - фундамент
Ванна має сталевий кожух прямокутної форми, а її стіну і подину виготовляють з вугільних блоків, теплоізольованих шамотною цеглою. У футерування поду вмонтовані сталеві катодні шини, завдяки чому вугільний корпус ванни є катодом електролізера. Анодами служать самообжігающіеся, вертикально розташовані вугільні електроди, занурені в розплав. При електролізі аноди поступово згоряють і переміщаються вниз. У міру згоряння вони нарощуються зверху рідкої анодної масою, з якої при нагріванні видаляються леткі і відбувається її коксування. Електроліт нагрівається до робочої температури 930-950 ° С. Глинозем, що витрачається в процесі електролізу, періодично завантажують у ванну зверху. Завдяки охолодженню повітрям на поверхні утворюється кірка електроліту. На бічній поверхні ванни утворюється твердіє шар електроліту (гарнісажу), пре-дохраняет футеровку від руйнування і теплоізолюючий ванну. При високій температурі глинозем AI2 O3. розчинений в електроліті, дисоціює на іони: А12 О3 = 2А1 3+ + O 2 На поверхні вугільної подини, що є катодом, іони відновлюються до металу: 2Al 3+ + 6e = 2al
У міру зменшення вмісту глинозему в електроліті його періодично завантажують у ванну електролізера. Рідкий алюміній накопичується на подине електролізера і періодично видаляється за допомогою вакуумних ковшів.
Кисневі іони розряджаються на вугільному аноді: 3O 2 6e = 3 / 2O2. окислюють анод, утворюючи СО і СО2. які видаляються вентиляційними пристроями. Електролізних ванни з'єднують послідовно в серії з 100-200 ванн.
Первинний алюміній, отриманий в електролізної ванні, забруднений домішками Si, Fe, неметаллическими включеннями (AI2 O3, С), а також газами, переважно воднем. Для очищення алюмінію його піддають рафінування або хлоруванням, або електролітич-ським способом.
Більш чистий алюміній отримують електролітичним рафінуванням, де електролітом є безводні хлористі і фтористі солі. У розплавленому електроліті алюміній піддають анодному розчиненню і електролізу. Електролітичним рафінуванням отримуютьалюміній чистотою до 99,996%, споживаний електричної, хімічної і харчовою промисловістю. Ще більш чистий алюміній (99,9999%) можна отримати зонної плавкою. Цей спосіб дорожче електролізу, мало продуктивний і застосовується для виготовлення
невеликих кількостей металу в тих випадках, коли необхідна особлива чистота, наприклад для виробництва напівпровідників.