В. С. Власова. учитель інформатики МОУ СЗШ №1 м Карабаша
С. В. Кувшинникова. учитель хімії МОУ СЗШ №1 м Карабаша
білки # 151; природні високомолекулярні речовини
Хімічні властивості білків
- Сформувати знання про склад і будову білків як вищого ступеня розвитку речовини.
- Сформувати знання про хімічні властивості білків.
- Розвиток умінь і навичок складання схем хімічних реакцій.
- Навчитися підтверджувати хімічні властивості білків експериментально, вирішувати завдання, які пов'язують хімію з біологією і медициною.
устаткування:
яєчний білок, розчин сульфату міді (II) і луги, концентрована азотна кислота, етанол, сіль заліза, вода, спиртівка, пробірки.
- усне опитування;
- робота на комп'ютері зі складання структурно-логічної схеми;
- хімічний диктант.
Перехід до вивчення нового матеріалу Значення амінокислот велике, так як з них побудовані молекули білків, які відіграють найважливішу рол в життєвих процесах.
В організмі людини і тварини білки під впливом (А) піддаються (Б), в результаті утворюються (В), які використовуються організмом для синтезу власних специфічних (Г).
(Відповідь учні дають після вивчення нового матеріалу) Орієнтовно-мотиваційний етап
- Білки, функції білків.
Основою живого організму, носіями спадкових ознак, є білки. З білками пов'язані всі життєві процеси.
Білки виконують різноманітні функції:
Які білки є біологічними каталізаторами?
Білкову природу мають численні ферменти, які каталізують реакції певного типу ферментів властива висока вибірковість, найбільша активність при нормальній температурі організму, залежність ферментної активності від рН.
Операційно-виконавський етап
- Склад і будова білків.
Розглянемо зображення чотирьох структур білка:
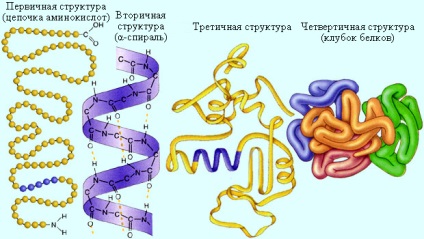
-
питання:
- Які хімічні елементи входять до складу білків?
- Використовуючи матеріал уроку хімічні властивості амінокислот, вкажіть які зв'язки у вторинній структурі білка? (Підручник О. С. Гібріелян. Хімія-10).
Складаємо схему № 3. Уявлення про структуру поліпептидного ланцюга в білках розробив Полінг Лайнус
-
питання:
білки # 151; високомолекулярні сполуки, що утворюються в результаті зв'язування окремих поліпептидних ланцюгів водневими зв'язками. Всі білки підрозділяються на глобулярні (розчинні у воді) і фібрилярні (нерозчинні у воді). Глобулярні білки компактні, мають сферичної і наближеними до неї формами. Глобулярний білок діаметром 2,5 нм є поліпептидний ланцюг довжиною до 50 нм, згорнуту в клубок. Фібрилярні білки зазвичай витягнуті і входять до складу тканин, м'язів, волосся.
- Хімічні властивості білків.
Хімічні властивості розглядаються з опорою на будову білків (учитель демонструє на столі, учні кожен на своєму робочому місці).
Схожі статті