Природжений синдром Нунан є наслідком стимуляції RAS-MAPK шляху і характеризується мультисистемним поразкою
Синдром Нунан є аутосомно-домінантне, вариабельно експрессіруемим мультисистемні захворювання з передбачуваною поширеністю 1 випадок на 1000-2500 осіб. Вперше згадав про нього Кобилинський в 1883 році.
Хвороба описана Жаклін Нунан, що повідомила про дев'ять пацієнтів зі стенозом клапана легеневої артерії, малим зростом, гіпертелоризм, помірним зниженням інтелекту, птозом, крипторхізм і скелетними порушеннями. Доктор Нунан, практикувати як дитячий кардіолог в університеті Айови, помітила, що у дітей з рідкісним типом пороку серця - стенозом клапана легеневої артерії - часто спостерігалися типові фізичні аномалії у вигляді малого росту, крилоподібні шиї, широко посаджених очей і низько розташованих вух. Хлопчики і дівчатка дивувалися однаково. Доктор Джон Опіц, колишній студент Нунан, першим ввів у вжиток термін "синдромом Нунан" для характеристики стану дітей, у яких відзначалися ознаки, схожі на описані Нунан. Пізніше Нунан написала статтю "гипертелоризм з фенотипом Турнера" і в 1971 році на Симпозіумі серцево-судинних захворювань назву "синдром Нунан" стало офіційно визнаним.
RAS-MAPK шлях - дуже важливий шлях сигнальної трансдукції, через який позаклітинні ліганди - певні фактори росту, цитокіни і гормони - стимулюють клітинну проліферацію, диференціювання, виживання і метаболізм (рисунок 1). Після зв'язування ліганда рецептори на поверхні клітин фосфорилюються в місцях їх ендоплазматичного регіону. Це зв'язування задіє адаптерні протеїни (наприклад, GRB2), які формують конститутивний комплекс з факторами обміну гуанінових нуклеотидів (наприклад, SOS), конвертують неактивний ГДФ- пов'язаний RAS в його активну ГТФ-пов'язану форму. Активовані RAS-протеїни потім активують RAF-MEK-ERK каскад через ряд реакцій фосфорилювання. В результаті активоване ERK проникає в ядро для зміни транскрипції цільових генів і коригує активність ендоплазматичний мішеней для індукції адекватних короткочасних і тривалих клітинних відповідей на стимул. Всі гени, залучені в синдром Нунан, кодують інтегральні для цього шляху протеїни. і мутації. що викликають хворобу, зазвичай підсилюють сигнал, що проходить через цей шлях.
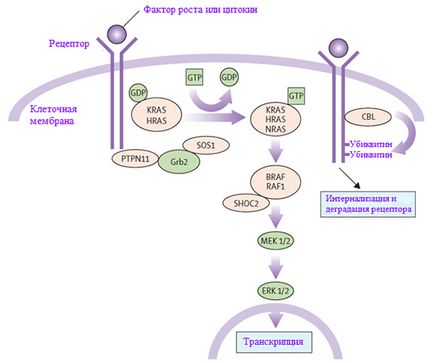
Малюнок 1. RAS-MAPK сигнальний шлях. Ростові сигнали передаються з активованих фактором зростання рецепторів до ядра. Мутації в PTPN11, KRAS, SOS1, NRAS і RAF1 асоційовані з синдромом Нунан, а мутації в SHOC2 і CBL асоційовані з подібним синдрому Нунан фенотипом.
Ознаки та симптоми
Приблизно у 10% хворих спостерігається слуховий дефіцит в низькочастотному діапазоні, викликаний перцептивної приглухуватістю. і у 25% - в високочастотному діапазоні. Вони пов'язані, зокрема, із структурними аномаліями внутрішнього вуха, включаючи аномалії скроневої кістки.
Синдром Нунан - друга за поширеністю синдромная причина вродженої вади серця, яку випереджає лише трисомия 21. Синдром проявляється декількома серцево-судинними фенотипами. Найбільш поширеним є стеноз легеневого стовбура, часто з диспластическими клапанамі- (50-60%), гіпертрофічна кардіоміопатія (20%) і потім - дефект міжпередсердної перегородки (6-10%), рідше спостерігаються дефект міжшлуночкової перегородки, стеноз периферичного відділу легеневого стовбура, передсердно-шлуночковий канал, аортальнийстеноз. аномалії мітрального клапана, звуження аорти і аномалії коронарних артерій. Гіпертрофічна кардіоміопатія може бути легкої або важкої форми і спостерігається з пренатального до підліткового віку. Майже 25% пацієнтів помирають внаслідок серцевої недостатності на першому році життя, хоча частота раптової смерті нижче, ніж при сімейної гіпертрофічної кардіоміопатії.
Електрокардіограми часто показують широкі QRS-комплекси з переважно негативним патерном в лівих грудних відведеннях і відхилення електричної осі вліво з гігантською Q-хвилею, іноді навіть при нормальній структурі серця і грудної стінки. З синдромом Нунан асоційовані цереброваскулярні аномалії: артеріовенозні мальформації, аневризми. гіпоплазія задніх судин і хвороба моя-моя.
Можлива аномальна пігментація: множинні пігментні невуси, плями кави-з-молоком і лентіго. Часто спостерігається keratosis pilaris плечей і обличчя може перешкоджати росту волосся і брів. Волосся часто густі і кучеряве, хоча тонкі, рідке волосся також описані.
Маса і зріст при народженні зазвичай нормальні. Низький зріст - характерний прояв синдрому Нунан, хоча зростання дорослих пацієнтів не завжди змінюється. Оскільки пубертатний сплеск росту часто порушується або затримується, превалювання низького зросту при синдромі Нунан найбільш виражено під час пубертатного періоду.
Крім того, старіння скелета затримується. У пізні роки підліткового періоду зростання пацієнтів посилюється. У хворих може спостерігатися нестача гормону росту, нейросекреторна дисфункція і резистентність до гормону росту. Пацієнти з PTPN11-асоційованим синдромом Нунан часто мають нормальні або трохи підвищені концентрації гормону росту і низькі концентрації IGF1. Експериментальні моделі синдрому Нунан Ptpn11 демонструють активацію ERK у відповідь на гормон росту - потенційну причину низького зросту і багатообіцяючу мішень для лікування. Динаміка зростання значно поліпшується при ERK1 / 2-ингибировании.
Початок пубертатного періоду затримано у хворих синдромом Нунан в порівнянні з населенням в цілому; 35% хлопчиків вступають в пубертатний період з 13,5-річного віку і 44% дівчаток - з 13-річного. Дорослі можуть піддаватися ризику порушення остеогенезу, асоційованого з чоловічим гіпо- естрогенізмом і результуючої підвищеною резорбцією кісток. Більшість немовлят з синдромом Нунан мають труднощі з харчуванням, які можуть вести до затримки росту. Спостерігається погане смоктання материнських грудей, подовжене час годування або рецидивуюча блювота; приблизно 25% немовлят повинні харчуватися через зонд протягом перших двох тижнів життя або довше. Гастроезофагеальний рефлюкс також звичайний. Ці симптоми зникають у дітей з найважчою формою на 15-му місяці життя. Зафіксовані порушення ротації кишечника, його незріла рухливість і затримка розвитку шлунково-кишкової моторики.
80% хлопчиків з синдромом Нунан мають одно- або двосторонній крипторхізм. Може спостерігатися дисфункція чоловічих гонад, викликана порушенням функції клітин Сертолі, а не крипторхізм. Фертильність жінок з синдромом Нунан не порушена. У 10% пацієнтів з синдромом Нунан є аномалії нирок. але більшість з них не потребує лікування.
Хоча немовлята з синдромом Нунан схильні до кількох гематологічним аномалій, включаючи тимчасовий моноцитоз, тромбоцитопенія і мієлопроліферативні захворювання, найбільш поширеними гематологічними порушеннями є кровотечі внаслідок дефектів коагуляції.
Лімфатичні аномалії, зазвичай периферичний лімфоїдний набряк, присутні приблизно у 20% індивідуумів. Периферичний лімфоїдний набряк може спостерігатися у немовлят і проходить в перші роки життя, але він іноді виникає і в пубертатному або дорослому періоді. Рідше спостерігаються водянка плода; пульмонарие, тестикулярні або кишкові лімфангіектазіі; хілезний випоти в плевральну і черевну порожнину; гипопластические лімфатичні судини ніг; аномальні лімфатичні судини грудної клітини; аплазія або відсутність грудного протока; гипопластические пахові і клубові лімфатичні судини; лімфоїдний набряк мошонки або вульви.
Множинні гігантоклітинні поразки асоційовані з синдромом Нунан, викликаним мутаціями в PTPN11 або SOS1. Пігментований віллонодулярний синовит - пролиферативное синовиальное ураження суглобів, сухожиль і сумки - часто спостерігається у хворих синдромом Нунан. Приблизно у 30% дітей є спінальна деформація, і хірургічне втручання рекомендується в двох з трьох випадках. Також описані деформація грудної клітки і широко розташовані соски (cubitus valgus і genu valgum).
Хворі синдромом Нунан схильні до ряду гематологічних неоплазій, особливо в дитинстві, включаючи ювенільний мієломоноцитарний лейкемію, гостру мієлогенну лейкемію і В-лімфоцитарна гостру лімфообластную лейкемію. Мієлопроліферативні порушення у хворих синдромом Нунан і ювенільний мієломоноцитарна лейкемія зазвичай не так яскраво виражені, як у пацієнтів з ювенільної мієломоноцитарний на лейкемію.
Ембріональна рабдоміосаркома (дванадцятипалої кишки, сечового міхура, сечового протоку, очниці, піхви і черевної порожнини), як правило, асоціюється з SOS1-герменатівной мутацією. Можуть спостерігатися і інші пухлини: гранулярноклеточная пухлина, пілоцітарной астроцитома, пухлина з клітин Сертолі в кріпторхіческом яєчку, нейробластома, інші гліальні пухлини (асоційовані з PTPN11-гермінативної мутацією). Патогенні мутації PTPN11 ведуть до п'ятикратного збільшення ризику розвитку раку. Описано також випадки злоякісного мастоцитоз і злоякісної епітеліоподібно ангіосаркоми.
У 95% хворих спостерігається, щонайменше, одна типова аномалія очей: косоокість, помилки рефракції, амбліопія або ністагм. Дві третини пацієнтів мають ураження передньої камери ока, включаючи катаракту, а 20% пацієнтів - зміни очного дна, включаючи друзи і гіпоплазію диска зорового нерва, колобоми і мієлінові нерви.
Більшість характерних рис синдрому Нунан можуть бути наслідком обструкції або дисфункції лімфатичної системи в період розвитку, включаючи стрічкову шию і виступання трапецієподібних м'язів, крипторхізм. широко розташовані соски, низько розташовані і ротирована назад вуха, гипертелоризм і птоз. Інші особливості синдрому Нунан включають вроджені пороки серця, superior pectus carinatum з inferior pectus excavatum, затримку в розвитку, низький зріст і лімфатичні дисплазії. Риси обличчя, асоційовані з синдрому Нунан, змінюються з віком (таблиця 1, рисунок 2).
Таблиця 1. Типові риси обличчя у хворих синдромом Нунан по віковим групам
Пренатальні риси неспецифічні, але включають многогідрамніон, гідронефроз, плевральнийвипіт, набряк, дефекти серця, розширені яремні лімфатичні мішки, кістозна гігро і підвищену прозорість в потиличній області. Для плода з нормальними хромосомами синдром Нунан з потиличних набряком діагностується приблизно в 1-3% випадків в першому триместрі і з кістозної гігрома - у 10% плодів, у другому триместрі.

Малюнок 2. П'ять генерацій сім'ї з синдромом Нунан, викликаним мутацією SOS1. Розрізнення рис обличчя стає більш м'яким з віком.
Таблиця 2. Кореляції між генотипом і фенотипом в синдромі Нунан *
Лікування і диференційний діагноз
Рекомендації з лікування синдрому Нунан описані в таблиці 3. Хоча характерні риси обличчя і інші ускладнення, асоційовані з подібними синдрому Нунан порушеннями, однотипні синдрому Нунан, мутації в двох інших генах - SHOC2 і CBL - асоційовані з додатковими функціями і не спостерігаються при синдромі Нунан.
Таблиця 3. Рекомендації з лікування
У період винесення діагнозу
Повний физикальное і неврологічне обстеження; консультація медичного генетика для підтвердження діагнозу, можливо молекулярно-генетичне тестування і генетичне консультування
Щорічне повне фізикальне і неврологічне обстеження; повторне генетичне тестування при негативному генотипі або для мультисистемного дослідження; генетичне консультування підлітків або молодих дорослих
Орхопексія у віці 1 рік при крипторхізмі; при наявності лимфоидного набряку - звернення в спеціалізовану клініку; при підвищенні внутрішньочерепного тиску - МРТ головного мозку і шийного відділу спинного мозку; при підозрі на судоми - електроенцефалограма і напрямок до невролога
Мультидисциплінарна оцінка розвитку
Щорічний скринінг розвитку для дітей у віці 5-18 років
Тестування у нейропсихолога, якщо скринінг виявив аномалії; раннє втручання, якщо затримка виявляється до трьох років; індивідуальний план навчання для дітей у віці 5-18 років з затримкою розвитку