Дане завдання легко вирішується із застосуванням рівняння Менделєєва-Клапейрона
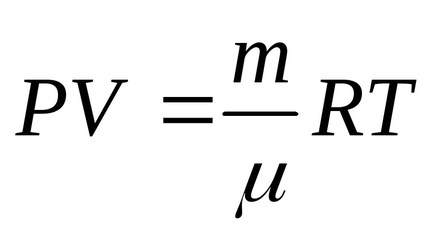
Запишемо його для першого стану газу:
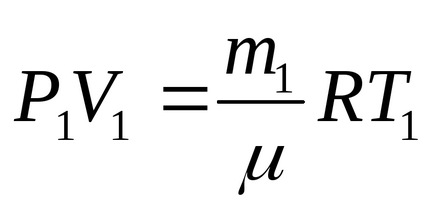
І для другого стану (коли частина газу випущена):
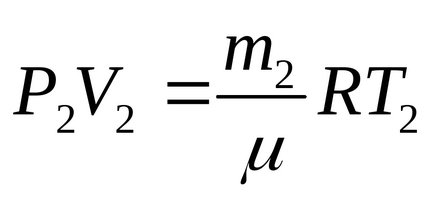
Вважаємо, що розмір балона не змінюється, отже, процес Ізохоричний V1 = V2 = V. Врахуємо також, що Т2 = Т1 -8, аm2 = m1 -0,4m1 = 0,6m1.
Поділимо рівняння (2) на рівняння (1):
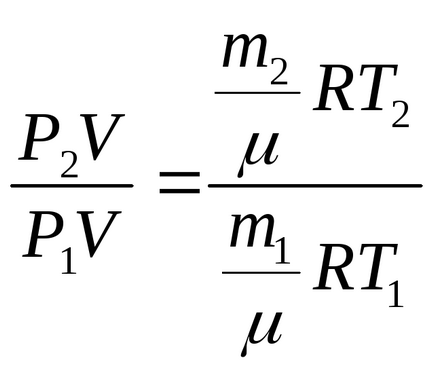
Відповідь: тиск зменшиться в 1,72 рази.
Кисень массойm = 2 кг займає об'емV1 = 1 м3і знаходиться під тиском Р1 = 2,02 ∙ 105Па. Газ був послідовно нагрітий при постійному тиску до об'емаV2 = 3 м3, а потім при постійному обсязі до тиску Р3 = 5 ∙ 105Па. Знайти зміну внутрішньої енергії ΔU, роботу газу А і передане газу кількість теплотиQ.
Зміна внутрішньої енергії ΔUнаходітся за формулою:
де μ-молярна маса кисню, а i- число ступенів свободи. Так як кисень в нормальних умовах - двухатомная молекула, отже, i = 5.
Повна зміна внутрішньої енергії буде залежати тільки від різниці початкової і кінцевої температури Т1 і Т3. які знайдемо через рівняння Менделєєва-Клапейрона
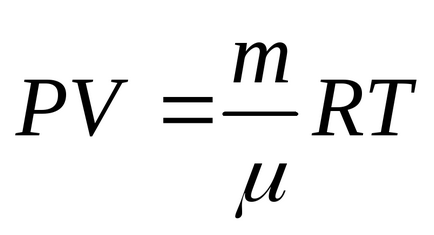
Підставляючи в (2) відповідні значення Р і V, отримаємо значення температури:
Підставляючи в (1) числові значення величин, отримуємо:
Робота газу дорівнюватиме сумі робіт газу на кожній дільниці: А = Аізоб + Аізохор. Робота газу в Ізохоричний процесі дорівнює 0, отже,
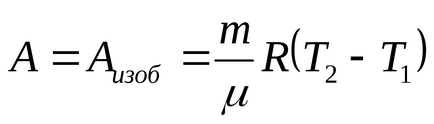
Температуру Т2 знайдемо за формулою (2):
Проведемо розрахунок за формулою (3) і отримаємо значення роботи:
Відповідно до першого початку термодинаміки, кількість теплоти Q, отримане газом, дорівнює сумі роботи А, досконалої газом, і зміни внутрішньої енергії ΔU:
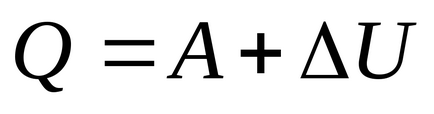
Провівши обчислення, отримаємо: (Дж).
Відповідь: ΔU = 3,25 МДж, А = 0,4 МДж, Q = 3,65 МДж.
Теплова машина робить роботу по циклу Карно. Температура нагрівача Т1 = 230ºС, холодильника Т2 = 300 К, причому холодильник цієї теплової машини служить нагрівачем інший теплової машини. У якій з машин ККД більше і у скільки разів, якщо різниця температур нагрівача і холодильника у обох машин однакова?
При опусканні гарячого металевого бруска відбувається передача деякої кількості теплоти Qмаслу і калориметр. При цьому брусок охолоджується до температури Т3. а масло і калориметр нагріваються до Т3. Вважаючи, що система ізольована від зовнішніх джерел тепла, складемо рівняння теплового балансу:
де Q1 - кількість теплоти, що віддається сталевим бруском, Q2 - кількість теплоти, що отримується калориметром, аQ3 - кількість теплоти, що отримується маслом. Масу масла знайдемо через значення обсягу і щільності:
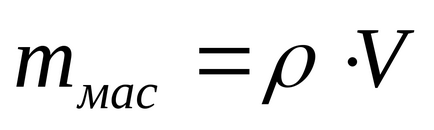
Запишемо рівняння (1) з урахуванням виразів для Q1, Q2, Q3 і (2):
,
звідки висловимо СМАС:
.
.
Відповідь: питома теплоємність масла дорівнює СМАС = 2 кДж / (кг ∙ К).
Визначити зміну ентропії ΔSпрі ізотермічному і изобарном розширенні азоту массойm = 100 г від обсягу 20 л до 148 л.
Вираз для знаходження ентропії:
а) При ізотермічному процесі Т = const, отже, її виносимо за знак інтеграла. Тоді (1) стосовно до ізотермічного процесу набуде вигляду:
В ізотермічному процесі
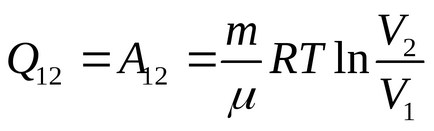
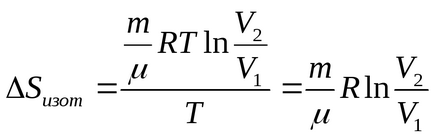
Проведемо обчислення: (Дж / К).
б) У изобарном процесі Р = const, а
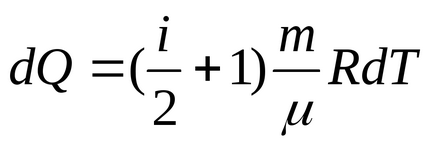
Так як в изобарном процесі зміна температури пропорційно зміні обсягу
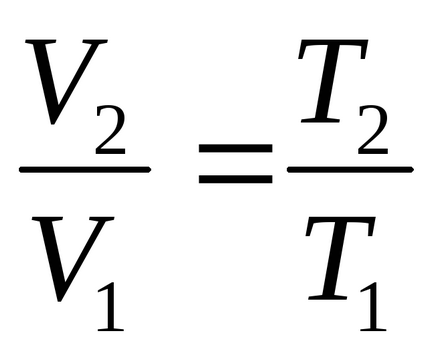
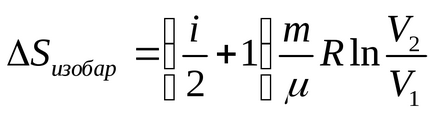
Проведемо обчислення: (Дж / К).
Відповідь: зміна ентропії в ізотермічному процесі ΔSізот = 59,4 Дж / К, а в изобарном - ΔSізобар = 207,75 Дж / К.