Виходячи з положення вуглецю в періодичній системі хімічних елементів Д.І. Менделєєва, охарактеризуйте хімічні властивості оксидів вуглецю.
Відповідно до можливих ступенями окислення атома вуглець утворює два оксиду: оксид вуглецю (II) - чадний газ і оксид вуглецю (IV) - вуглекислий газ.

Завдання. Поясніть механізм утворення хімічних зв'язків в молекулі оксиду вуглецю (II).
Отримання оксидів вуглецю
Оксид вуглецю (II) в промисловості отримують в спеціальних генераторах (рис. 50). Розглянемо найбільш поширений газогенератор шахтного типу. У газогенератор завантажують тверде паливо (кокс), знизу подається дуття:
Склад отриманих генераторних газів залежить від природи окислювача (виду дуття), типу газифікованого палива і режиму процесу. Найбільш багаті оксидом вуглецю (II) водяний (до 36%) і парокіслородной (до 66%) генераторні гази. Перетворення твердого палива в газоподібний називається газифікацією палива.
У лабораторії оксид вуглецю (II) СО отримують з мурашиної кислоти при нагріванні в присутності концентрованої сірчаної кислоти як водовіднімаючих кошти:
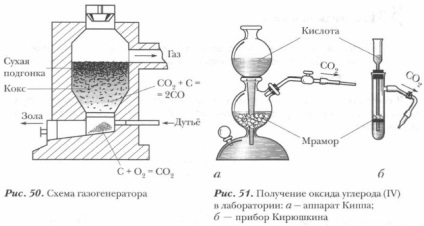
У лабораторії ж оксид вуглецю (IV) СО2 отримують дією соляної кислоти на тверді карбонати (рис. 51).
Фізичні та хімічні властивості оксиду вуглецю (II)
Оксид вуглецю (II) СО, або чадний газ, - безбарвний газ, без запаху, трохи легший за повітря, погано розчинний у воді. Сильна отрута!
Оксид вуглецю (II) при звичайних умовах досить інертний. Він не взаємодіє з водою, кислотами і лугами, є несолеобразующіе оксидом. Для вуглецю характерна ступінь окислення +4, вона більш стійка, тому оксид вуглецю (II) проявляє відновні властивості:Як відновник він широко застосовується в металургійній промисловості для отримання металів:
Оксид вуглецю (II) горить синім полум'ям з виділенням великої кількості теплоти.