3 методика: Назва іонних соедіненійНазванія багатоатомних соедіненійНазванія ковалентних сполук
Уміння давати назви основних хімічних сполук - необхідна складова успішного вивчення хімії. Дотримуйтесь цього посібника, щоб дізнатися деякі базові правила присвоєння назв хімічних сполук, а також навчитися називати хімічні сполуки, які ви побачили вперше.
Метод 1 з 3: Назва іонних з'єднань
Метод 2 з 3: Назви багатоатомних сполук
- 1 З'ясуйте, що таке багатоатомний з'єднання. Ці сполуки складаються з груп атомів, пов'язаних один з одним, причому вся група має позитивний або негативний заряд. Ви можете виконувати з багатоатомних сполуками три базові операції:
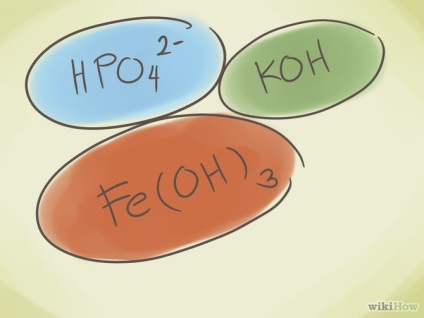
- Додавати атом водню в початок з'єднання. Тоді в початок назви з'єднання додається слово "гідро". Це знижує негативний заряд на одиницю. Наприклад, "карбонат" CO32- перетвориться в "гідрокарбонат" HCO3-.

- Прибирати атом кисню з сполуки. Заряд залишиться таким же, а закінчення назви з'єднання зміниться з "-ат" на "ит". Наприклад: перехід від NO3 до NO2 - це перехід від "нітрату" до "нітриту".

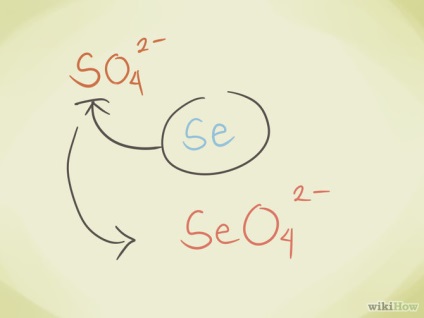
- Замінювати центральний атом іншим з тієї ж групи періодичної системи. Наприклад, сульфат SO42- може стати селенатом SeO42-.
- Додавати атом водню в початок з'єднання. Тоді в початок назви з'єднання додається слово "гідро". Це знижує негативний заряд на одиницю. Наприклад, "карбонат" CO32- перетвориться в "гідрокарбонат" HCO3-.
- 2 Запам'ятайте найбільш часто зустрічаються складні іони. Дані іони - база для формування більшості назв багатоатомних сполук. Вони наведені нижче в порядку зростання негативного заряду:

- Гідроксид-іон: OH-
- Нітрат-іон: NO3-
- Гідрокарбонат-іон: HCO3-
- Перманганат-іон: MnO4-
- Карбонат-іон: CO32-
- Хромат-іон: CrO42-
- Дихромат-іон: Cr2O72-
- Сульфат-іон: SO42-
- Сульфит-іон: SO32-
- Тіосульфат-іон: S2O32-
- Фосфат-іон: PO43-
- Іон амонію: NH4 +
- 3 Складайте назви сполук на основі даного списку. Об'єднайте назву якого-небудь елементу або елементів, пов'язаних зі складним іоном, і назвіть з'єднання. Якщо елемент стоїть перед складним іоном, назва елемента просто ставиться після назви іона.
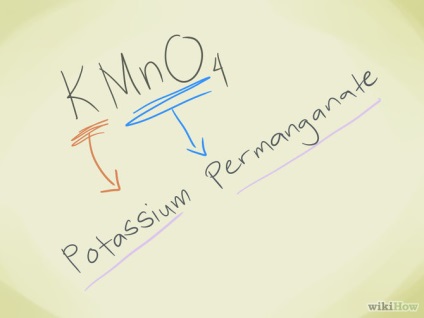
- Приклад: KMnO4. Ми бачимо, що іон MnO4- - це перманганат. K - це калій, тому назва з'єднання - перманганат калію.
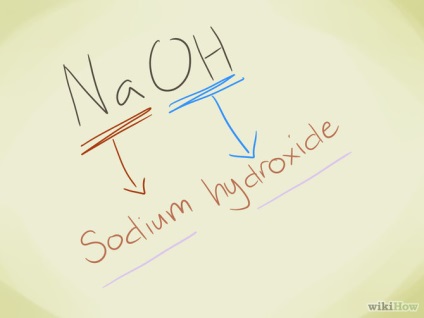
- Приклад: NaOH. Ми бачимо, що OH- - це гідроксид-іон. Na - це натрій, тому назва з'єднання - гідроксид натрію.
- Приклад: KMnO4. Ми бачимо, що іон MnO4- - це перманганат. K - це калій, тому назва з'єднання - перманганат калію.
Метод 3 з 3: Назви ковалентних сполук
- 1 З'ясуйте, що таке ковалентное з'єднання. Ковалентні з'єднання утворюються з двох або більше елементів-неметалів. Ім'я з'єднання базується на кількості присутніх атомів. Додається префікс - це латинське числівник, що характеризує кількість молекул.
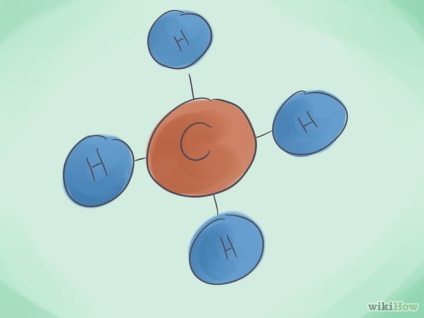
- 2 Вивчіть префікси. Запам'ятайте префікси для позначення кількості атомів від 1 до 8:
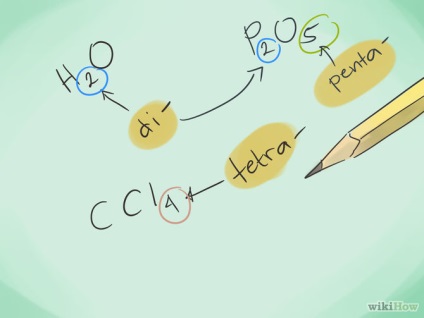
- 1 атом - "Моно-"
- 2 атома - "Ді-"
- 3 атома - "Три-"
- 4 атома - "тетра"
- 5 атомів - "пента-"
- 6 атомів - "гекса-"
- 7 атомів - "гептил"
- 8 атомів - "окта-"
- 3 Називайте з'єднання. Використовуючи відповідні префікси, назвіть нове з'єднання. Ви можете додавати префікс до будь-якої частини з'єднання, в якому є кілька атомів.
- Приклад: CO - це монооксид вуглецю, а CO2 діоксид вуглецю.

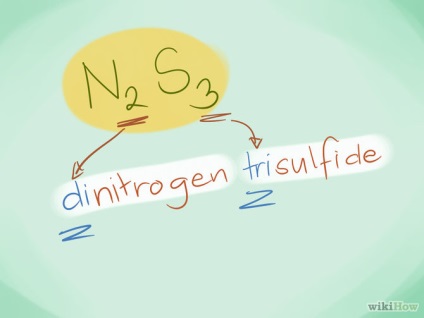
- Приклад: N2S3 - це трисульфід діазота.
- У більшості випадків префікс "моно-" можна не використовувати, оскільки при відсутності префіксів мається на увазі саме він. Однак цей префікс до сих пір використовується для монооксиду вуглецю в зв'язку з використанням цього терміна з часів ранньої хімії.
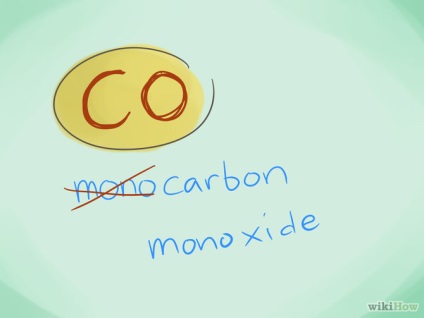
- Приклад: CO - це монооксид вуглецю, а CO2 діоксид вуглецю.
- Звичайно ж, у цих правил є безліч виключень. Наприклад, незважаючи на те, що CaCl2 має два атома хлору, він називається хлоридом кальцію, а НЕ дихлорида кальцію, як можна було б очікувати.
- Також важливо розуміти, що все це не відноситься до органічної хімії.
- Ці правила призначені для людей, які починають вивчати хімію і науку. Коли ви досягнете просунутого рівня, ви дізнаєтеся, що існують інші правила, наприклад правило змінної валентності.