Сівков А.В. Ощепков В.Н. Жорно А.А. Корякін А.В.
Досвід НДІ урології
- удосконалилася техніка імплантації радіоактивних зерен;
- впроваджено планування брахітерапії в режимі реального часу, що дозволило виконувати її більш прецизионно і умень-шити навантаження на критичні органи;
- досягнуто зниження тривалості операції, яка становить від п'ятнадцяти хвилин до півгодини;
- важливим фактором є проведення післяопераційного контрольного планування, що дозволяє оцінити якість проведеного лікування (рисунок 1).
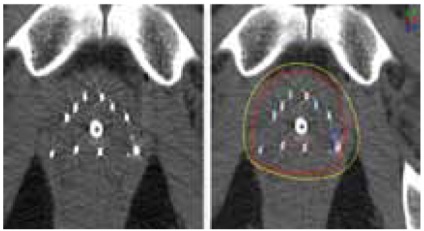
Малюнок 1. Контроль положення зерен за допомогою КТ і післяопераційні дозиметрія
Таблиця 1. П'ятирічні результати застосування брахітерапії в НДІ урології
В даний час під наглядом в НДІ урології складаються понад 230 пацієнтів з РПЗ у віці від 42 до 81 року і терміном спостереження до 11 років.
Необхідно підкреслити важливість відбору хворих. Зокрема, при поділі пацієнтів на групи найгірші результати були отримані у пацієнтів, що мали індекс Глісон 7 і вище (малюнок 2). Така ж тенденція спостерігається для рівня простатичного антигену (ПСА) більше 10 нг / мл (рисунок 3). У своїй практиці ми використовуємо наступні критерії відбору:
- клінічна стадія T1c-T2b;
- рівень ПСА менше 10 нг / мл;
- обсяг ПЖ до 50 см3 (за даними ТРУЗІ) при відсутності вираженої инфравезикальной обструкції;
- показник Глисона менше 7 балів;
- низький ризик екстракапсулярного поширення пухлини, ураження сім'яних пухирців і лімфатичних вузлів за даними МРТ і номограм.
При більших розмірах ПЖ рекомендовано призначення гормональної терапії терміном до 3-х місяців.
Пацієнтам стадій T2b-T3a доцільно комбіноване лікування із застосуванням дистанційної променевої терапії (40 Гр).
Нами було розроблено низку прийомів, що поліпшують результативність і безпеку лікування. Зміни техніки імплантації дозволили знизити частоту міграції джерел (рисунок 4).
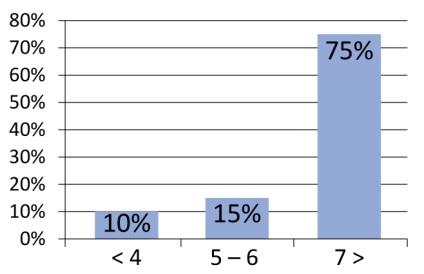
Малюнок 2. Частота рецидивів в залежності від стадії по Глісон
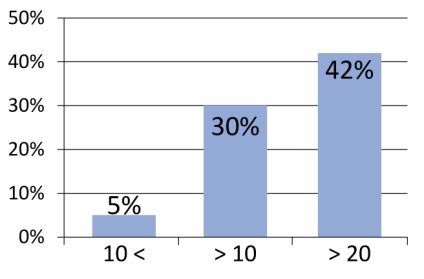
Малюнок 3. Частота рецидивів в залежності від вихідного рівня ПСА
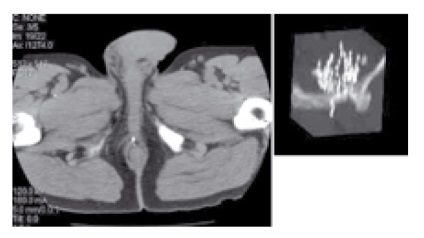
Малюнок 4. Міграція імплантів
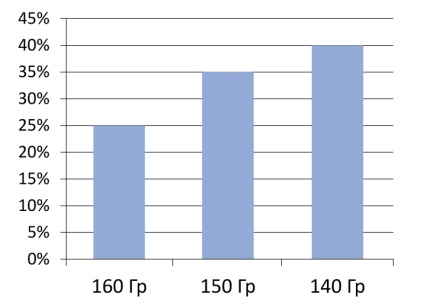
Малюнок 5. Частота біохімічного рецидиву в залежності від дози
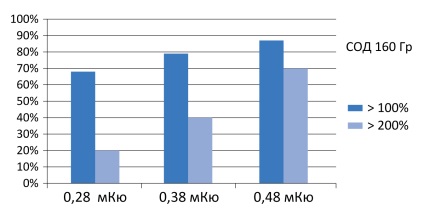
Малюнок 6. Використання джерел низької активності забезпечує кращий результат
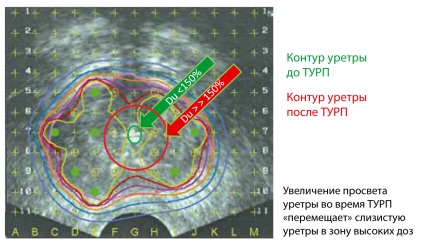
Малюнок 7. Поверхневий уретральний некроз і трансуретральна резекція
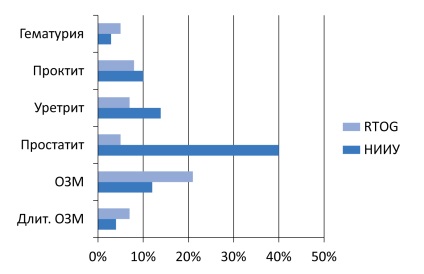
Малюнок 8. Ускладнення брахітерапії РПЖ
Ефективність та безпечність лікування прямо залежать від дози подведенного випромінювання (малюнок 5). Тому важливим завданням є досягнення необхідного балансу між цими критеріями (рисунок 6)
Ми використовуємо для імплантації «зерна» різної активності, поміщаючи в бічні частки передміхурової залози джерела більш високої активності, а поблизу уретри і прямої кишки, для зменшення навантаження на ці органи, - низькою.
Для корекції даного стану ми стандартно використовуємо альфа1-адреноблокатори. Нами було проведено пілотне дослідження по НЕОАД'ЮВАНТНА застосування альфа 1 АБ, в якому було отримано майже дворазове зменшення частоти розвитку обструктивних ускладнень в післяопераційному періоді.
У пацієнтів з більшим обсягом передміхурової залози ми проводимо неоад'ювантну гормональну терапію, мета якої - зменшити розміри органа.
Питання застосування превентивної трансуретральної резекції (ТУР) залишається відкритим. Проте, якщо хворому належить виконати брахітерапії і є виражена ІВО, то ТУР краще виконати до брахітерапії за 6-12 місяців, ніж після. Це пов'язано з досить високим ризиком розвитку серйозних ускладнень - стриктури уретри і нетримання сечі. Основною причиною цих ускладнень є розвиток поверхневого уретрального некрозу (малюнок 7). Довгий час вважалося, що брахітерапії протипоказана пацієнтам, які перенесли ТУРП, в зв'язку з високим ризиком розвитку нетримання сечі. Наш досвід свідчить, що брахітерапії здійсненна з високим ступенем безпеки в віддаленому періоді після ТУРП, ретельної дозиметрії і прецизійної установки джерел.
висновок
Брахітерапія - сучасний і безпечний метод лікування локалізованого РПЖ у пацієнтів низького і помірного ризику. Досягнуті нами результати лікування відповідають таким в провідних спеціалізованих клініках світу (малюнок 8).