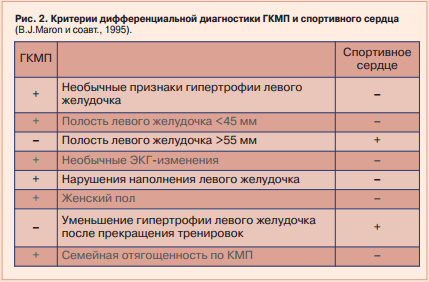
Селен і спорт
Патологія серця дуже часто супроводжує заняття спортом
Смерть спортсмена - це тільки крайній і трагічний етап цілого каскаду порушень, що виникли в організмі спортсмена в результаті інтенсивних занять спортом. Як ми побачимо далі - в сукупності з іншими механізмами. Випадки спортивної смерті - це тільки «верхівка айсберга», крайня ступінь проблеми, поширеною набагато ширше!
Насправді ці питання вже більше сотні років в поле зору лікарів і вчених в різних країнах. Термін «спортивне серце» введений в 1899 році для людей, що активно займаються спортом. Основоположник радянської кардіології Г. Ф. Ланг в 1938 році докладно описав «серце, патологічно змінене в результаті надмірних напружень спортивного характеру». Я не зупиняюся на питаннях класифікації, дослідники з різних сторін вивчали «спортивне серце», описували його як напруга серця, міокардіальну дистрофію, перетренувалися серце, останнім часом частіше використовують назви «кардіоміопатія напруги», «стрессорная кардіоміопатія спортсменів». Загальний підсумок цих досліджень такий: патологія серця (найчастіше - у формі кардіоміопатії) - поширена дуже широко, її ознаки в різній мірі знаходять в 1/3 випадків вже у дітей, що займаються спортом! З підвищенням інтенсивності тренувань, у професійних спортсменів, цей відсоток збільшується (за деякими даними - понад 50%!). Тому всі роки йде бурхлива дискусія, чи є цей процес патологією серця, або це фізіологічна реакція здорового серця на підвищене навантаження. І незрозуміло, коли, в який момент відбувається перехід від нормальної реакції до незворотних змін в міокарді.
І зверніть увагу, як і в разі раптової смерті спортсменів, тут дослідники не знаходять відповідь, чому у одних спортсменів серце страждає, а в інших ні. А якщо страждає - чому в ряді випадків гіпертрофія міокарда наростає, в інших - успішно компенсується при зниженні навантажень. Спортивні лікарі не можуть запропонувати спортсменам нічого, крім припинення занять спортом при виявленні якихось змін міокарда. А причини патології серця так і залишаються невідомими.
Термін «кардіоміопатія» застосовується для опису патології серця з невідомою етіологією. Як пишуть дослідники, «встановлення етіології і уточнення патогенезу якого-небудь захворювання, що відноситься до кардіоміопатія, сприяли б виділенню його з цієї групи в ряд відомих хвороб або в самостійну нозологічну форму».
Раптова серцева смерть у спорті
читайте також ► Серце спортсмена
Згідно з легендою раптова смерть, пов'язана з фізичним навантаженням вперше була зафіксована в 490 році до нової ери, коли молодий грецький солдат Фідіпід помер відразу після подолання бігом відстані від Марафону до Афін (42 кілометри 195 метрів), щоб повідомити про перемогу греків над персами. Сьогодні під ВС в спорті розуміють смерть, що настала безпосередньо під час навантажень, а також протягом 24-х годин з моменту появи перших симптомів, які змусили змінити або припинити спортивну діяльність.
У випадках ВСС в спорті зазвичай проводиться судово-медичний розтин, оскільки смерть зазвичай настає поза лікувальним закладом. Основним завданням судово-медичного експерта є не тільки встановлення причини, а й виключення її насильницького характеру.
- у чоловіків товщина міокарда не повинна перевищувати 13 мм, а кінцево-діастолічний розмір лівого шлуночка - не більше 65 мм;
- у жінок - 11 і 60 мм (відповідно);
- у підлітків 15-17 років чоловічої статі - 12 і 60 мм;
- у підлітків 15-17 років жіночої статі - 11 і 55 мм.
► Крім того, спортивні навантаження протипоказані при наступних пороках серця:
- аортальна недостатність при наявності регургітації, гемодинамічно значущих желудочковихнарушеній ритму в спокої або під час навантажувального тесту, дилатації висхідного відділу аорти;
- недостатність трикуспідального клапана при будь-якого ступеня трикуспідального регургітації;
- мітральна недостатність при наявності регургітації, порушення функції лівого шлуночка (фракція викиду
Аритмогенність КАРДІОМІОПАТІЯ ПРАВОГО ШЛУНОЧКА
Аритмогенна кардіоміопатія ПЖ - захворювання м'язи серця, що характеризується частковим або повним прогресуючим фіброзно-жировим заміщенням міокарда ПШ, пізніше - залученням до процесу ЛШ з відносно інтактною перегородки.
Захворювання недавно ідентифіковано і важко діагностується, тому його поширеність точно невідома, але вважається, що може варіювати в межах від 1: 3000 до 1:10 000, співвідношення чоловіки. жінки становить 2,5: 1. Перші клінічні прояви можуть виникнути в юнацькому віці, рідко - старше 40 років.
Точна причина захворювання невідома, однак в деяких сім'ях існують безперечні докази його успадкування. У більшості сімей, де більше одного хворого, найбільш імовірним типом успадкування є аутосомно-домінантний. Описано також принаймні один добре відомий варіант аритмогенной кардіоміопатії ПЖ, який успадковується по аутосомно-рецесивним типом.
Генетичними дослідженнями ідентифіковано принаймні 7 локусів генів, відповідальних за розвиток захворювання. З аритмогенной кардіоміопатією ПЖ також асоціюються мутації генів, що кодують білки вставних дисків (десмоплакін, плакоглобін зі специфічним фенотипом, плакофілін, десмоглеін, десмоколлін). Ознаки захворювання можуть варіювати навіть у членів однієї сім'ї, і патологія може проявитися через покоління. Вважається, що заняття спортом не можуть викликати аритмогенну кардіоміопатію ПЖ, проте захворювання частіше реєструють серед спортсменів. Мутації генів ріанодінового рецепторів серця ^ уІ2) асоціюються з поліморфної шлуночкової тахікардією, викликаної фізичними навантаженнями і ювенільної раптовою смертю.
При морфологічному дослідженні серця залученим виявляється частіше ПЖ, який має плямистий вигляд: змінені ділянки можуть бути оточені нормальними тканинами. Залучення ПЖ може бути регіонарним (20%) або дифузним (80%). Міокард ПШ прогресивно редукується, заміщаючи жирової і фіброзної тканиною, яка відрізняється від нефіброзной жировій інфільтрації, що виникає в ПЖ з віком. На ранніх стадіях захворювання стінки правих відділів серця товщають, але надалі через накопичення жирової тканини і появи ділянок дилатації вони стають більш тонкими (рис. 12.1а, б).
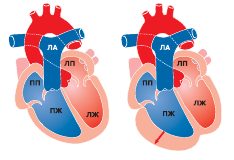
Аритмогенна кардіоміопатія ПЖ
а) ділянки жирової тканини призводять до ослаблення і вибухне м'язової стінки; б) ПЖ збільшується
Жирове переродження міокарда поширюється частіше від епікардіальних шарів до ендокардит. Міокард уражається переважно в області виносить тракту, верхівки і субтрікуспідальной зони, які розглядаються в якості «трикутника дисплазії».
При аритмогенной кардіоміопатії ПЖ липоматоз супроводжується переважно дилатацией виносить тракту ПШ або генералізованої дилатацией. Фіброліпоматоз характеризується наявністю фокальній аневризми ПЖ і випинанням в області верхівки, нижньої стінки, субтрікуспідальной і інфундібулярной зони.
У міру прогресування фіброзно-жирова дистрофія вражає також ЛШ і передсердя.
Серед молекулярних механізмів аритмогенной кардіоміопатії ПЖ розглядаються генетично детермініруемие мутації в десмосомальних протеїнах, а також інгібування сигнальних шляхів.
Стрес-індукований розрив десмосомальних зв'язків клітин може запускати процес апоптозу, викликати атрофію міокарда та заміщення його жировою тканиною.
Вогнища жирового переродження і інтерстиціального фіброзу при аритмогенной кардіоміопатії ПЖ не проводять електричні імпульси, внаслідок чого дезорганізована структура серця обумовлює виникнення безладної електричної активності, електричні імпульси можуть ставати розсіяними, внаслідок чого, крім порушень ритму серця, можуть виникати порушення його скоротливості (рис. 12.2а , б).
а) до скорочення; б) після скорочення
Основними клінічними симптомами аритмогенной кардіоміопатії ПЖ є:
• відчуття серцебиття, перебої в роботі серця, напади шлуночкової тахікардії;
• підвищена стомлюваність, запаморочення, непритомність;
• раптова зупинка кровообігу.
Описано 4 клінічні стадії захворювання:
• субклиническая, незначні шлуночкові аритмії можуть відзначатися або бути відсутнім;
• стадія явних електричних порушень, правошлуночкові аритмії і ризик зупинки серця пов'язані з морфофункціональними змінами ПЖ;
• стадія правошлуночковоюнедостатності з прогресуючим залученням ПЖ і подальшої його глобальної систолічною дисфункцією;
• стадія кінцевої бівентрікулярной СН.
На ЕКГ визначаються:
• спонтанні шлуночкові тахікардії зі зміною комплексу QRS по типу блокади лівої ніжки пучка Гіса;
• негативні зубці Т у відведеннях V на тлі синусового ритму;
• розширення комплексу QRS;
• неповна блокада правої ніжки пучка Гіса;
• ектопічні важкі аритмії: шлуночкова екстрасистолія, фібриляція шлуночків, передсердно тахікардія, фібриляція передсердь.
Приблизно у І пацієнтів реєструється характерна епсилон- хвиля і ППШ.
Методом холтерівського моніторування можна діагностувати епізоди шлуночкової тахіаритмії. Для оцінки прогресування захворювання важливо проводити реєстрацію ЕКГ в динаміці.
При ехокардіографії-дослідженні виявляються:
• дилатація ПШ і порушення його скоротливості (асинергія, дифузна гіпокінезія, зниження ФВ);
• локальна аневризма ПЖ;
• збільшення правого передсердя;
• ліві відділи серця частіше не змінені.
За допомогою допплер-ехокардіографії визначається порушення діастолічної функції ПШ і трикуспидальная регургітація. Для більш точної візуалізації ПЖ застосовують контрастну ехокардіограмі міокарда.
Методом МРТ візуалізуються ділянки заміщення міокарда жировою тканиною, фокальное витончення стінки і локальні аневризми. Продемонстровано хороша кореляція між результатами цього методу і результатами морфологічного дослідження міокарда.
Для підтвердження діагнозу використовують рентгенконтрастний вентрикулографію, при якій виявляють дилатацію ПШ з сегментарними порушеннями його скорочення, випинання контуру в області дисплазії і підвищення трабекулярную.
При ендоміокардіальної біопсії визначають фіброзно-жировій інфільтрації міокарда ПШ.
Великі діагностичні критерії:
• сімейний характер захворювання, підтверджений даними аутопсії або при хірургічному втручанні;
• епсилон- хвиля або локалізоване розширення комплексу QRS (> 110 мс) в правих грудних відведеннях (У1-У3);
• фіброліпоматозное заміщення міокарда за даними ендоміокардіальної біопсії;
• значна дилатація і зниження ФВ ПШ при відсутності або мінімальному залученні ЛШ;
• локалізована аневризма ПЖ;
• виражена сегментарная дилатація ПШ;
Малі діагностичні критерії:
• наявність в сімейному анамнезі випадків передчасної раптової смерті (у осіб у віці молодше 35 років) внаслідок передбачуваної аритмогенной кардіоміопатії ПЖ;
• ППШ на усередненої ЕКГ;
• інвертований зубець Т в правих грудних відведеннях у осіб у віці старше 12 років при відсутності блокади правої ніжки пучка Гіса;
• шлуночковатахікардія з ознаками блокади лівої ніжки пучка Гіса, документована по ЕКГ або результатами холтерівського моніторування або під час навантажувального тесту;
• часті шлуночковіекстрасистоли (> 1000/24 ч при холтерівське моніторування ЕКГ);
• помірна глобальна дилатація або зниження ФВ ПШ при незмінному ЛШ;
• помірна сегментарна дилатація ПШ;
• регіонарна гіпокінезія ПЖ.
Для вибору антиаритмічної терапії необхідне проведення інвазивного ЕФД і проб з дозованим фізичним навантаженням.
Серед антиаритмічнихпрепаратів ефективні аміодарон і соталол. Дигоксин застосовують при тахисистолической формі фібриляції передсердь для уповільнення ЧСС. Для відновлення синусового ритму проводять кардіоверсію.
Діуретики застосовують при СН у хворих із затримкою рідини.
З хірургічних методів лікування застосовують абляцию, якщо джерело порушеною електричної активності ідентифікований за допомогою електрофізіологічних тестів. У випадках якщо аритмії контролю не за допомогою лікарських засобів або абляції (велика поразка або наявність множинних аритмогенних вогнищ), вшивають імплантований кардіовертерний дефібрилятор, в деяких випадках потрібно імплантація водія ритму. Трансплантацію серця застосовують рідко, якщо контроль ритму неможливий іншими методами.