Зміна ентропії в оборотних і необоротних процессах.doc
Зміна ентропії в оборотних і необоротних процесах
Розглянемо зміна ентропії в оборотних термодинамічних процесах. Для таких процесів. Звідси випливає, що в оборотних процесах ентропія може як зростати, так і зменшуватися. Температура є позитивною величиною. Тому при підводі теплоти до системи (dq> 0) ставлення dq / T, рівне ds, буде більше нуля. Отже, в цьому випадку ентропія системи зростає. Якщо ж теплота відводиться від системи (dq<0), то ds<0 и энтропия убывает.
Інтегруючи рівняння для ds в межах від початкового стану 1 до кінцевого 2, знайдемо, що ентропія робочого тіла зміниться на величину
В оборотному адіабатні процесі dq = 0. Тому з (5.13) маємо s2-s1 = 0 і s2 = s1, тобто в оборотному адіабатні процесі ентропія постійна (s = const).
Розглянемо тепер, як змінюється ентропія в необоротних процесах. Нехай будь-якої довільний цикл складається з двох процесів: незворотного 1-а-2 і оборотного 2-b-1 (рис. 5.5). Такий цикл є незворотнім. Вираз (5.12) для нього матиме вигляд
Для оборотного процесу 2-b-1, згідно (5.13), маємо
Тоді вираз (5.14) запишеться у вигляді
тобто в необоротний процес значення інтеграла менше, ніж зміна ентропії в кінцевому і початковому станах.
У диференціальної формі вираження (5.16) має вигляд.
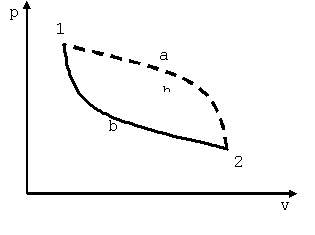
Мал. 5.5. Незворотний цикл, який складається з незворотного 1-a-2 і оборотного 2-b-1 циклів
Так само, як і (5.12), формула (5.17) являє собою рівняння другого закону термодинаміки для необоротних процесів. У загальному випадку для оборотних і необоротних процесів з урахуванням рівнянь (5.8), (5.12) і (5.9), (5.17) можна записати
(5.18) і (5.19) (5.20)
У наведених виразах знак рівності відноситься до оборотних, а знак нерівності - до незворотних процесів.