Літій - перший хімічний елемент-метал. Розташований у другому періоді I групи A підгрупи.
У вигляді простого речовини літій - м'який сріблясто-білий метал (температура плавлення 180,5 o С, температура кипіння 1336,6 o С) (рис. 1). З металів він найлегший (щільність 0,539 г / см 3).

Мал. 1. Літій. Зовнішній вигляд.
Літій хімічно дуже активний. З киснем і азотом взаємодіє за звичайних умов, тому на повітрі відразу ж окислюється, утворюючи темно-сірий наліт продуктів взаємодії (Li2 O, Li3 N). При температурі вище 200 o С загоряється. В атмосфері фтору і хлору, а також брому і йоду самозаймається при звичайних умовах.
Валентність літію в з'єднаннях
Літій - третій за рахунком елемент Періодичної таблиці Д.І. Менделєєва. Він знаходиться в другому періоді в IA групі. Ядро атома літію містить 3 протона і нейтрона (масове число дорівнює 7). В атомі літію є два енергетичних рівня, на яких знаходяться 3 електрона (рис. 2).
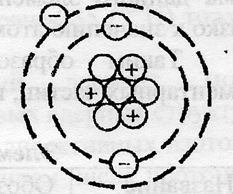
Мал. 2. Будівлі атома літію.
Електронна формула атома літію в основному стані має вигляд:
А енергетична діаграма (будується тільки для електронів зовнішнього енергетичного рівня, які по-іншому називають валентними):
Атом літію має один валентний електрон (неспарених), що свідчить про те, що для літію характерна валентність рівна I. Валентність літію постійна у всіх з'єднаннях (Li IH, Li I 2 O, Li I OH, Li I NO3. Li I Cl і т.д.)
Приклади розв'язання задач
Зразок літію масою 0,5 г розчинили у воді. На нейтралізацію отриманого розчину витратили 29,2 г 1,5% -ної соляної кислоти. Яка масова частка (%) літію в початковому зразку?
Запишемо рівняння реакцій:
LiOH + HCl = LiCl + H2 O (2).
Визначаємо масу і кількість речовини соляної кислоти (молярна маса - 36,5 г / моль):
ω = msolute / msolution × 100%;
msolute = ω / 100% × msolution;
msolute (HCl) = ω (HCl) / 100% × msolution;
msolute (HCl) = 1.5 / 100% × 29,2 = 0,438 г;
n (HCl) = m (HCl) / M (HCl);
n (HCl) = 0,438 / 36,5 = 0,012 моль.
Визначаємо кількість речовини LiOH, прореагував з HCl. Відповідно до рівняння (2):
n (LiOH): n (HCl) = 1: 1,
значить, n (LiOH) = n (HCl) = 0,012 моль.
Визначаємо кількість речовини, масу і масову частку літію в початковому зразку (масова частка дорівнює 7 г / моль). Відповідно до рівняння (1):
n (Li): n (LiOH) = 1: 1;
n (Li) = n (LiOH) = 0,012 моль.
m (Li) = n (Li) × M (Li);
m (Li) = 0,012 × 7 = 0,084 г;
ω (Li) = msolute (Li) / msolution (new) × 100%;
ω (Li) = 0,084 / 0,5 × 100% = 16,8%.