Більшість твердих речовин має кристалічну будову, яке характеризується строго певним розташуванням частинок. Якщо з'єднати частинки умовними лініями, то вийде просторовий каркас, званий кристалічною решіткою. Точки, в яких розміщені частинки кристала, називають вузлами решітки. У вузлах уявної решітки можуть перебувати атоми. іони або молекули.
Залежно від природи частинок, розташованих у вузлах, і характеру зв'язку між ними розрізняють чотири типи кристалічних решіток: іонну. металеву. атомну і молекулярну.
Іонними називають решітки, у вузлах яких знаходяться іони.
Їх утворюють речовини з іонним зв'язком. У вузлах таких грат розташовуються позитивні і негативні іони, пов'язані між собою електростатичним взаємодією.
Іонні кристалічні решітки мають солі. лугу. оксиди активних металів. Іони можуть бути прості або складні. Наприклад, в вузлах кристалічної решітки хлориду натрію знаходяться прості іони натрію Na + і хлору Cl -. а в вузлах решітки сульфату калію чергуються прості іони калію K + і складні сульфат-іони S O 4 2 -.
Зв'язки між іонами в таких кристалах міцні. Тому іонні речовини тверді. тугоплавкі. нелеткі. Такі речовини добре розчиняються у воді.
Кристалічна решітка хлориду натрію

Кристал хлориду натрію
Металевими називають решітки, які складаються з позитивних іонів і атомів металу і вільних електронів.
Їх утворюють речовини з металевим зв'язком. У вузлах металевої решітки знаходяться атоми і іони (то атоми, то іони, в які легко перетворюються атоми, віддаючи свої зовнішні електрони в загальне користування).
Такі кристалічні решітки характерні для простих речовин металів і сплавів.
Температури плавлення металів можуть бути різними (від \ (- 37 ° С \) у ртуті до двох-трьох тисяч градусів). Але все метали мають характерний металевий блиск. гнучкість. пластичність. добре проводять електричний струм і тепло.
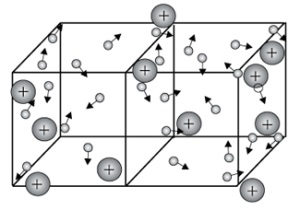
Металева кристалічна решітка

Атомними називають кристалічні решітки, у вузлах яких знаходяться окремі атоми, з'єднані ковалентними зв'язками.
Такий тип решітки має алмаз - одне з аллотропних видозмін вуглецю. До речовин з атомної кристалічною решіткою відносяться графіт. кремній. бор і германій. а також складні речовини, наприклад карборунд SiC і кремнезем. кварц. Горний кришталь. пісок. до складу яких входить оксид кремнію (IV) Si O 2.
Таким речовинам характерні висока міцність і твердість. Так, алмаз є самим твердим природним речовиною. У речовин з атомної кристалічною решіткою дуже високі температури плавлення і кипіння. Наприклад, температура плавлення кремнезему \ (1728 ° С \), а у графіту вона вище \ (4000 ° С \). Атомні кристали практично нерозчинні.
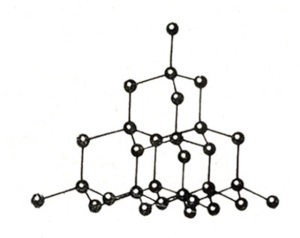
Кристалічна решітка алмаза

Молекулярними називають решітки, у вузлах яких знаходяться молекули, пов'язані слабким міжмолекулярним взаємодією.
Незважаючи на те, що всередині молекул атоми з'єднані дуже міцними ковалентними зв'язками, між самими молекулами діють слабкі сили міжмолекулярної тяжіння. Тому молекулярні кристали мають невелику міцність і твердість. низькі температури плавлення і кипіння. Багато молекулярні речовини при кімнатній температурі є рідинами і гази. Такі речовини летючі. Наприклад, кристалічні йод і твердий оксид вуглецю (IV) ( «сухий лід») випаровуються, не переходячи в рідкий стан. Деякі молекулярні речовини мають запах.
Такий тип решітки мають прості речовини в твердому агрегатному стані: благородні гази з одноатомними молекулами (He. Ne. Ar. Kr. Xe. Rn), а також неметали з дво- і багатоатомних молекулами (H 2. O 2. N 2. Cl 2. I 2. O 3. P 4. S 8).
Молекулярну кристалічну решітку мають також речовини з ковалентними полярними зв'язками: вода - лід. тверді аміак. кислоти. оксиди неметалів. Більшість органічних сполук теж являють собою молекулярні кристали (нафталін. Цукор. Глюкоза).
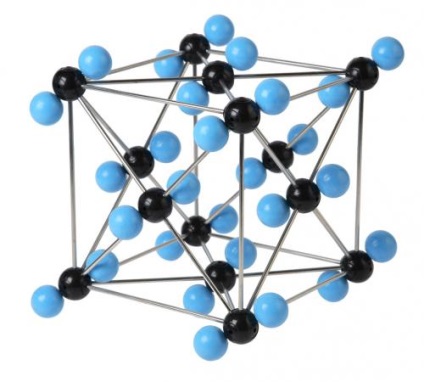
Кристалічна решітка вуглекислого газу