Вода - це дивовижне і унікальне речовина
Навколишнє нас вода - це речовина з унікальними властивостями, які не тільки ще повністю не пояснені, але далеко не всі відомі. Немає речовини, більш дивного і загадкового, ніж звичайна вода. Її властивості не підкоряються закономірностям, властивим більшості оточуючих нас речовин, що викликано унікальністю будови молекули води.

Молекула води має дісімметріі: киснева частина молекули має негативний заряд, а воднева - позитивний. Вони зміщені відносно один одного, тому молекула води є електричним диполем і, в той же час, володіє магнітним моментом. Наявність просторової асиметрії дозволяє молекулі води, зв'язуючись між собою різним чином, утворювати дуже складні і різноманітні стабільні структури - кластери, які мають місце як в твердому, так в рідкому і навіть в газоподібному стані води. Наведемо кілька прикладів особливих властивостей води.
Вода - найсильніший природний розчинник: у воді розчиняються в тій чи іншій мірі всі речовини. Кожен раз, наприклад, випиваючи склянку гарячого чаю, ми разом з ним випиваємо 0,1 міліграма розчиненого в ньому скла. Вода має високий дипольниммоментом і, внаслідок цього унікально високою діелектричної постійної, найвищою серед всіх рідин! Як тільки іон певної речовини потрапляє в воду, він моментально покривається гідратної оболонкою, утворюючи «гігантський атом». Недарма ще алхіміки говорили: «Речовини не реагують один з одним інакше, як тільки в рідкому вигляді» (тобто в водному розчині). Коли розчиняються речовини потрапляють у воду, вони завдяки властивостям води посилено поділяються на все більш дрібні частинки, аж до молекул і іонів. Виходять гідратованих частки розчинених речовин, які і беруть участь в різних хімічних реакціях.
Вода - одне з найзагадковіших речовин нашої планети. Будучи нормальним мономолекулярним з'єднанням, вона повинна була б кипіти при + 70 ° C, а замерзати майже при -100 ° C. На відміну від всіх інших рідин, вода при затвердінні зменшує свою вагу. Максимальна щільність води має місце при + 4 ° C. Цей факт надзвичайно важливий для біосфери. В результаті лід утворюється на поверхні водойм, не даючи їм промерзати до дна, і, тим самим, не даючи загинути рибам та іншим представникам водної фауни в зимовий час.
Поверхневий натяг чистої води більше, ніж у будь-якій іншій рідині, крім ртуті. У абсолютно чистої води поверхневий натяг таке, що по ній можна було б кататися на ковзанах. Наявність домішок різко знижує величину поверхневого натягу води. Одна з «дивацтв» води в тому, що ця речовина - єдине на Землі - завжди виступає в трьох «особах» - рідкому, твердому і газоподібному.
Розчинники є, як правило, або кислотами або лугами. Лише вода (OH- і OH +) проявляє властивості, як кислоти, так і підстави. Ступінь кислотності або ощелачивания будь-якого розчину вимірюється величиною pH, яка змінюється від 0 для кислоти до 14 для лугу. Нейтральний кислотно-лужний баланс в воді, коли число позитивних і негативних іонів одно, відповідає pH = 7. Чим менше значення pH, тим більше кисла реакція середовища і сильніше її кислотні властивості. Нормальною вважається вода з pH = 6-8. При pH = 3-6 реакція слабокисла. При pH = 8-11 - слаболужна. Значення кислотно-лужного балансу крові здорової людини коливається в дуже вузьких межах pH = 7,35-7,45. Будь-які відхилення - патологія. Зрушення рН нижче 7,35 призводить до закислення (ацидозу), а вище 7,45 - до підвищення лужності (алкалоізу) організму. Зрушення (нижче 6,8 і вище 7,8) призводять до серйозних порушень викликає хвороби. До речі, і для пиття найбільш корисна вода з такими ж значеннями рН, як у нормальної крові, хоча тут можуть бути і відхилення.
Наведемо значення рН деяких середовищ, що представляють інтерес:
Слина 5,8 - 7,4; шлунковий сік 1,5 - 1,8; молоко 6,6; кави 5; пиво 4,5 - 5; томатний сік 4,6; апельсиновий сік 3,7; харчової оцет 3; лимонний сік 2,4.
Дуже чиста вода в капілярах замерзає при -70 ° C. При таненні вода зберігає льодово структуру у вигляді фрагментів (кластерів) дуже довго, аж до температури кипіння Прихована теплота плавлення води - найбільш висока серед всіх речовин, за винятком аміаку та водню, а прихована теплота випаровування - найбільш висока з усіх речовин. Питома теплоємність також найбільша за винятком рідкого аміаку і водню. Вона приблизно в десять разів вище, ніж у гірських порід.
На світлі, мабуть, немає двох абсолютно однакових сніжинок. Кожен момент часу, кожна точка простору в один і той же момент часу, несуть свою унікальну інформацію, яку сприймає і фіксує в своїй структурі утворюється сніжинка. Кожна сніжинка, падаючи на землю, проходить через шари повітря, що відрізняються вологістю, температурою, забрудненням та іншими параметрами. Тому серед мільйонів сніжинок навряд чи можна знайти дві абсолютно однакові.
Як різноманітні форми сніжинок, інею, морозних візерунків на вікнах - твердих кристалів води, так ще більш дивно різноманітні форми і властивості рідких кристалів, що складають рідку воду.
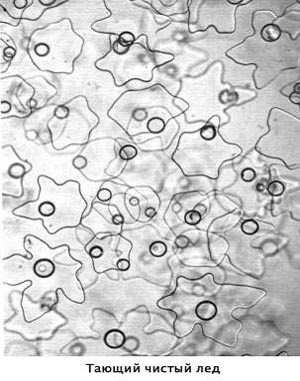
На малюнку представлені фотографії (Джил Уолкер), який тане чистого льоду і типові форми кристалів, що утворюються в замерзає чистій воді. У тане льоду добре видно кластери, які потім, деформуючись і змінюючи форму, зберігаються і в рідкій воді, аж до температури кипіння. Навіть водяна пара складається не тільки з окремих молекул, але на 10% з різних більш складних структур.
«Важка вода». У важкій воді весь водень замінений на дейтерій. Ні за кольором, ні за смаком, ні за запахом вона не відрізняється від звичайної води. Але фізичні властивості її дещо інші. Замерзає вона при 3,8 ° C, кипить при 101,4 ° C. В результаті цих відмінностей природні води різного походження відрізняються за ізотопним складом. Це результат багаторазового випаровування і конденсації з кругообіг води. Середнє співвідношення в природних водах важкої води і води звичайної 1/6000. Питома вага важкої води на десять відсотків більше, ніж у води звичайної. На відміну від звичайної води, важка вода має максимальну щільність при + 11,6 ° C.
У свій час в пресі було багато публікацій про «живий» і «мертвої» води, про способи їх отримання, біологічну дію і видах використання. Не зупиняючись більш детально на цьому питанні, зазначимо лише, що обидва ці види води виходять шляхом електролізу води і відрізняються величиною pH. «Мертва вода» (анолит) має кисле середовище і надає потужний дезінфікуючий і стерилізуючий дію, використовується для лікування виразок, гнійних ран, шкірних захворювань. «Жива вода» (катали) має лужне середовище і є потужним біостимулятором, покращує діяльність клітин, сприяє виведенню шлаків і підсилює захисні механізми організму. Обидва ці кошти, як «жива», так і «мертва» вода є сильнодіючими засобами і для свого застосування вимагають обережності і досвіду.
Цікаві результати дає використання для пиття «обезгаженной» води, води містить вдвічі менше розчинених в ній газів, як це має місце в рідинах біологічних об'єктів. Це покращує клітинний обмін, стимулює фізіологічні процеси. Умивання такою водою покращує якість шкіри.
До сих пір дискутується проблема 37 градусної температури в тваринному світі. Як відомо, при нагріванні будь-якої речовини теплоємність його зростає. Будь-якого, крім води: при її нагріванні від 0 до 37 градусів теплоємність падає, і лише при подальшому нагріванні починає зростати. Цей факт означає, що при 36-37 градусах для підвищення температури деякого об'єму води необхідна мінімальна кількість тепла. Мабуть, саме ця властивість води стало селектірующім фактором еволюції у виробленні теплокровности на рівні 37 градусів Цельсія. А підвищення температури потрібно для підвищення інтенсивності протікання біологічних процесів.