Практична робота №1
Правила техніки безпеки при роботі в хімічному кабінеті. Прийоми поводження з лабораторним обладнанням та нагрівальними приладами
Мета: познайомитися з правилами техніки безпеки при роботі в хімічній лабораторії і
Устаткування: лабораторний штатив, спиртівка, тримач, пробірка, круглодонная і конічна колби, сірники.
Досвід 1. Пристрій лабораторного штатива
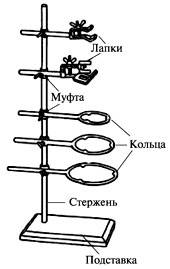
Штатив служить для кріплення деталей хімічних установок при виконанні дослідів. Він складається з масивної чавунної підставки, в яку угвинчений стрижень. На стрижні за допомогою муфт зміцнюють лапки і кільця
Муфти з укріпленими в них лапкою і кільцями можна переміщати уздовж стрижня і закріплювати в потрібному положенні, для чого необхідно послабити кріплення муфти до стрижня і, піднявши її на необхідну висоту, закріпити
Досвід 2. Прийоми роботи з спиртівкою
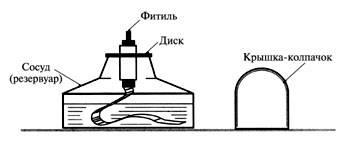
Зніміть ковпачок з спиртівки і поставте його на стіл. Перевірте, чи щільно диск прилягає до отвору судини, вона має бути закрита повністю, інакше може спалахнути спирт в посудині. Запаліть спиртівку сірником
Дослід 4. Будова полум'я
Запаліть ще раз спиртівку і розгляньте, яка будова має полум'я. Для встановлення різниці температур в різних областях полум'я внесіть на 2-3 с лучинку в середню, найбільш широку, частина полум'я (щоб вона перетинала все його частини по горизонталі, як показано на малюнку)
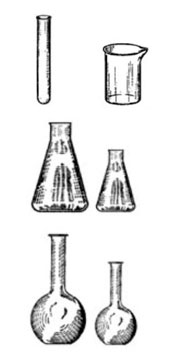
Більшість дослідів проводять в скляному посуді: пробірках, хімічних склянках, колбах. Під час досліду в них доводиться перемішувати вміст. У пробірці, як правило, змішують малі кількості речовин (не більше 2 мл). Висота стовпчика рідини при змішуванні розчинів в пробірці не повинна перевищувати 2 см. Перемішування розчинів в пробірці виробляють швидким енергійним постукуванням по її нижнього кінця. У колбі вміст перемішують круговими рухами, а в склянці - скляною паличкою з гумовим наконечником
Чому для виготовлення хімічного посуду найбільш часто використовується скло?
Чому забороняється струшувати пробірку з речовиною, закриваючи отвір пальцем? K яких наслідків це може призвести
Практична робота №2
Спостереження за змінами, що відбуваються з запаленою свічкою, їх опис
Мета: спостерігати фізичні і хімічні явища при горінні свічки.
Устаткування: предметне скло, свічка, сірники, суха пробірка, утримувач.
Досвід 1. Фізичні явища при горінні свічки
Візьміть вигнуту під прямим кутом Г-подібну скляну трубку, один кінець її внесіть в середню частину полум'я, а інший опустіть в пробірку
Kакой процес має місце при плавленні парафіну?
Що спостерігаєте на стінках пробірки?
парафін починає танути близько гніту, утворюючи круглу калюжку.
Дослід 2. Виявлення продуктів горіння в полум'ї
Візьміть шматочок жерсті, закріпіть його в утримувачі для пробірок, внесіть в зону темного конуса свічки, що горить і потримайте 3-5 с. Швидко підійміть жесть
Суху, бажано охолоджену, але не запітнілу пробірку закріпіть в тримачі, переверніть догори дном і потримайте над полум'ям до запотівання. В ту ж пробірку швидко прилейте 2-3 мл вапняної води
Що з'явилося на нижній поверхні жерсті?
Чому запотіла пробірка? Що сталося з вапняної водою?
Практична робота №3
Поділ суміші річкового піску і солі.
Мета: Вивчити методи розділення сумішей.
Устаткування: суміш річкового піску і солі, спиртівка, пробірки, фільтр, воронка, стакани.
1. Розчинити трохи суміші в воді, поклавши її в стакан і долив воду. Ретельно перемішати. І почекати.
Пісок осідає на дно, сіль розчиняється у воді.
2. Скласти фільтр. Вкласти його в лійку, після чого воронку опустити в склянку.
3. Поступово доливати в воронку з фільтром отриманий розчин.
4. Перелити частина фільтрату в пробірку. Запалити спиртівку. Пробірку закріпити в утримувачі. Після чого піднести до полум'я пальника і нагрівати в нижній частині.
Частинки піску осідають на фільтрі, вода з розчиненою в ній сіллю фільтрується в стакан.
Вода випаровується, на стінках осідає сіль. Таким чином суміш солі і піску розділена.
Практична робота №4
Ознаки хімічних реакцій
Мета: розглянути приклади хімічних реакцій і виявити їх ознаки.
Обладнання: пробірки, мідний дріт, спиртівка, оксид міді (II), розчин сірчаної кислоти, мармур, розчин соляної кислоти, розчини хлориду заліза (III) і роданида калію, розчини сульфату натрію і хлориду барію.
Досвід 1. Взаємодія мармуру з кислотою
Покладіть в невелику склянку шматочки мармуру. Прилейте в стакан стільки соляної кислоти, щоб нею вкрилися шматочки. Внесіть в стакан палаючу лучину
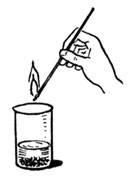
Спостерігається виділення газу.
Дослід 2. Взаємодія хлориду заліза (III) з роданідом калію
У пробірку налийте 2 мл розчину хлориду заліза (III), a потім додайте кілька крапель розчину роданида калію KCNS (солі роданістоводородной кислоти HCNS з кислотним залишком CNS)
Відбувається зміни колір розчину (криваво червоний)
Дослід 3. Взаємодія сульфату цинку з хлоридом барію
У пробірку налийте 2 мл розчину сульфату цинку. Потім додайте кілька крапель розчину хлориду барію
Спостерігається випадання білого осаду