кількість носіїв мутації. Середня частота невиправлених помилок - 1 на 10 10
І білок і нуклеїнова кислота - це біополімери, тобто біологічні макромолекули. Вони складаються з безлічі (багатьох тисяч) з'єднаних один з одним «ланок» - мономерів.
Мономери у цих хімічних сполук різні. Білки складаються з амінокислот, нуклеїнові кислоти складаються з нуклеотидів.
Білки виконують безліч функцій, а у нуклеїнових кислот тільки 2 (передача генетичної та реалізація генетичної інформації і синтез білка). Однак, без послідовності нуклеотидів неможливо відтворити амінкіслотную послідовність в складі білка.
9. Схожість і відмінності в будові білків і вуглеводів
Мають полімерне будову (складні полімери, або поліконденсати), складаються з безлічі мономерів. Мономерам білка є різні амінокислоти (NH2-CHR-COOH).
У складі будь-якої амінокислоти до одного і того ж атому вуглецю приєднуються дві сильно заряджені групи (аминогруппа NH2 + і карбоксильная група COOH-), завдяки своїм властивостям амінокислоти можуть брати участь в складних хімічних реакціях, в т.ч. в освіті довгих полімерів. Білки - головний функціональний елемент будь-якого організму. У всіх живих істот у формуванні білків беруть участь 20 основних амінокислот. Середній розмір білка - близько 300 амінокислот. Функція конкретного білка визначається послідовністю його амінокислот.
1 - не несуть на собі заряду зовсім (вуглеводневі залишки)
2 - радикали зі слабкими електростатичними зарядами (гідроксильна, карбонильная, тіогруппи)
3 - мають сильний позитивний заряд (аминогруппа)
4 - сильний негативний заряд (карбоксильная, фосфатна група)
Молекула білка може мати ДУЖЕ складними хімічними властивостями і може виконувати ДУЖЕ складні функції.
Завдяки особливостям свого хімічного будови, білки надзвичайно різноманітні за своїми хімічними властивостями і виконуваних в організмі функцій
виконуються тільки білками:
1. каталітична (ферментативна);
1. пасивний транспорт (по градієнту) - канал;
2. активний транспорт - мембранний насос;
4. рухова (актин, міозин);
8. будівельна (кератин);
3) первинна структура - послідовність амінокислот;
4) вторинна структура: - # 945; -Спіралі;
- # 946; -листи. (Численні слабкі водорондние зв'язку, за рахунок яких відбувається скручування у вторинні структури)
3) третинна структура - тривимірні молекули, які утворюються за рахунок невикористаних власних зарядів. Гідрофобні зв'язку - слабкі, але стабільні за рахунок кількості. S-S зв'язок - міцна, здатна зв'язувати молекули і утворювати третинну структуру;
4) четвертичная структура (молекулярні комплекси). Класичний приклад - Гемоглобін. (Складається з 2 молекул # 945; -глобіна, 2 молекул # 946; -глобіна, гема і іона заліза.)
З вторинної структури починається конформація молекул під температурою. Фактором, на неї впливає, є концентрація різних іонів. Змінивши свою конформацію, білок може залишитися в стабільному стані. Зміна конформації впливає на хімічні властивості молекули - здатності виконувати потрібну опцію.
На відміну від жирів і вуглеводів білки володіють величезним структурним різноманітністю => біологічні функції білків теж разюче різноманітні.
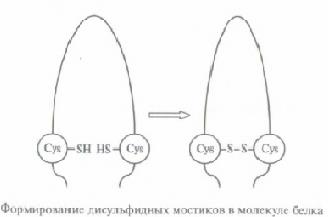
Одним з 20 варіантів амінокислот, які використовуються в складі білків, є цистин (Cys). У його радикал міститься функціональна група SH. Якщо 2 залишку цистину в третинної структурі виявляються поблизу один від одного, між ними, під дією особливого ферменту, може виникнути дисульфідних місток S-S.Такіе містки відіграють роль стяжок, що стабілізують третинну структуру молекули білка.
Функції конкретної білкової молекули залежать не тільки від її амінокислотноїпослідовності, але і від її конформації в даний момент. (Наприклад, зміна конформації молекул білка за допомогою високої температури веде до незворотної інактивації білка (сире-варене яйце)).
Змінюючи в своїх клітинах концентрацію деяких іонів, організм здатний тонко регулювати біологічну активність власних білків. (Кристали солі на яєчному білку - каламутні розлучення - тимчасова інактивація білків).
Білки - полімерні сполуки. І серед вуглеводів теж можуть бути полімери (наприклад, складні вуглеводи - крохмаль, глікоген, целюлоза, хітин).
І білки і вуглеводи виконують структурну функцію (білки - каркас клітини у тварин, вуглеводи - клітинна стінка)
Вуглеводи і білки виконують захисну функцію, у білків вона активна (захист організму імуноглобулінами), а у вуглеводів пасивна (зміцнює клітинні стінки за рахунок хітину і целюлози).
Різні мономери. У білків - амінокислоти, при тому, вони можуть бути різними, а у вуглеводів ланки Н-С-ОН. У вуглеводів будова простіше, ніж у білків, білки мають величезне структурний різноманітність.
Вуглеводи через свого одноманітного будови можуть виконувати тільки запасну і енергетичну функції, в той час як функції білків разюче різноманітні.
Білки - складні полімери, а вуглеводи - можуть бути полімерами, а можуть і не бути.
І білки і вуглеводи виконують запасаючу функцію (у білків - казеїн, у вуглеводів - крохмаль і глікоген)
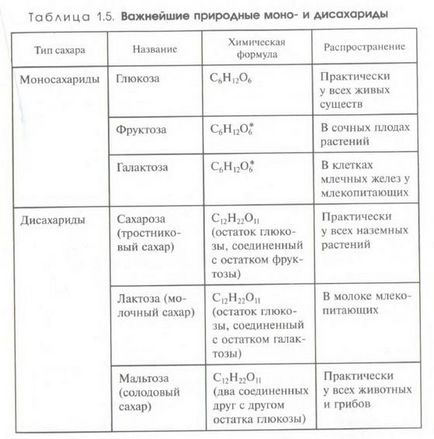
Органічні речовини, що містять карбонільну групу і кілька гідроксильних груп. Є гідрофільними речовинами, тому що багато (ОН), багато хто з них розчиняються у воді (цукру).
1. Моносахариди (одна невелика ланцюжок (3≤n≤7) з декількома ланками Н-С-ОН): глюкоза (C6H12O6) - це циклічний моносахарид, тому що його молекули замикаються в кільце через 1 з атомів О2; фруктоза, галактоза (ізомери).
2. Дисахариди (2 кільцевих моносахарида, з'єднані один з одним через атом кисню): сахароза (C12H22O11); (Сахароза = глюкоза + фруктоза)
3. Полісахариди. складаються з численних залишків моносахаридів) крохмаль, глікоген, целюлоза, хітин. Через великих розмірів своїх молекул полісахариди практично нерозчинні в воді і не мають солодкого смаку.
Всі вуглеводи влаштовані більш-менш однотипно, отже, їх функції порівняно прості і однотипні.
1. Енергетична. (Енергія за рахунок окислення глюкози)
C6H12O6 + O2 → CO2 + H2
O + E (АТФ) → світло, тепло, механічна, електрична,
синтез інших зв'язків.
2. Запасна. (Запас речовин у багатьох організмів представлений, в основному, полісахариди; у тварин і грибів полісахарид - глікоген)
3. Будівельний (полісахариди складають основу клітинних стінок)