Аполіхін О.І. Сівков А.В. Ощепков В.Н. Кешиша Н.Г. Шадеркін І.А.
Методи «рятівної» терапії застосовуються при місцевому або біохімічному рецидив раку передміхурової залози після проведення його лікування по радикальним програмами.
Визначення біохімічного рецидиву після фокальних методів лікування є предметом дискусії. До теперішнього часу єдиної думки не існує.
Після констатації біохімічного рецидиву, необхідно відповісти на питання: «Чи є це прогресування місцевим або системним?». Для підтвердження
характеру рецидиву необхідно використання всіх сучасних засобів візуалізації: ТРУЗІ передміхурової залози, магнітно-резонансну томографію передміхурової залози і органів таза (МРТ), комп'ютерну томографію заочеревинного простору і таза для візуалізації збільшених лімфовузлів,
позитронно - емісійної томографії (ПЕТ), остеосцинтиграфії і біопсії передміхурової залози після променевих методів або зони уретровезікального анастомозу після РПЕ. Після променевих методів і аблятівних технологій біопсію доцільно виконувати не раніше, ніж через 18 місяців після проведеного лікування.
Таблиця 1. Місцевий рецидив після РПЕ
Критерії диференціювання місцевого
рецидиву від генералізованого
Більш ніж у 80% хворих
з місцевим прогресуванням
Більш ніж у 80% хворих
з системним прогресуванням
A. Heidenreich, M. Bolla, S. Joniau, M.D. Mason, V. Matveev, N. Mottet, H-P. Schmid, T.H. van der Kwast, T. Wiegel, F. Zattoni. Guidelines on Prostate Cancer
Рятівні методи лікування РПЖ
До варіантів «рятівного» лікування відносять: дистанційну променеву терапію, РПЕ, високодозової брахітерапії, кріоабляцію і HIFU-терапію.
Найчастіше при місцевому рецидиві після радикальної простатектомії виконують спасітельнуюдістанціонную променеву терапію (64-66 Гр на ложі передміхурової залози). Показано, що чим менше вихідний рівень ПСА після виконаної РПЕ, тим краще результати лікування. Наприклад, якщо ПСА до дистанційної променевої терапії не перевищував 0,2 нг / мл, то 5-річна безрецидивної виживаність досягає 77%, тоді як у пацієнтів з рівнем ПСА 0,2-1,0 нг / мл, вона становить 34% і 0% відповідно.
Таблиця 2. Ускладнення після СРПЕ і РПЕ
Рятівна високодозової брахітерапії (СВБТ) може виконуватися після дистанційної променевої терапії та перманентної брахітерапії. До свідчень відносять: необструктивний тип сечовипускання; час подвоєння ПСА більше 6 місяців; сума балів по Глісон менше або дорівнює 6; рівень ПСА менше 10 нг / мл; час передбачуваної тривалості життя більше 5 років.
Рятівна кріоабляція після ДЛТ представляється «идеаль
ної »для пацієнтів з клінічною стадією менш Т2С; показником Глисона менше 7, ПСА менше 10 нг / мл на момент виконання ДЛТ. «Ідеальний» обсяг передміхурової залози для виконання кріоабляціі: 20-30 см 3. П'ятирічна виживаність без біохімічного рецидиву складає 59% (Табліца3).
Кіль-
кість
пацієнтів
Медіна
спостереження (міс.)
Поріг оцінки биохим
мического рецидиву
Рятівна HIFU-терапія. показання для цього методу такі ж, як і для рятівної кріоабляціі передміхурової залози. Однак необхідно відзначити, що для рятівної HIFU обструктивний тип сечовипускання є відносним протипоказанням, а ТУР в анамнезі протипоказанням не є.
% негативних
біопсій ПЖ
виживання без
біохімічесrого рецидиву
визначення біохімічного
рецидиву
Комбінація гістології та ПСА
Надир ПСА + 2 нг / мл
Zacharakis
еt al.
Надир ПСА> = 0,2 нг / мл
Надир ПСА + 2 нг / мл
Рятівна HIFU можлива і після брахітерапії. У нас є власний невеликий досвід лікування з використанням апарату Sonablate- 500: трьом пацієнтам зі стадією T2а-bNxM0 виконувався HIFU при місцевому рецидиві після брахітерапії. Середній рівень ПСА перед процедурою склав 4,5 нг / мл. Період спостереження склав від трьох до дев'яти місяців. Середній рівень ПСА після лікування - 0,3 нг / мл. Наявність імплантів в передміхуровій залозі не перешкоджав виконанню HIFU-терапії.
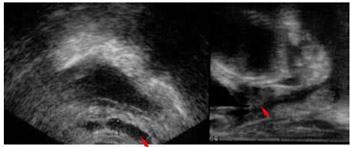
Малюнок 1. Рятівна HIFU-терапія (HIFU) після РПЕ
• При місцевому рецидиві після РПЕ найбільш широко застосовують ДЛТ. Перспективи застосування HIFU і кріоабляціі на даний момент активно вивчаються.
• При місцевому рецидиві після ДЛТ в якості альтернативи РПЕ можливе застосування аблятівних технологій - HIFU і кріоабляціі. Потрібно вивчення найближчих та віддалених результатів.
• При місцевому рецидиві після перманентної брахітерапії найбільш перспективним також є використання HIFU і кріоабляціі.
• При місцевому рецидиві після кріотерапії технічно можлива повторна процедура, а при відсутності ефекту - виконання СРПЕ або ДЛТ.
• При місцевому рецидиві після HIFU-терапії технічно можливо виконання ще одного сеансу абляції, СРПЕ.
• Велика кількість методів рятівної терапії та їх комбіноване застосування відкриває великі перспективи лікування РПЖ. Однак, необхідно накопичення досвіду і вивчення віддалених результатів.
Ключові слова: рак простати, сальважние методи, використання апарату Sonablate-500, біохімічний рецидив, місцевий рецидив.
Keywords: prostate cancer, salvage therapy, use of the deviceSonablate-500, biochemical failure, local recurrence.