Методи інактивації вірусів. Хімічні методи інактивації вірусів.
У промислове виробництво вірусних препаратів з наростаючою швидкістю залучаються все нові і нові вірусні агенти. Переважна більшість нових об'єктів відноситься до класу так званих «оболонкових вірусів». Спостерігається тенденція швидкого скорочення періоду між відкриттям чергового збудника і організацією лабораторних і промислових виробництв інактивованих препаратів.
Вимоги з безпеки посилюються в зв'язку з необхідністю в багатьох випадках приготування концентратів вірусних антигенів. Слід зазначити, що інактивація повинна бути не тільки ефективною, але і максимально щадить (селективної). Іншими словами, супутні зміни в структурі вірусних частинок і їх компонентів повинні бути мінімальними. Однак механізм инактивирующих впливів у багатьох відношеннях недостатньо з'ясований і їх використання часто носить емпіричний характер.
Так як віріони в центрі агрегатів, утворених клітинними і сироватковими компонентами. можуть бути захищені від інактивації, руйнування і видалення агрегатів різними методами очищення вірусної суспензії є важливим етапом перед інактивацією. При виготовленні цільновіріонних НЕ-реплицирующихся вакцин використовують хімічні і фізичні методи інактивації вірусів.
Хімічні методи інактивації вірусів
З хімічних сполук найбільш часто використовують два основних типи інактиваторів: ретікулірующіе (розпушують) агенти і алкілуючі агенти.
До ретікулірующім агентів належать альдегіди, в тому числі формальдегід, глютаральдегид і гліцідальдегід, з яких найбільш часто використовують формальдегід. До алкірующім агентів належать бетапропіолактон, етиленімін і інші азиридин.
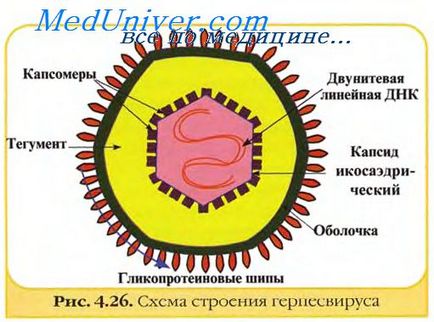
Механізм дії инактивирующих агентів. ймовірно, полягає в наступному: 1) взаємодіючи з нуклеїновими кислотами, вони унеможливлюють їх реплікацію; 2) викликають ретикуляції білків.
Механізм дії инактивирующих агентів краще вивчений стосовно білкам, ніж до нуклеїнових кислот, хоча в цілому залишається в повному обсязі з'ясованим. Інактивація вірусів, здається, ґрунтується на подвійному дії ретикуляції білків, що взаємодіють з клітинними рецепторами, і блокаді реплікації нуклеїнових кислот. Необхідна концентрація инактивирующих агентів залежить, головним чином, від відносної концентрації білків і нуклеїнових кислот в інактівіруемой середовищі. Температура і гомогенність інактівіруемой субстрату також грають ключову роль в кінетиці інактивації вірусу.
Можливість оборотності змін реактивних груп (аминогруппа лізину, фенольні ядра тирозину) необхідно враховувати, особливо в разі використання формальдегіду.
Повнота інактивації вірусу повинна визначатися відразу після виготовлення вакцини.
Найбільш загальноприйнятими інактивує агентами є формальдегід, бета-пропіолактон і етиленімін. Одним з переваг бета-пропіолактоном, використовуваного для виготовлення вакцини проти сказу, і етиленіміну, що застосовується у виготовленні вакцини проти ящуру, є те, що вони повністю гідролізуються протягом декількох годин з утворенням нетоксичних продуктів.
Формальдегід інактивує віруси завдяки високій реакційній здатності щодо білків і нуклеїнових кислот. Він вступає в з'єднання не тільки з вірусними частками, але і з численними компонентами середовища, в яку його додають.
Механізм інактивації вірусів формальдегідом складний і характеризується двома типами реакцій. Взаємодія формальдегіду з нуклеїнової кислотою і білками вірусу протікає, відповідно, по типу реакції першого і другого порядку. Найбільш істотна для інактивації перша, яка, однак, значною мірою залежить від другої.
Взаємодіючи з нуклеїновими кислотами і білками, формальдегід реагує в основному з аміногрупами. Приєднання формальдегіду до аминогруппам пуринів і піримідинів знищує матричну і інформаційну активність нуклеїнових кислот.
Формальдегід з більшою швидкістю взаємодіє з аміногрупами амінокислот і білків з утворенням метілольних похідних, ніж з азотистими підставами нуклеїнових кислот. Склалося уявлення, що з білками і нуклеїновими кислотами вірусів формальдегід реагує в дві стадії. Спочатку, в результаті взаємодії формальдегіду з амино- або іміногрупи, швидко утворюються дуже нестабільні метілольних похідні, а потім, в результаті вторинних реакцій - бісметіленовие похідні.
Продукти взаємодії формальдегіду з амінокислотами здатні вступати в реакцію з нуклеїновими кислотами значно швидше, ніж сам формальдегід.
У другій стадії відбувається повільне взаємодія первинних продуктів реакції з іншими групами білків, в результаті чого утворюються ковалентно пов'язані димери поліпептидів. При цьому ущільнюється білкова оболонка і зменшується її проникність. Внаслідок цього знижується швидкість інактивації вірусу. Під впливом формальдегіду в вирионах кліщового енцефаліту утворювалися глікопротеїнові димери і комплекс РНК з білками нуклеокапсида. Останній відрізнявся високою стабільністю і руйнувався тільки РНКази. Передбачається, що освіта цього комплексу - основний механізм інактивації вірусу. Глікопротеїн, екстрагований з інактивованого вірусу, володів нормальної антигенної та иммуногенной активністю.
Слід зазначити, що реакція формальдегіду з аміногрупами оборотна, тобто при видаленні надлишку реагенту або розведенні розчину активність нуклеїнової кислоти може бути відновлена. Процес взаємодії вірусу з формальдегідом залежить від таких факторів, як концентрація реагенту, температура, рН середовища.
За оптимальних умов інактивації взаємодія формальдегіду з білками багатьох вірусів не робить значного впливу на їх антигенні властивості. Однак ряд вірусів втрачає значну частину антигенної активності при інактивації формаліном. Це особливо стосується оболонкових вірусів і, перш за все, вірусів кору та респіраторно-синцитіальним (PC) вірусу. Наприклад, инактивирован-ва формаліном вакцина проти PC-вірусу викликала утворення антитіл до білка F, що не придушували його інфекційну і сімпластообразующую активність. Більш того, вакцинація приводила до ускладнення перебігу хвороби при подальшому її виникненні. Ймовірно, під дією формаліну змінюються епітопи глікопротеїну, відповідальні за індукцію віруснейтралізуючих антитіл.
Це стосується, перш за все, поверхневого F білка, відповідального за протективний імунітет. Однак багато хто з вірусів, які відносно добре переносять інактивацію формаліном, виявляються досить чутливими до змін її умов. Підвищення концентрації формальдегіду в десять і більше разів в порівнянні з оптимальною (0,1% -ної) призводило до морфологічних змін поверхневого антигену вірусу гепатиту В і зниження його активності, а збільшення тривалості обробки очищеного поліовірусу супроводжувалося значним ушкодженням капсида деяких віріонів. З метою пом'якшення шкідливої дії формальдегіду на антигенність і імуногенність вірусів стали застосовувати стабілізуючі речовини. Встановлено, наприклад, що додавання арілдона (5,4 М) не впливає на інактивацію аттенуірованних і вірулентних штамів поліовірусу формаліном (1: 4000, 37 ° С) і, в той же час, сприяє збереженню імуногенності за рахунок стабілізації D-антигену.