Карбіду (від лат. Carbo - вугілля), соед. вуглецю з металами. а також з бором і кремнієм. За типом хім. зв'язку карбіди ділять на іонні (солеобразние), ковалентні і металлоподобниє (іонно-ковалентно-металеві). Іонні карбіду (див. Табл. 1) утворюють метали I і II гр. (Соотв. М2 С2 і МС2), РЗЕ і актиноїди (МС, М2 С3. МС2), а також Аl. У цих соед. атом С в залежності від типу гібридизації (sp 3. sp 2 або sp) утворює іони З 4. (C = C 4. (С = С = С) 4. (C = C) 2. Ковалентні карбіду (див. Табл. 2) утворюють В і Si; атом С в цих соед. Знаходиться в стані sp- , sp 2 - і sp 3-гібридизації. Металлoподобние карбіди утворюють перехідні метали IV-VII гр. З, Ni і Fe. В цих карбідах зв'язок метал-вуглець іонно-ковалентний, причому атом С негативно заряджений, зв'язок метал - метал чисто металева, атоми С між собою не пов'язані.
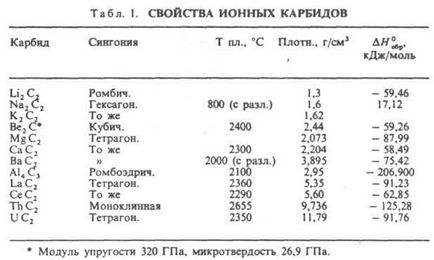
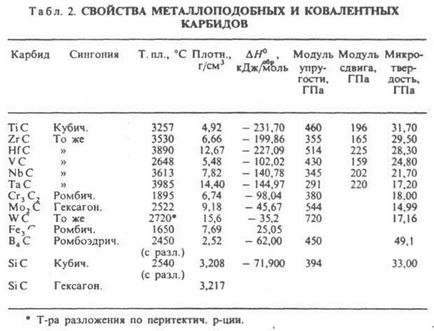
До Арбіден лужних металів кристалізуються в гратах типу графіту. атоми металів розміщуються між вуглецевими шарами, побудованими з гексагoн. сіток. Карбіди щел.-зем. металів кристалізуються в гранецентрір. тетрагон. решітці типу СаС2. карбіди РЗЕ, монокарбіду актиноидов і перехідних металів в гранецентрір. кубічної типу NaCl, сесквікарбіди актиноидов М2 С3 в об'емноцентрір. кубич. решітці типу Рu2 С3. Іонні карбіди лужних металів розкладаються при т-ре ок. 800 ° С, карбіди щел.-зем. металів в інтервалі 1800-2300 ° С, ковалентні карбіди і металлоподобниє розкладаються і плавляться при більш високих т-рах. У периодич. системі в межах групи т-ри плавлення карбідів зростають зі збільшенням порядкового номера металу і зазвичай в 1,5-2 рази вище, ніж т-ри плавлення відповідних металів. Це обумовлено високою міцністю зв'язку М - С. металоподібними карбіди мають металеві. провідність, для них характерний покладе. температурний коеф. r. Для сесквікарбідов величина r (досягає 500 мкОм. См) приблизно на порядок вище, ніж для Дикарбид і монокарбіду (20-50 мкОм. См). Дикарбид РЗЕ також мають металеві. св-вами. Карбіди В і Si, а також Be, Mg і Аl - напівпровідники. Мех. св-ва карбідів залежать від міцності хім. зв'язку, ступеня її ковалентності і межатомного відстані. наиб. високою твердістю мають карбіди В, Si, Be, а також монокарбіду РЗЕ і перехідних металів; твердість останніх зменшується при переході від карбідів підгрупи IVа до карбидам підгрупи VIa. Всі карбіди при кімнатній т-рі - тендітні в-ва, їх пластич. деформація можлива в умовах всебічного стиснення при дуже високій напрузі. Іонні карбіди розкладаються водою з утворенням метану. ацетилену. метилацетилену або суміші вуглеводнів і гідроксиду металу. напр.
Ковалентні і металлоподобниє карбіди не розкладаються водою і більшістю мінер. к-т і лугів. Отримують карбіди з елементів, відновленням оксидів металів. газофазним способом, металотермічних. Синтез з елементів здійснюють при високих т-рах в вакуумі або інертному атмосфері. Залежно від технол. параметрів процесу утворюються порошки з розміром частинок від 0,5 мкм до 2 мм. Синтез може здійснюватися в режимі горіння. т. к. в результаті р-ції виділяється велика кількість тепла, або в плазмі при 5000-10000 До в дугових, високочастотних і надчастотних плазмотронах. В результаті швидкого охолодження з парогазової суміші елементів в плазмообразующих газі (Аr або Не) утворюються ультрадисперсні порошки з розмірами частинок 10-100 нм. Відновленням оксидів металів виробляють наиб. важливі сполуки. - бору карбіду. кремнію карбіди. а також вольфраму карбіду. титану карбід і ін. Карбіди перехідних металів. Газофазним способом отримують карбіди з хім. соед. к-які випаровуються, розкладаються, а потім відновлюються і взаємодій. один з одним, напр.
Найчастіше цей синтез здійснюють в плазмі. отримуючи дисперсні порошки. За металлотерміч. способу оксиди металів відновлюють металами (Mg, Al або Са) у присутності. вуглецю. напр.
МО + С + М g. МС + МgО.
Особливо чисті карбіди, що не містять кисню та азоту. синтезують взаємодій. З і металу в розплаві ін. Металу або сплаву. напр. TiC отримують в сплаві Fe Ni. З іонних карбідів наиб. важливий кальцію карбід СаС2. з ковалентних В4 С і SiC. Металлоподобниє карбіди упрочняют чавун і сталь [Fe3 C, (Fe, Cr) 3 C, Fe2 W2 C, (Fe, Cr, Mo) 23 C6], вони є основою твердих вольфраму сплавів (WC, TiC, WC, TiC, TaC, WC) і ін. твердих сплавів (TiC, VC, Сr3 С2. ТаС), використовуваних для обробки металів різанням. Карбіди застосовують також як відновники. раскислители і каталізатори. вони входять до складу жароміцних і жаростійких композиційних матеріалів. в т. ч. керметів.
===
Ісп. література для статті «Карбідо». Стормс Е. Тугоплавкі карбіди, пров. з англ. М. 1970; Гольдшмідт X. Сплави впровадження, пров. з англ. в. 1-2, М, 1971, Той Л. Карбіди і нітриди перехідних металів. пер. з англ. М, 1974. Самсонов Г. В. Упадхая Г. Ш. Нешпор В. С. Фізичне матеріалознавство карбідів, К. 1974, Високотемпературні карбіди, під ред. Г. В. Самсонова, К, 1975, карбід і сплави на їх основі, під ред. Г. В. Самсонова, К, 1976, Властивості, отримання та застосування тугоплавких сполук, Довідник, під ред. Т. Я. Косолапова. М, 1986, П. С. Кислий.
