Так, в будь-якому атомі, а значить, і в будь-який молекулі повинні бути дрібні електричні частинки. Але чому ж оточуючі нас тіла далеко не завжди обна-ружівают свій заряд? Це можна пояснити дуже про-сто. Електричні заряди атомів не дають про себе знати тому, що позитивний заряд в атомі в точності ра-вен негативного, і дії обох зарядів вже на невеликій відстані від атома взаємно погашаються - заряди нейтралізують один одного. Однак в деяких випадках, наприклад при розчиненні, при нагріванні, атоми можуть втрачати чи приєднувати одну або кілька електричних частинок і перетворюватися в заряджені осколки - іони.
Тепер спробуємо з'ясувати, які електричні частинки може втрачати чи купувати атом - поклади тільні або негативні. Щоб вирішити це питання, ми повинні дізнатися, як розташовані заряди в атомі, як побудований сам атом.
У першому розділі нашої книжки ми вже вирішували за-дачу про розподіл зарядів, захованих в картонній коробці. Така ж по суті завдання стоїть перед нами і зараз. Різниця тільки в масштабах. Атоми мають раз-заходи в кілька стомільйонний часток сантиметра. Зна-чит, і внутріатомні заряди, поміщені одна від одної на відстані не в один сантиметр, як в коробочці, з-бражённой на малюнку 2, а в сто мільйонів разів ближче. Приблизно на таку відстань і потрібно «підібратися» до атома з пробним зарядом. Та й сам пробний заряд повинен бути не важче атома, інакше він буде занадто грубий, - його не зрушать електричні сили атома. Зробити такий заряд не під силу людському мистецтву, але, на щастя, на допомогу тут прийшла сама природа. Проб-ні заряди доставили нам радіоактивні речовини. Електрони, що випускаються цими речовинами альфа-частинки виявилися цілком придатними для «промацування» внутрішньоатомних зарядів. Альфа-частинки досить малі і легкі. Ско-рости їх величезні: зустрічаються альфа-частинки, що летять зі швидкістю 20 ТОВ кілометрів в секунду. Альфа-ча - стіци мають позитивний електричний заряд. Таким чином, вони цілком підходять для дослідження будови атома.
Але як провести досвід? Побачити окремі атоми і альфа-частинки не можна навіть в самий сильний мікроскоп. Але ж ми повинні заглянути всередину атома і по поведе-ням альфа-частинок дізнатися, як розташовані в атомі за-ряди.
Перш за все треба було знайти спосіб, як стежити за шляхами альфа-частинок. Це зробити вдалося. Є ве-суспільством - сірчистий цинк, - яке має інтерес-ним властивістю: якщо на нього падає альфа-частинки, воно світиться - дає короткочасну спалах. За спалаху можна дізнатися, куди потрапила вилетіла з крупиці ра-радіоактивного речовини альфа-частинки, а знаючи це місце, можна, очевидно, збагнути, яким шляхом вона летіла, хоча в польоті і залишалася невидимою.
Потім слід було знайти потрібну для альфа-ча - стіци мішень. Такий мішенню послужив дуже тонкий, товщиною в тисячну частку міліметра, листок металу.
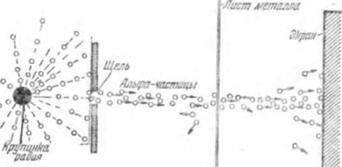
Установка для досліду була зібрана так, як схематі-но показано на рис. 4. Велика чорна точка зліва - крихта радіоактивного елемента радію. З неї в усіх напрямках безперервним потоком вилітають альфа - частинки. Щілина, що прорізає в товстій металевій пластинці, пропускає вузький «промінь» альфа-частинок. Він па-дає на мішень - тонкий листок металу. А за листком поставлений екран, покритий сірчистим цинком.
І ось виявляється, що тонкий листок металу - не перешкода для мчать з величезною швидкістю альфа - частинок. Вони пронизують листок наскрізь і, падаючи на середину екрана, дають яскраве світіння. Це навело вчених на думку, що атом зовсім не є суцільною часткою речовини, а складається з окремих частин, розділених пу-простим простором, через яке альфа-частинки можуть вільно пролітати.
Але деякі альфа-частинки поводяться інакше. Вони відхиляються від прямого шляху. Це видно з того, що в інших місцях екрану теж спалахують і гаснуть від-слушні іскорки - сліди ударів альфа-частинок, змінивши-ших свій напрямок. Більшість частинок лише трохи змінює напрямок свого польоту, але є і такі, ко-торие відхиляються сильно, а деякі відскакують назад. Як це пояснити?
Альфа-частинка заряджена позитивно. Значить, від-хилити її може тільки деякий позитивний заряд в атомі, або, точніше, позитивно заряджена частина атома, більш важка, ніж сама альфа-частинки. Цю частину атома називають ядром. Якщо альфа-частинки налітає прямо на ядро, «лобовим ударом», то вона може бути відкинута назад. Оскільки таких частинок в нашому досвіді мало, ми робимо висновок, що потрапляння в ядро - рідкісний випадок. А це свідчить про те, що раз-заходи ядра дуже малі.
Тепер картина проходження альфа-частинок через металевий листок ясна: частинки, що не випробували відхилення від прямолінійного шляху, пройшли далеко від атомних ядер. Частинки, відхилилися в сторону, про-йшли на невеликих відстанях від ядер, і дуже небагато частинок потрапило прямо в ядро і було відкинуто назад.
Таким чином, досвід з обстрілом атома альфа-частини-цями доводить нам, що позитивні заряди атома зосереджені в маленькому важкому ядрі. А отрицатель-ні? Вони не дають про себе знати в цьому досвіді. Вони вдосконалення-шенно не діють на альфа-частинку, не можуть притягнути її до себе. І нам залишається зробити висновок, що негативні заряди у вигляді легких найдрібніших частинок розподілені навколо ядра. Ці найдрібніші частинки негативного електрики і були названі електронами.
Як же тепер ми повинні уявляти собі будову атома? - У центрі атома знаходиться ядро. У ньому заклю-1 чени все позитивні заряди атома і майже вся його маса (рис. 5). А навколо ядра розташовуються електрони.
Електрони становлять оболонку атома, легко прони-цаемую для альфа-частинок. Виходячи з цього, ми можемо припустити, що саме електрони, як більш легкі і тому більш рухливі, слабкіше пов'язані з атомом і можуть переходити від одного атома до іншого.
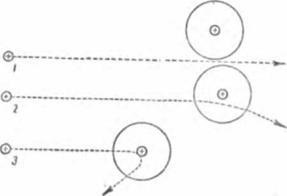
Мал. 5. Альфа-частинки зустрічають на своєму шляху атоми металу. Цифрами 7, 2 і 3 позначені альфа-частинки; великі гуртки -атоми, в центрі їх - позитивно заряджені ядра.
Досліди це повністю підтвердили. Виявилося, що багато атоми, наприклад атоми металів, легко втрачають частину своїх електронів. Це відбувається і при нагрівання-ванні, і при освітленні, і при дії тих же альфа-ча - стіц. Інші ж атоми, навпаки, більш схильні присівши-об'єднуючим до своєї оболонці зайві електрони. Як від-рив, так і приєднання електронів до атома називають іонізацією (бо атом при цьому перетворюється-тається в іон).
Тепер ми можемо відповісти і на запитання про те, як з молекули соляної кислоти при розчиненні виходять позитивний іон водню і негативний іон хлору. Атом водню віддає електрон атома хлору, і в резуль-таті в оболонці атома хлору виявляється надлишок отри-цательних зарядів (по. Порівняно з кількістю поклади-них зарядів в ядрі), а водневий атом стає позитивно зарядженим іоном. Так як водневий атом віддав тільки один електрон, а атом хлору отримав цей електрон, то очевидно, що заряди отриманих іонів рівні заряду електрона.