Визначення молекулярної маси проводиться різними методами: осмометріческім, гельфільтраціонним, оптичним та ін. Проте найбільш точним є метод седиментації, запропонований Т. Сведбергом. Він заснований на тому, що при ультрацентріфугірованіі прискоренням до 900 000 g швидкість осадження білків залежить від їх молекулярної маси.
Найважливішим властивістю білків є їх здатність проявляти як кислі так і основні, тобто виступати в ролі амфотерних електролітів. Це забезпечується за рахунок різних диссоциирующих угруповань, що входять до складу радикалів амінокислот. Наприклад, кислотні властивості білку надають карбоксильні групи аспарагінової глутамінової амінокислот, а лужні - радикали аргініну, лізину і гістидину. Чим більше дикарбонових амінокислот міститься в білку, тим сильніше виявляються його кислотні властивості і навпаки.
Ці ж угруповання мають і електричні заряди, що формують загальний заряд білкової молекули. У білках, де переважають аспарагінова і глутамінова амінокислоти, заряд білка буде негативним, надлишок основних амінокислот надає позитивний заряд білкової молекули. Внаслідок цього в електричному полі білки пересуватимуться до катоду або анода в залежності від величини їх загального заряду. Так, в лужному середовищі (рН 7 - 14) білок віддає протон і заряджається негативно, тоді як в кислому середовищі (рН 1 - 7) пригнічується дисоціація кислотних груп і білок стає катіоном.
Таким чином, фактором, що визначає поведінку білка як катіона або аніона, є реакція середовища, яка визначається концентрацією водневих іонів і виражається величиною рН. Однак при певних значеннях рН число позитивних і негативних зарядів зрівнюється і молекула стає електронейтральної, тобто вона не буде переміщатися в електричному полі. Таке значення рН середовища визначається як ізоелектричної точка білків. При цьому білок знаходиться в найменш стійкому стані і при незначних змінах рН в кислу або лужну сторону легко випадає в осад. Для більшості природних білків ізоелектрична точка знаходиться в слабокислою середовищі (рН 4,8 - 5,4), що свідчить про переважання в їх складі дикарбонових амінокислот.
Властивість амфотерности лежить в основі буферних властивостей білків і їх участі в регуляції рН крові. Величина рН крові людини відрізняється постійністю і знаходиться в межах 7,36 - 7,4. незважаючи на різні речовини кислого або основного характеру, регулярно надходять з їжею або утворюються в обмінних процесах - отже існують спеціальні механізми регуляції кислотно-лужної рівноваги внутрішнього середовища організму. До таких систем відноситься розглянута в гл. "Класифікація" гемоглобіновая буферна система (стор.28). Зміна рН крові більш ніж на 0,07 свідчить про розвиток патологічного процесу. Зрушення рН в кислу сторону називається ацидозом, а в лужну - алкалозом.
Важливе значення для організму має здатність білків адсорбіроватьь на своїй поверхні деякі речовини і іони (гормони, вітаміни, залізо, мідь), які або погано розчинні у воді, або є токсичними (білірубін, вільні жирні кислоти). Білки транспортують їх по крові до місць подальших перетворень або знешкодження.
Водні розчини білків мають свої особливості. По-перше, білки мають більшу спорідненість до води, тобто вони гідрофільних. Це означає, що молекули білка, як заряджені частинки, притягують до себе диполі води, які розташовуються навколо білкової молекули і утворюють водну або гідрадну оболонку. Ця оболонка охороняє молекули білка від склеювання і випадання в осад. Величина гідратної оболонки залежить від структури білка. Наприклад, альбуміни легше зв'язуються з молекулами води і мають відносно велику водну оболонку, тоді як глобуліни, фібриноген приєднують воду гірше, і гідратне оболонка і них менше. Таким чином, стійкість водного розчину білка визначається двома факторами: наявністю заряду білкової молекули і навколишнього неї водної оболонки. При видаленні цих факторів білок випадає в осад. Даний процес може бути оборотним і необоротним.
Оборотне осадження білків (висолювання) передбачає випадання білка в осад під дією певних речовин, після видалення яких він знову повертається в своє початкове (нативное) стан. Для висолювання білків використовують солі лужних і лужноземельних металів (найчастіше в практиці використовують сульфат натрію і амонію). Ці солі видаляють водну оболонку (викликають зневоднення) і знімають заряд. Між величиною водної оболонки білкових молекул і концентрацією солей існує пряма залежність: чим менше гидратная оболонка, тим менше потрібно солей. Так, глобуліни, які мають великі і важкі молекули і невелику водну оболонку, випадають в осад при неповному насиченні розчину солями, а альбуміни як більш дрібні молекули, оточені великою водною оболонкою, - при повному насиченні.
Нативная молекула білка
Денатурована молекула білка. Рисочки позначають зв'язку в молекулі нативного білка, що розриваються при денатурації

еобратімое осадження пов'язано з глибокими внутрішньомолекулярними змінами структури білка, що призводить у втраті ними нативних властивостей (розчинності, біологічної активності та ін.). Такий білок називається денатурованим, а процес денатурацією. Денатурація білків відбувається в шлунку, де є сильнокислая середовище (рН 0,5 - 1,5), і це сприяє розщепленню білків протеолітичними ферментами. Денатурація білків покладена в основу лікування отруєння важкими металами, коли хворому вводять per os ( "через рот") молоко або сирі яйця з тим, щоб метали денатуруючи білки молока або яєць.
Адсорбувати на їх поверхні і не діяли на білки слизової оболонки шлунка і кишечника, а також не всмоктувалися в кров.
Розмір білкових молекул лежить в межах 1 мкм до 1 нм і, отже, вони є колоїдними частинками, які у воді утворюють колоїдні розчини. Ці розчини характеризуються високою в'язкістю, здатністю розсіювати промені видимого світла, не проходять крізь напівпроникні мембрани.
В'язкість розчину залежить від молекулярної маси і концентрації розчиненого речовини. Чим вище молекулярна маса, тим розчин більш в'язкий. Білки як високомолекулярні сполуки утворюють в'язкі розчини. Наприклад, розчин яєчного білка у воді.
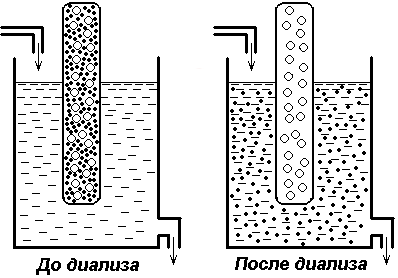
оллоідние частки не проходять через напівпроникні мембрани (целофан, колоїдну плівку), так як їх пори менше колоїдних частинок. Непроникними для білка є всі біологічні мембрани. Це властивість білкових розчинів широко використовується в медицині і хімії для очищення білкових препаратів від сторонніх домішок. Такий процес поділу називається діалізом. Явище діалізу лежить в основі дії апарату "штучна нирка", який широко використовується в медицині для лікування гострої ниркової недостатності.
Діаліз (білі великі гуртки - молекули білка, чорні - молекули хлористого натрію)
Мінеральні речовини молока
Структурно-механічні властивості масла.
За Ребиндера існують два основних типи структур.
Перший тип - коагуляционная структура - це просторові сітки, що виникають шляхом безладного зчеплення найдрібніших частинок дисперсної фази або Мікромолекули через тонкі розшарування даного середовища.
Другий тип - це центр кристалізації-конденсаційна структура. утворюється в результаті безпосереднього зрощення кристалів з утворенням при цьому полікристалічного твердого тіла.
Жирові основи маргарину відносяться до коагуляционному типу структур. Консистенція і пластичні властивості жирових основ маргарину в основному визначаються співвідношенням твердої і рідкої фаз в тому чи іншому харчовому жирі. Це співвідношення твердої і рідкої фаз характерно для якихось певних умов кристалізації (температура, час, перемішування). При цьому важливе значення має склад безперервної середовища і дисперсної фази і характер розміщення дисперсної фази в безперервній рідкому середовищі.
Для деяких видів харчового жиру при певній температурі і умовах кристалізації кількість твердої дисперсної фази може вийти за межу оптимального співвідношення фаз, і тоді на поверхні кристалів утворюються настільки тонкі плівки безперервної рідкого середовища, що вони не можуть заважати масовому хаотичного зрощенню кристалів один з одним. В цьому випадку ми завжди будемо мати найбільшу твердість жирової основи, крихкої консистенції і найгірші пластичні властивості.
Якщо при кімнатній температурі плівки рідкої безперервної середовища є оптимальними по товщині, тобто такими, які не створюють умов для зрощування кристалів при зберіганні, при механічному або термічному впливі на систему, то в цьому ідеальному випадку ми завжди будемо отримувати зміцнені коагуляційні структури, які і визначають найкращі пластичні властивості жирових основ.
Щоб отримувати зміцнені коагуляційні структури, що володіють найкращими пластичними властивостями, за кордоном часто вводять в рецептуру жирової основи два види саломаса з температурою плавлення 32 ° С і 42 ° С. При цьому вводиться досить значна кількість рідких рослинних масел. Зазначене, з одного боку, створює в жировій основі найкращі співвідношення твердої і рідкої фаз, забезпечуючи консистенцію, подібну з вершковим маслом, а з іншого боку, створює умови для сталості консистенції маргарину в досить великому інтервалі температур. Поряд з цим, введення в жирову основу високоплавких саломасов знаходиться в протиріччі з вимогами фізіологів до складу харчових жирів.
Перш за все, слід зазначити, що тільки наявність високоефективних емульгаторів-стабілізаторів дозволило створити сучасну технологію у виробництві маргарину і забезпечити вироблення харчового жирового продукту високої якості. Поверхнево-активні добавки забезпечують отримання тонкодисперсної емульсії в міцний зв'язок частинок дисперсної фази з безперервною середовищем (твердим при кімнатній температурі жиром). Основне питання в виробництві маргарину - це вплив поверхнево-активних добавок на структурно-механічні властивості маргарину, і зокрема на здатність до солюбилизации.
Адсорбційний шар емульгатора підвищує стійкість емульсії, особливо в тих випадках, коли цей шар структурується, утворюючи плівку поверхневого гелю з сильно підвищеною в'язкістю і міцністю.
Ці властивості мають особливе значення для виробництва маргарину, оскільки готовий продукт являє собою емульсію найдрібніших частинок рідкої фази, рівномірно розміщених в безперервному середовищі твердої фази при кімнатній температурі.
З проблемою міцності емульсій тісно пов'язане питання про тип утворюються з даними емульгатором емульсій. Існує можливість утворення двох типів. Значення співвідношення обсягів фаз для певного типу утворюється емульсії пояснюється тим, що коалесценція і розшарування емульсії даного типу відбуваються тим інтенсивніше, чим менший об'єм дисперсійного середовища і чим більше - дисперсної фази. Якщо емульгатор забезпечує стійку емульсію тільки одного типу, то співвідношення обсягів перестає мати вирішальне значення у визначенні типу емульсії. Інверсія залежить не тільки від співвідношення обсягів фаз, але і від концентрації і хімічної природи емульгатора.
Емульгатори повинні мати наступні властивості:
- зменшувати поверхневий натяг;
- досить швидко адсорбироваться на поверхні розділу фаз, перешкоджаючи злиття крапель;
- мати специфічну молекулярну структуру з полярними і неполярними групами;
- впливати на в'язкість емульсії.
Ефективність дії емульгатора є специфічною властивістю, що залежать від його природи, типу емульгіруемость речовин, температури, рН середовища, концентрації, часу емульгування і т.д.
Ефективність дії і природа емульгатора визначають тип емульсії.
Гідрофільні емульгатори, краще розчинні у воді, ніж у вуглеводнях, сприяють утворенню емульсій типу масло - вода, а гідрофобні, краще розчинні у вуглеводнях, - емульсій типу вода - масло. Співвідношення розмірів полярної і неполярний частин молекул емульгатора характеризується спеціальним показником - гідрофільно-ліпофільний баланс. Якщо ГЛБ емульгатора становить 3-6, утворюється емульсія вода - масло, при значенні ГЛБ 8-13 утворюється переважно емульсія типу олія - вода.
Маргарин являє собою переохолоджену емульсію типу вода в маслі. При цьому не виключена можливість утворення емульсії змішаного типу з переважанням емульсії вода - масло.
Основні функції емульгаторів:
- створення стійкої високодисперсною емульсії;
- стабілізація і запобігання відділення вологи і жиру в готовому продукті;
- забезпечення стабільності при зберіганні;
- забезпечення антіразбризгівающей здатності при смаженні;
- забезпечення пластичності;
- забезпечення створення стійкої форми кристалічної решітки в процесі структуроутворення;
- забезпечення заданих функціональних властивостей готового продукту в залежності від галузі використання маргарину.
В Україні протягом багатьох років використовувалися емульгатори, вироблені в Росії, і власного виробництва, що виробляються на напівпромислових виробництвах. До них відносяться емульгатори:
- Т-1 - продукт гліцероліза яловичого жиру або саломаса;
- Т-2 - продукт полімеризації гліцерину, етерифіковані стеаринової кислотою;
- Т-Ф - суміш емульгатора Т-1 і харчового фосфатидного концентрату в співвідношенні 2: 1;
- ПМД - харчові монодігліцеріди;
- КЕ - комбінований емульгатор - суміш ПМД і фосфатидного концентрату в співвідношенні 3: 1.
Широка гамма емульгаторів Нижегородського заводу - різні види дистильованих моногліцеридів. В даний час в Нижньому Новгороді освоєно виробництво серії нових емульгаторів на основі лецитину. Це лецитини стандартні, лецитини фракціоновані - фосфадітілхолін і фосфадітілсерін, а також гідролізовані лецитини.
В останні роки в Україні переважно використовуються емульгатори різних модифікацій серії Dimodan, Palsgaard (на деяких підприємствах Квест).
У різні періоди перевага в попиті на ці два види емульгаторів переходило від одного до іншого. Можна сказати, що тут має місце конкуренція якість - ціна.
Залежно від жирності маргарину і сфери його застосування використовують емульгатори Dimodan PVP (Dimodan HP), Dimodan ВІД (Dimodan S-T PEL / B), Dimodan НГ. Для маргаринів жирністю нижче 40%, які в даний час користуються попитом у населення, використовують додатково (крім Dimodan ВІД, або Dimodan НГ. Або Dimodan LS) ефіри полігліцерина і рицинолевої кислоти - Grinsted PGPR90.
Слід зазначити, що фірми-виробники дають рекомендації щодо застосування різних видів емульгаторів і стабілізуючих систем в залежності від призначення маргаринів. Дотримання цих рекомендацій дозволяє отримати продукцію високої якості