Порфірини. природні макрогетероциклічних пігменти, що містять в молекулі цикл порфина (формула I). Формально виходять з порфина заміщенням атомів Н в циклі на різні органічне радикали. До Порфірини відносять такі важливі пігменти, як гемо- глобіну, хлорофіли, цитохроми і деякі ін. Ферменти (каталаза, пероксидаза). Виявлено Порфірини також у виділеннях тварин, оперенні птахів, шкаралупі яєць, раковинах молюсків, нафтах, бітумах, копалин органічне залишках, метеоритах.
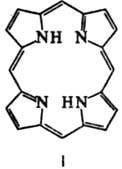
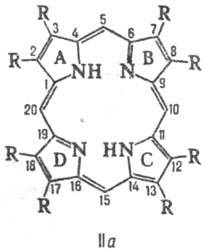
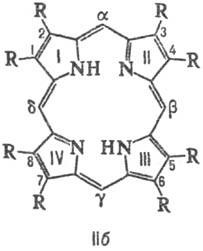
Атоми З в Порфірини нумерують, згідно але номенклатури ІЮПАК (формула Па) або Фішера (Ш). Чотири атома С (5, 10, 15 і 20 у формулі Ш), що зв'язують піррольних цикли, називають мезо-вугле-рідними атомами.
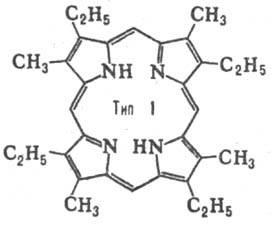
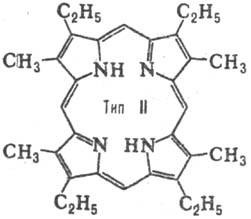
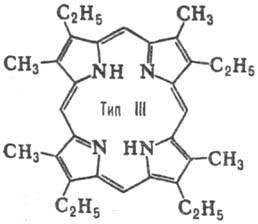
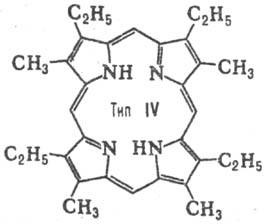
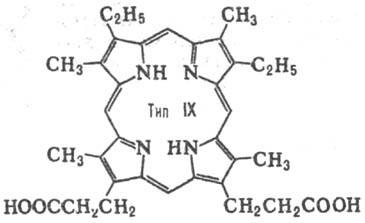
Число ізомерів положення для Порфірини визначається кількістю заступників і їх розташуванням в молекулі. Для Порфірини з двома заступниками (наприклад, СН3 і С2 Н5) за умови, що обидва заступники присутні в кожному піррольних циклі, можливі 4 типи ізомерів. При наявності трьох різні заступників число типів зростає до 15. Природні Порфірини з двома заступниками мають головним чином розташуванням типу III, з трьома-типу IX (див. Табл.).
Порфина і порфіринів-високоплавкі інтенсивно забарвлені сполуки (головним чином темно-червоного кольору); т. різні порфина 360 ° С, порфіринів-близько 500 ° С Порфірини добре розчинний в СНCl3. ДМФА, гірше в етанолі і метанолі, не розчинний у воді. Молекули Порфірини плоскі і зазвичай асоційовані внаслідок утворення водневих зв'язків. В УФ спектрі Порфірини l макс
400 нм (так званої смуга Сорі, е 400 000), 500 600 нм (е 15 000 і менше)
Порфірини-ароматичні структури; мають високу енергією сполучення (840 кДж / моль), що проявляється в стабільності з'єднань. Для порфіринового циклу характерна наявність двох таутомерних форм:
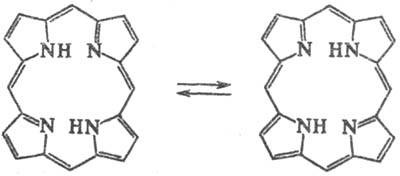
Порфірини-амфотерні сполуки; атоми N в молекулі здатні приєднувати протони з утворенням моно- або дікатіо-нів, обидві групи NH-отщеплять протони з утворенням моно- або діаніонов: РН2порфірін, Р 2 -діаніон, -дікатіон Порфірини-слабкі кислоти; Рк1 і РК2 (для етіопорфіріна) +16, рК3 октаалкілпорфірінов близько +5,5 (2,5% -ний водний розчин додецилсульфату Na).
При взаємодія з солями металів Порфірини утворюють метало-порфірини, найважливіший з яких-гем, або ферропрото-порфирин (див. Гемоглобін); найбільш важливий гидрируются. метало-порфирин-хлорофіл. Металлопорфиринов легко вступають в реакції електрофор. заміщення, головним чином по мезо-положенням. Для вільних порфіринів ці реакції утруднені внаслідок утворення в кислому середовищі дікатіона, який не вступає в електрофор. реакції.
Порфірини і їх металокомплексів легко відновлюються. Найлегше протікає електрохімічний відновлення з утворенням моно- і діаніонов, які є сильними ну-клеофіламі і швидко реагують (головним чином по мезо-вуглець-ним атомам) з донорами протонів і такими електрофілами, як СН3 I. М'яке гідрування циклу Порфірини призводить до хлорину (формула III) і Флорін (IV), більш глибоке-к бактеріохлорінам (V), порфодіметенам (VI), порфомете-нам (VII) і порфіріногенам (VIII).
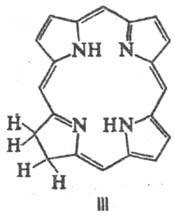
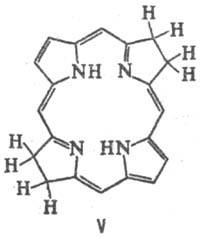
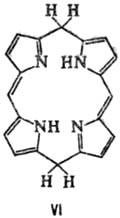
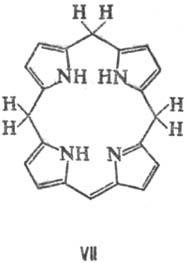
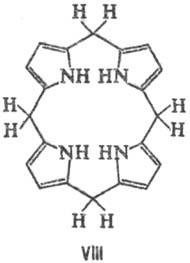
Якщо в Порфірини присутні ненасичені заступники, наприклад ві-нільная група, то до порфіріногенов такі з'єднання відновлюються амальгамою Na. Обробка порфіріногенов О2 повітря на світлі, йодом або 2,3-дихлор-5,6-діціанобен-зохіноном призводить до їх переходу в Порфірини Під дією HI відбувається, як правило, розрив кільця Порфірини і освіту суміші піролів.
Під дією м'яких окислювачів або електрохімічних Порфірини і їх металокомплексів утворюють продукти окислення-катіон-радикали, під дією сильних окислювачів (наприклад, СrO3. КМnО4) відбувається розрив кільця:
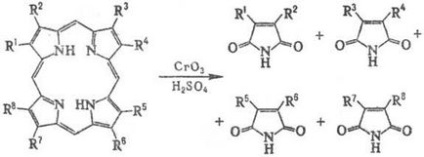
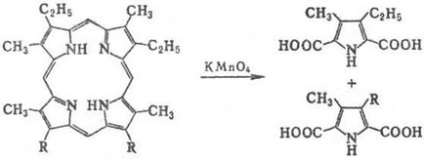
Окислить. розщеплення Порфірини в організмі призводить до утворення жовчних пігментів. Порфірини порівняно легко метіліруется по атомам N, наприклад
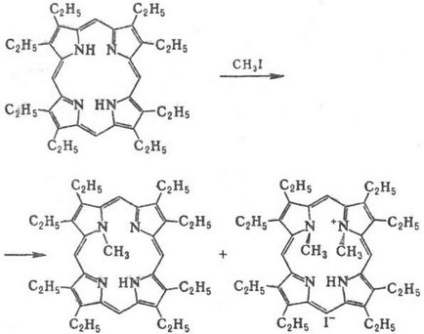
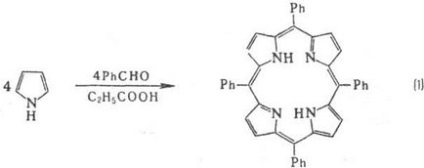
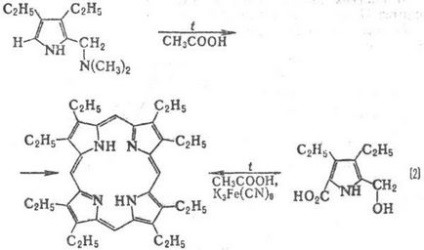
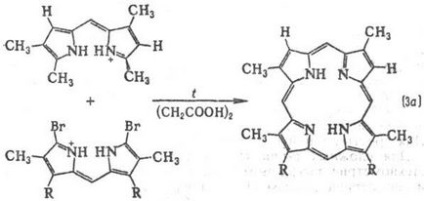
Метальних групи відчувають просторів. труднощі, внаслідок чого макроцикл виявляється "гофрованим". Методи синтезу порфіринів: конденсація монопірролов з альдегідами (реакція 1); самоконденсаціі монопірролов, що містять в положенні 2 групу СН2 Х, де X = О Ас, ОН, Сl, Вr, N (CH3) 2 (реакція 2); конденсація діпіррілметенов і діпірастворілметанов (3а і 3б); конденсація тетрапіррольних Інгер-Медиатим, які може бути отримано, в свою чергу, з діпіррілметенов, діпіррілметанов або ступінчастим синтезом з монопірролов (наприклад, реакція 4).
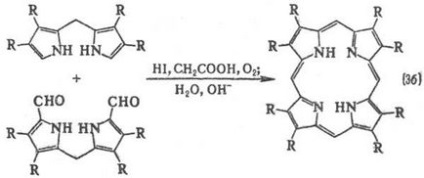
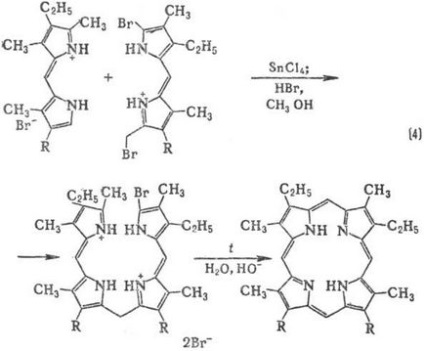
У клітинах рослинних і тваринних організмів біосинтез порфіринів здійснюється з гліцину і янтарної кислоти.
ПОРФІРІНИ- основа деяких природні барвників, модельні сполуки для вивчення процесу оксигенації при фотосинтезі, лек. препарати в терапії раку (наприклад, димер гематопорфірину-фото-Фрін); металлокомплексов Порфірини-каталізатори окислення і епоксідірованія вуглеводнів.
Література: Хімія біологічно активних природних сполук, під ред. Н.А. Преображенського і Р.П. Євстигнєєва, М. 1976, с. 100-84; Загальна органічна хімія, пер. з англ. т. 8, М. 1985, с. 388-413; Порфірини: структура, властивості, синтез, під ред. Н.С. Еніколопяна, М. 1985; Порфірини: спектроскопія, електрохімія, застосування, під ред. Н.С. Еніколопяна, М. 1987; Falk J. E. Porphyrins and meta! Lopcrphyrins, Amst.-L.-N. Y. 1964; Dolphin D. (ed.), The Porphyrins. Structure and synthesis, v. 1, pt A, L.-N. Y. 1978. P. Порфірини Євстигнєєва.
Хімічна енциклопедія. Том 4 >> До списку статей