При зміні зовнішніх умов пасивний метал може знову перейти в активний стан. Цей процес називають активацією, або депассіваціей. Речовини або процеси, що порушують пасивний стан металів або ускладнюють наступ пасивності, називають активаторами або депассіваторамі. [C.306]
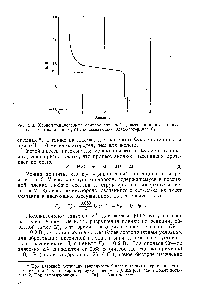
Мал. 5.3. Хронопотенціограмма мимовільної депассіваціі заліза після виключення струму в 1 н. Н23 04, що показує Флад-потенціал Ер
Перші два сплаву іноді легируют титаном або ніобієм для підвищення допустимого вмісту вуглецю і азоту. Всі ці сплави можна загартовувати від 925 ° С без погіршення корозійних властивостей. Завдяки тому, що вони зберігають пасивність в агресивних середовищах. їх корозійна стійкість зазвичай вище, ніж у звичайних феритних і деяких аустенітних нержавіючих сталей. представлених в табл. 18.2. Вони більш стійкі. наприклад в розчинах Na l, HNO3 і різних органічних кислот. Якщо з якої-небудь причини відбувається локальна або загальна депассівація цих сталей, то вони піддаються корозії з більшою швидкістю. ніж активовані никельсодержащие аустенітні нержавіючі стали. мають в своєму складі такі ж кількості хрому і молібдену [8, 9]. [C.301]
Ряд дослідників, визнаючи електрохімічний природу корозійного розтріскування металів. вказують на переважне значення конкуренції депассіваціі і пасивації, локалізованої на концентраторах механічної напруги. [C.335]
А в роботі [8а] показано, що час депассіваціі сплавів збільшується з ростом вмісту хрому. в той час як Флад-потенціал зменшується. [C.75]
Потенціал Р (см. Рис. 5.1), при якому починається пассивация заліза (потенціал пасивації) близький до Флад-потенціалу, але не дорівнює йому, так як, по-перше, існує омічний падіння напруги в ізолюючому шарі. і по-друге, внаслідок того, що pH електроліту в глибині пір цього шару відрізняється від pH в обсязі електроліту (концентраційна поляризація). На процес депассіваціі ці обставини не впливають. [C.75]
Випадає гідроокис заліза видаляють фільтруванням. При концентрації золота 1-2 л і при температурі електроліту 18-25 ° С щільні опади золота виходять лише при щільності струму 0,1-0,2 а дм з виходом по току 25-35%. Для депассіваціі золотих анодів в електроліт вводять сегнетову сіль. При застосуванні більш концентрованих по металу електролітів (10-25 г л Лі) і нагріванні електроліту до 70 ° С можлива інтенсифікація процесу (катодна щільність струму до 6 а / дм). При роботі з нерозчинними анодами (графіт, платина, нержавіюча сталь) в електроліті можуть накопичуватися іони Си ". [C.209]
На стан пасивності істотно впливають де-Пасиватор, серед яких особливо активні іони хлору. які адсорбуються на аноді, десорбіруя при цьому кисень або витісняючи його з вузлів кристалічної решітки фазової плівки. Оскільки іони хлору дають добре розчинні сполуки, то при введенні їх в електроліт пасивний стан нікелю усувається або не виникає взагалі. Підвищення температури також сприяє депассіваціі анода, так як збільшується розчинність пасивуються плівки в електроліті. Якщо ж пасивність обумовлена адсорбцією кисню. то з підвищенням температури відбувається його десорбція. [C.276]
Промивання і сушіння готового продукту. Витягнуті з електролізера графітові анодні стрижні з осадом ЕДМ-2 подрібнюють в щековой дробарці і направляють в металургійну осадочную машину для відділення графіту. При використанні свинцевих анодів свинець після зняття діоксиду марганцю направляється на переплавку для виготовлення нових анодів. Титанові аноди після депассіваціі використовують повторно. [C.194]
Сторонні аніони, що накопичуються в розчині, не беруть участі в електрохімічних реакціях за винятком іонів хлору, які можуть викликати депассівацію анода. Накопичення карбонатів, що утворюються в результаті поглинання діоксиду вуглецю з навколишньої атмосфери. допускається до значень, при яких істотно не зменшується електропровідність розчину. [C.127]
На процес корозії істотно впливає засоленість ґрунту та наявність в ньому хімічно агресивних речовин. Зі збільшенням їх концентрації в ґрунтовій воді число вогнищ корозії скорочується, а глибина каверн і піт-тингов зростає. Руйнування труб в значній мірі сприяє присутність хлоридів і сульфатів, які при певній концентрації викликають депассівацію стали і активізують швидкість. її розчинення. Дослідженнями, встановлено, що при утриманні іона сульфату в розчині більше 50-100 мг / л відбувається депассівація стали, причому з підвищенням температури процес цей активізується [7]. Так як водні витяжки з пінобетону і мінеральної вати містять 500-550 мг / л SOi (при pH = 11,5 і 8), то трубна сталь може активно розчинятися під цими теплоізоляційними матеріалами. Швидкість розчинення стали в реальних умовах буде визначатися доступом кисню. [C.15]
Важливими показниками морської води як корозійного середовища є концентрація солей і водневих іонів (pH), її електропровідність. Величина pH в морській воді різних басейнів становить 8,1-8,4. Висока солоність і ступінь дисоціації забезпечують наявність великої кількості хлор-іонів. які витісняють кисень з окисної захисної плівки металу, викликають депассівацію. Тому найбільш раціонально морські споруди захищати лакофарбовим покриттям в комплексі з електрохімічної захистом. [C.70]
Пасивність металу - стан досить високої корозійної стійкості, обумовлене гальмуванням анодної реакції іонізації в певній галузі потенціалів. Перехід металу з активного стану в пасивне називається пасивацією, зворотний Процес зазвичай називають депассіваціей (активацією). Уповільнення корозії поверхні металу при пасивації обумовлено утворенням на ній фазових або адсорбційних плівок. [C.20]
Промивання діоксиду марганцю. При отриманні ЕДМ-2 витягнутий-н, перші з електролізера графітові анодні стрижні з осадом МПНВ подрібнюють в щековой дробарці. Потім графіт відокремлюють від МПНВ в металургійній осадової машині. При роботі на свинцевих анодних стрижнях свинець після зняття МПНВ йде на переплавку для виготовлення нових анодних стержнів. Титанові анодні стрижні після депассіваціі використовуються повторно. Шматки МПНВ розмелюють так, щоб 95% проходило через сито 100 мещ, а 65% -через сито 200 меш. Отриманий продукт промивають, фільтрують і подають на сушку. [C.184]
Щоб уникнути депассіваціі анодів необхідно стежити, щоб напруги ня на Ваїне було не менше 3,5-4 В. [c.203]
В ефективно зростаючої тріщині повинна встановлюватися негативний зворотний зв'язок між ступенем локалізації корозії і агресивністю (складом) внутрішньої мікросередовища. За відсутності такого зв'язку агресивність внутрішнього середовища за рахунок гідролізу розчинних продуктів корозії може вирости до значень, що викликають депассівацію бічних стінок тріщини. Це призведе до округлення вістря тріщини і далі до переродження її в піттінг. [C.112]
При поаи1іеніі поляризації частка активної поверхні збільшується в результаті зростання числа двомірних зародків і переходу раніше неактивних ділянок зростання в активні (депассівація). Крім того, при смещеіні потегщіала в негативну сторону підвищується концентрація частинок. Все це призводить до збільшення градієнта концентрації, в результаті чого поверхнева дифузія перестає бути уповільненою стадією. Швидкість процесу осадження почне лимитироваться інший стадією, найбільш ймовірно - стадією переносу заряду. При ще великих поля- [c.342]
Відбувається депассівація захисного шару і корозія розвивається зі значною швидкістю. Це пояснюється збільшенням а, 1сорб-ції активують агентів при збільшенні потенціалу. Адсорбція відбувається на дефектних частинах окисної плівки. в результаті утворюються сульфіти, сульфати і карбонати, добре розчиняються у воді, що призводить до виразкової корозії. [C.116]
При зміні зовнішніх умов пассівньпг метал може знову перейти в активний стан. Цей процес називають депассіваціей або активацією, а речовини нли процеси, що сприяють порушенню пасивного стану. називають депассіваторамі і.лн активаторами. [C.51]
Зовнішня поляризація змінним струмом збільшує корозію металів. так як в цьому випадку періодично низку ються анодний і катодний поляризація (анодні і катодні напівперіоди струму). Змінний струм ускладнює також проіесс пассивации у пасивуються мета.плов внаслідок протікання відновних реакцій і депассіваціі утворюються плівок в катодний напівперіод струму. [C.56]
Зіставляючи криві зносу платини на ПТА, отримані радіоізотопним і ваговим методами. Можьо зробити висновок. що крива на рис. У-14 є відповідним продовженням кривої 2 на рис. У-13. В умовах переривання процесу електролізу через кожні 6-7 год постійна швидкість корозії платини не була одержана навіть після 300 ч анодної поляризації. Дані про швидкість корозії платини. отримані в цих дослідах, очевидно, завищені через деякій депассіваціі платини під час перерв процесу електролізу [11, 45]. [C.159]
Теоретична електрохімія Видання 3 (1970) - [c.590]