З правила Лешательє слід, що підвищення тиску буде сприятливо позначатися як на рівновазі реакції окислення в - воно буде зміщуватися в бік освіти, так і на збільшенні її швидкості, бо підвищення тиску даному випадку рівносильно підвищенню концентрації і, що беруть участь в реакції. Зі збільшенням тиску обсяг апаратів в контактній системі може бути значно меншим. Однак підвищений тиск при контактному способі виробництва сірчаної кислоти не отримало застосування. Це пояснюється тим, що зі збільшенням тиску виникають труднощі в підборі каталізатора і в аппаратурном оформленні процесу, в той час як і при атмосферному тиску можна отримати досить високі ступінь контактування і швидкість течії процесу. Крім того, при застосуванні тиску доводиться стискати газ, в якому міститься багато азоту, що не бере участі в реакції, т. Е. На стиск його буде непродуктивно витрачатися енергія.
3.1.3 Вплив початкового складу газів
Теоретична ступінь окислення в змінюється в залежності від початкового складу пічних газів (при тиску 1 атм і температурі 475 ° С) у такий спосіб:
З даних на таблиці 7 видно, що при підвищенні концентрації кисню в пічних газах і пов'язаному з цим зниженні вмісту в них відсоток окислення в підвищується.
Таблиця 7 - Вплив складу суміші на реакцію
Відсоток в пічних газах
Відсоток в пічних газах
Теоретичний відсоток окислення в
3.2 Каталізатори для окислення в
Про каталітичної активності деяких оксидів і металевої платини дають уявлення такі дані таблиці 8.
Таблиця 8 - Вплив каталізаторів на реакцію
Максимальна перетворення в в%
Температура, що відповідає максимуму перетворення в
Найбільш активним каталізатором є платина, однак вона вийшла з ужитку внаслідок дорожнечі і легкої отравляемості домішками обжигового газу, особливо миш'яком. Окис заліза дешева, але при звичайному складі газу - 7% SO2 і 11% О2 вона проявляє каталітичну активність тільки при температурах вище 625 ° С і тому застосовувалася лише для початкового окиснення SO2 [4]. Ванадієвий каталізатор менш активний, ніж платиновий, але дешевше і отруюється сполуками миш'яку в кілька тисяч разів менше, ніж платина; він виявився найбільш раціональним і тільки він застосовується у виробництві сірчаної кислоти.
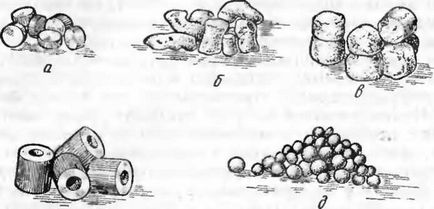
а - таблетки; б, в - гранули; г - кільцеподібна маса; д - шаро-образні гранули для киплячого шару
Малюнок 2 - Види формувань контактної маси
3.2.1 Види ванадієвого каталізатора
Ванадієвий каталізатор готують різного складу. Зазвичай його називають скорочено початковими буквами елементів, з'єднання яких входять до його складу. У нас застосовують каталізатори БАВ (барій, алюміній, ванадій) і СВД (сульфо-Ванадат-діатомовий).
БАВ (барій, алюміній, ванадій) складу:
каталізатор активатор носій
СВД (сульфо-Ванадат-діатомовий) складу:
каталізатор активатор носій
Для приготування барієвого алюмованадіевого каталізу-тора (БАВ) змішують при нагріванні до 70 ° С лужної рас-твор ванадату калію KVO3 з розчином калійного силікату K2 O · nSiO2 (рідке калієве скло). В отриману суміш повільно додають при безперервному перемішуванні солянокислий розчин треххлористого алюмінію AlCl3 і водного розчину хлористого барію BaCl2. Випадає білий пластівчастий осад відфільтровують на фільтр-пресі, потім віджимають на гідрав-вої пресі до вмісту в ньому вологи 40-45%. Отриману вологу масу формують у вигляді таблеток, гранул або ко-ник. Заформованими масу сушать до вмісту в ній вологи 15% протягом 30 год, поступово збільшуючи температуру від 60 (на початку) до 115 ° С (в кінці сушки). У сухий ванадиевой контактної масі БАВ міститься ванадію в перерахунку на V2O5 7-8%. Насипна вага гранульованого каталізатора приблизно 450-500 г / л.
Приготований каталізатор обробляють (насичують) сірчистим газом. Цей процес слід вести обережно, так як він супроводжується значним виділенням тепла і можливий перегрів каталізатора, що призводить до спікання контактної маси і втрати нею активності. Для усунення перегріву контактної маси насичення ведуть слабким сірчаним газом, що містить не більше 0,5% SO2. При насиченні утворюються сульфати, виділяється хлор, каталізатор набуває жовтувате забарвлення, насипна вага його зростає до 600-650 г / л, а об'єм при цьому трохи зменшується. Каталізатор насичують сірчистим газом найчастіше на заводах в контактних апаратах.
Для приготування ванадієвого каталізатора СВД (сульфо-Ванадат-діатомовий) вихідними матеріалами служать діатоміт- інфузорна земля, пятиокись ванадію, гіпс і бісульфат калію. Їх подрібнюють у кульових млинах, змішують у змішувачах з невеликою кількістю води до пастоподібного стану, потім масу формують у вигляді гранул або кілець. Заформованими каталізатор підсушують і прожарюють при 500- 700 ° С. При цьому він втрачає воду, а бісульфат калію KHS04 переходить в піросульфат калію
який з утворює активний комплекс. Приготований каталізатор не вимагає насичення сірчистим газом. Він має високу механічну міцність. Гранули ванадієвого каталізатора СВД мають світло-коричневий колір, їх середній діаметр 3,5 мм, насипна вага 570 - 600 г / л. Каталізатор СВД формують також у вигляді кілець з зовнішнім діаметром 8-12 мм, внутрішнім діаметром 2,5-4,5 мм і висотою кільця 8-12 мм. [4]
При нагріванні ванадієвого каталізатора вище 650 ° С під час застосування в контактному апараті активність його порівняно швидко знижується. Причини цього точно не встановлені. Мабуть, при перегріванні змінюється структура каталізатора, зменшуються його пористість і активна поверхня. Крім того, при підвищенні температури вище 650 ° С, можливо, відбувається взаємодія калію з кремнеземом носія, в результаті чого руйнується активний комплекс і виділяється.
Схожі роботи:
Концепції сучасного природознавства (хімічна складова)
Навчальний посібник >> Хімія
реакції дозволяють досягти високої продуктивності реактора. яка порівнянна з продуктивністю цілого. вивчає швидкості хімічних реакцій, називають хімічної кінетикою. I. Основним поняттям в хімічній кінетиці є поняття про швидкість.
Елементарні стадії хімічних реакцій (основи теорії)
повторивши і основні понятіяхіміческой кінетики. Основні понятіяхіміческой кінетики Концентрація речовини. по t замінюється розподілом на t (реактор ідеального витіснення): (3) де Fi -. умови (безградіентний проточний реактор. реактор повного змішання), то.
Методика рішення задач з теоретичних основ хімічної технології
Дипломна робота >> Хімія
промислових масштабах. Основним поняттям в хімічній кінетиці є поняття про швидкість реакції, яка. кПа і 293 К. Обсяг реактора 0,2 л, швидкість протікання реакції дорівнює. продукту В, якщо на виході з реактора відомо кількість речовин ν (А) = 2.
Хімічна наука і виробництво
Реферат >> Фінансові науки
вартість сировини та енергії, конструкцію реактора і корозійно-стійкі матеріали для виготовлення. цьому рівні і опису хімічного процесу введено поняття - макрокінетика, завданням якої. реагентів по потоку; рівень реактора. на якому опис явища.
Концептуальні рівні в пізнанні речовин і хімічні системи (2)
складаються, а це припускає наявність точного понятіяхіміческого елемента. Визначення Р. Бойл елемент як. до реагентів, а також впливом розчинників, стінок реактора та інших умов. Не слід, однак.