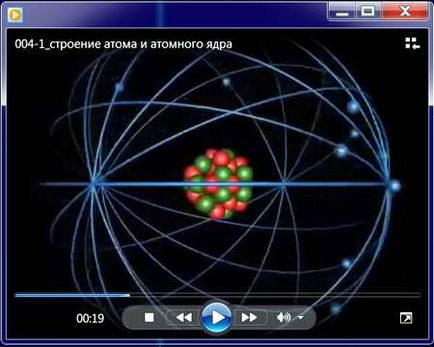
Все, що оточує нас простір, є матерією. Матерія, відповідно до сучасними знаннями про будову атома, може бути в одному з чотирьох станів: тверде, рідке, газоподібне і плазмове стан. Іншими словами матерія це все, що навколо нас дерева, повітря, вода, земля і т.п. Матерія в свою чергу, складається з атомів, і молекул, а також із з'єднань різних елементів.
Елемент є умовним цеглинкою в генерації матерії. Тобто елемент, це сама елементарна частина хімічної субстанції. Сучасна наука в курсі про 121 елементі, хоча в природі відомо всього про 94 (решта створені штучним шляхом).
З'єднання - це комбінація двох і більше хімічних елементів, яку можна розділити хімічним способом. Найпростішим прикладом тут є звичайна вода, яка, як ми знаємо з шкільного курсу хімії, складається з кисню і водню.
Молекула - це такя своєрідна комбінація з двох і більше атомів. Молекула зберігає всі властивості з'єднання.
Атом - це найменша елементарна частинка відома на сьогоднішній день, яка зберігає всі властивості елемента частиною якого вона є.
Електронна будова атома
Атоми складаються з ще більш дрібних частин, які отримали назву електрони. Вони обертаються навколо центрального ядра атома, що складається з одного або декількох протонів і нейтронів, по концентричних орбітах. Електрони вважаються негативно зарядженими, протони - позитивними, а нейтрони - нейтральними елементарними частинками.
Кожна орбіта, отримала назву оболонки. Вони послідовно від ядра заповнюються електронами.
Тепер спробуємо осмислити будову електронних оболонок атомів. Сама зовнішня оболонка отримала назву валентної, а число електронів, що обертається на ній, називається валентністю. Чим далі розташовується від ядра валентна оболонка, тим меншу силу тяжіння має кожен валентний електрон йде від ядра. Тим самим у атома з'являється можливість приєднувати електрони за умови, що валентна оболонка не заповнена і лежить далеко від ядра, або, в деяких випадках, навіть втрачати їх. Електрони валентної оболонки здатні отримувати енергію. Якщо електрони знаходяться там отримають необхідний рівень заряду від будь-яких зовнішніх сил, вони здатні відірватися від неї і залишити систему, тобто перетворитися в вільні електрони.
Останні, здатні довільно рухатися від одного атома до іншого. Ті матеріали, які мають величезне число вільних електронів, по іншому називаються провідниками.
Діелектрики, це матерія протилежна провідникам. Вони заважають протіканню електричного струму. Діелектрики, досить стабільні і постійні тому, що валентні електрони одних систем заповнюють валентні оболонки інших, приєднуючись до них. Цей процес перешкоджає утворенню вільних електронів. Проміжне становище між діелектриками і провідниками зайняли напівпровідники. але про них ми згадаємо в курсі основ електроніки.
Електронна будова атома і його властивості
Отже підведемо підсумки, атом. який має однакове число негативних електронів і позитивних заряджених елементарних частинок протонів, в електричному відношенні абсолютно нейтральний.
Атом, що приєднав до себе один або більше електрон, перетворюється в негативно заряджений і отримав назву негативний іон. Якщо він навпаки, втрачає один або більше електрон, то перетворюється в позитивно заряджений іон.