ХІНОЛІНОВИЕАЛКАЛОІДИ. містять в молекулі залишок хіноліну або деяких його похідних. Включають понад 300 представників. Виділено з рослин 14 родин, а також деяких мікроорганізмів і тварин. Наїб. багаті ними рослини сімейства рутових (Rutaceae), маренових (Rubiaceae), парнолістнікових (Zygophyliaceae) і складноцвітих (Compositae).
Розрізняють слід. основні групи хіноліновий алкалоїдів: 1) прості хіноліни (загальна ф-ла I; R = Н, ОСН3. R '= алкіл, арил), 4-хінолони (II; R = Н, СН3. R' = Н, алкіл, арил ) і 2-хінолони (III; R = Н, СН3. R '= Н, алкіл, алкеніл); 2) гемітерпеноідние і терпеноідние тріцікліч. похідні типів IV-Х; З) фуранохіноліни, до яких відносяться, зокрема, похідні діктамніна (XI; R = ОСН3) і сполуки. типу ХII; 4) димерні алкалоїди, напр. ХIII. До хіноліновий алкалоїдів іноді відносять також сполуки. містять крім хіноліну залишки хінуклідину (зокрема, хінін), -карболіна (як в XIV) та ін .; однак частіше їх виділяють в окремий клас алкалоїдів, специфічний для рослин певних пологів, напр. хінного дерева (Cinchona), селітрянки (Nitraria).
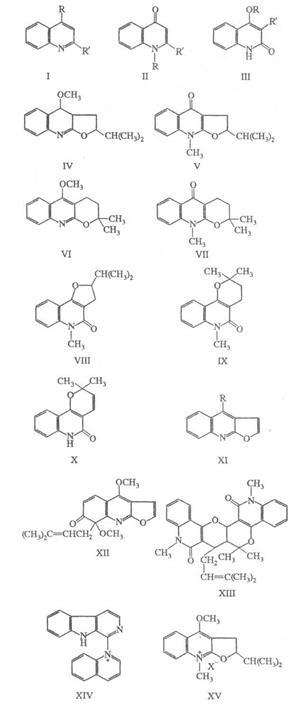
Кожній групі алкалоїдів притаманні характерні хім. і спектральні св-ва. Загальні св-ва Л. а. містять в положеннях 2 або 4 метоксігруппи: а) здатність изомеризоваться при нагр. з СН3 I в N-метил-2 (або 4) -хінолони (напр. IV изомеризуется в V, VI - в VII); б) легкість гідролізу (дементірованія) в лужному або кислому середовищі, напр. XI (R = OCH3) XI (R = OH). Природні і синтетичні. четвертинні хінолінова алкалоїди пріпіролізе або нагріванні з безводним пиридином перетворюються в відповідні третинні підстави, напр. з'єднання XV в IV.
2-Хінолони, напр. 4-метокси-3-дебати-2-хінолон [III; R = CH3. R '= СН2 СН = С (СН3) 2] при нагр. з конц. НС1 або НВr в крижаній СН3 СООН утворює трициклічні хінолінова алкалоїди типу VII і IX.
Характерна р-ція фуранохінолінових алкалоїдів (XI) -гідрогеноліз фуранового кільця з утворенням З-етил-2-хінолонових похідних (III; R = СН3. R '= С2 Н5).
Для дослідження структури хіноліновий алкалоїдів використовують спектральні методи. За значенням максимумів поглинання в ЙК і УФ спектрах і характером їх зміщення в залежності від рН середовища розрізняють не тільки групи хіноліновий алкалоїдів, а й іноді положення заступників. Mace-спектрометрія дозволяє встановити приналежність алкалоїду до певної групи і розрізняти такі близькі ізомери, як V і VII; VIII і IX. Відповідно до положення і інтегральної інтенсивності смуги поглинання в області 1610-1665 см -1 ІК спектру можна розрізнити 2 і 4-хінолони, а також ізомерні сполуки V і VIII, VII і IX. У більшості випадків про повну структурі хіноліновий алкалоїдів можна судити за даними спектрів ЯМР 1 Н і 13 С.
Різні хінолінова алкалоїди мають різних біогенетіч. попередників. Так біосинтез хініну і похідних кінуреновой к-ти (I; R = ОН, R '= СООН) здійснюється з триптофану, а хіноліновий алкалоїдів сімейства рутових (соед. I-ХIII, XV) - з антраниловой кислоти.
Хінолінові алкалоїди володіють широким спектром физиологич. активності. Більшість алкалоїдів надає заспокійливу дію на центр. нервову систему: нек-риє з них, напр. фліндерсін (X), проявляють антіфідантние св-ва. В медицині застосовується хінін і ехінопсин (II; R = CH3. R '= Н) як стимулятор центр. і периферич. нервової системи.
Хінін (C20 H24 N2 O2) - основний алкалоїд кори хінного дерева з сильним гірким смаком, що володіє жарознижуючим і знеболювальні властивості, а також вираженим дією проти малярійних плазмодіїв. Це дозволило протягом тривалого часу використовувати хінін як основний засіб лікування малярії. Сьогодні з цією метою застосовують більш ефективні синтетичні препарати, але з певних причин хінін знаходить своє застосування і в даний час.
Хінін є алкалоїдом, що містяться в корі різних видів хінного дерева. У цій корі крім хініну міститься хінідин, цінхонін, цінхонідін і ряд інших алкалоїдів. До складу молекули хініну входять хіноліновий і хінуклідіновие цикли, пов'язані групою атомів - СН - ОН. Хінін є ізомером хінідину. У медичній практиці застосовуються гідрохлорид, дигидрохлорид і сульфат хініну. Підстава хінінарастворяется в етиловому спирті (1: 1), хлороформі (1. 3), діетиловому ефірі, насиченому водою (1: 4), слабо розчиняється у воді. Гідрохлорид хініну розчиняється в етиловому спирті (1: 1), хлороформі (1: 2), воді (1. 23), слабо розчиняється в діетиловому ефірі. Сульфат хінінарастворяется в етиловому спирті (1: 95), слабо розчиняється у воді (1 810), діетиловому ефірі і хлороформі.
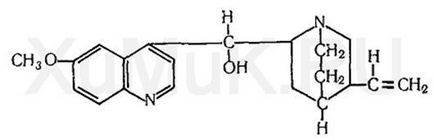
Хінін екстрагується органічними розчинниками з лужних водних розчинів. Максимальні кількості хініну екстрагіруютсяхлороформом при рН = 9. 10.
Застосування. Дія на організм. Залежно від прийнятої дози хініну він може викликати пригнічення центральної нервової системи, головний біль, запаморочення, порушення зору. Хінін збуджує мускулатуру матки і підсилює її скорочення. Він так само викликає скорочення селезінки. Хінін діє на збудника малярії і є одним з ефективних протималярійних лікарських препаратів. Його застосовують при аритміях. Хінін застосовується в акушерській практиці для збудження і посилення пологової діяльності. При передозіровкехініна, що застосовується вагітними жінками, може наступити аборт.
Метаболізм. В організмі хінін піддається метаболізму шляхом окислення хінолінова і хінуклідіновие циклів. При цьому утворюються 2-оксіхінін, 2'-оксіхінін, діоксіхінін. При метаболізмі може окислюватися вінільні група в молекулі хініну з утворенням хінетіна. Також може окислюватися хінуклідіновие цикл з утворенням гемохінной кислоти (6-метокси-хінолін-4-кетокарбоновой кислоти). Метаболіти і незначна частина незв'язаного хініну виводиться з організму з сечею.
Попередня проба на наявність хініну в сечі. У ділильну воронку вносять 2 мл сечі, яку подщелачивают розчином аміаку, а потім додають 4 мл хлороформу і збовтують протягом 5 хв. Від водної фази відділяють шар органічного розчинника, який збовтують з 3 мл 10% -го розчину сірчаної кислоти. Синя флуоресценція водної фази вказує на наявність хініну в сечі. Флуоресценція стає більш вираженою, якщо кислу водну витяжку опромінювати УФ-світлом.
Виявлення хініну по флуоресценції. Розчини хініну, підкислені сірчаною кислотою, мають блакитну флуоресценцію. При наявності іоновхлора і деяких інших іонів в розчинах флуоресценція хініну послаблюється.
Флуоресценція хініну як двухосновного підстави залежить від рН середовища. У кислому середовищі хінін має блакитну флуоресценцію. У лужному середовищі (рН
9) хінін має фіолетову флуоресценцію. Продукти окислення хініну мають жовто-зелену флуоресценцію.
Виконання досвіду. Досліджуваний розчин вносять у фарфорову чашку і випарюють насухо. До сухого залишку додають 4-5 мл 0,1 н. растворасерной кислоти. Отриманий розчин переносять в пробірку, яку опромінюють УФ-променями. При наявності хініну з'являється блакитна флуоресценціяраствора. Від додавання до цієї рідини декількох крапель 0,1 н. розчину гідроксиду натрію інтенсивність блакитний флуоресценції слабшає, а потім (при рН
9) з'являється фіолетова флуоресценція.
Якщо до розчину хініну, підкисленою сірчаною кислотою, додати кілька крапель бромної води, розведеної десятикратним об'ємом води (до повного гасіння флуоресценції), а потім додати кілька крапель 25% -го розчину аміаку до лужної реакції, то з'являється жовто-зелена флуоресценція.
Талейохінная реакція. Від додавання до хініну бромної води, а потім аміаку утворюється зеленого кольору талейохін, який екстрагіруетсяхлороформом:
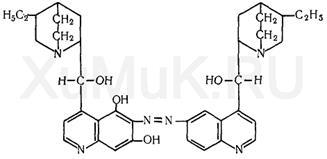
Виконання реакції. Розчин досліджуваної речовини випарюють насухо. До сухого залишку додають 1 мл води. До отриманого розчину по краплях додають бромную воду (уникаючи її надлишку) до слабо-жовтого забарвлення. Від додавання кількох крапель розчину аміаку до слабо-жовтого розчину з'являється яскраво-зелене забарвлення, яка при нейтральній реакції стає синьою, а при додаванні кислоти переходить в червону або фіолетову. При збовтуванні рідини, що має зелене забарвлення, з хлороформом останній набуває зелене забарвлення.
На відтворюваність реакції впливає концентрація досліджуваної речовини, обсяги додаються реактивів і т. Д. Реакції мешаютамідопірін, антипірин, кофеїн і ін.
Ерітрохінная реакція. Кілька крапель досліджуваного розчину випарюють насухо, додають 1 мл води, слабо підкисленою сірчаною іліуксусной кислотою, краплю бромної води і краплю 10% -го розчину гексаціаноферрата (III) калію. Отриману рідину добре збовтують, потім по краплях додають аміак до лужної реакції. При наявності хініну в досліджуваному розчині з'являється рожева або червоно-фіолетове забарвлення, яка при збовтуванні з хлороформом переходить в хлороформний шар.
Виявлення хініну методом хроматографії. Для виявлення хініну застосовують метод хроматографії в тонкому шарі силікагелю. З цією метою використовується та ж методика, що і для виявлення морфіну (див. Гл. V, § 34).
Плями хініну на хроматограмі мають рожево-бурого забарвлення (Rf = 0,39 ± 0,01).