За допомогою рівняння стану можна знайти залежність тиску газу від температури при постійному обсязі. Цю залежність експериментально встановив французький фізик Ж. Шарль (1746-1823) в 1787 р * Маючи рівнянням стану ідеального газу, вдаватися до досвіду вже немає необхідності.
закон Шарля
Відповідно до рівняння (3.9.9)
Тиск даної маси газу при постійному обсязі прямо пропорційно абсолютній температурі. В цьому і полягає закон Шарля.
Із закону Шарля слід, що ставлення тисків даної маси газу при постійному обсязі дорівнює відношенню його абсолютних температур:
Процес зміни тиску газу, викликаний зміною температури при постійному обсязі, називають ізохорним (від грецьких слів isos - рівний і chora - займане місце). Залежність тиску газу від температури графічно зображується прямою лінією - Ізохор. Різним обсягами відповідають різні ізохорами (рис. 3.14). Так як з ростом обсягу газу при постійній температурі тиск його падає (закон Бойля-Маріотта), то ізохора, що відповідає обсягу V2, лежить нижче ізохорами, що відповідає обсягу V1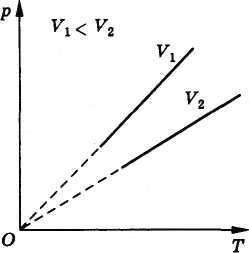
Всі прямі закінчуються на початку координат. Значить, тиск ідеального газу при абсолютному нулі дорівнює нулю, так само як і обсяг.
Пропонуємо читачеві самостійно переконатися в тому, що закон Шарля можна записати у формі
де р0 - тиск газу при температурі Т = 273 К, а коефіцієнт γ, званий температурним коефіцієнтом тиску газу, дорівнює температурному коефіцієнту об'ємного розширення:
Коефіцієнт γ є відносна зміна тиску при зміні температури газу на 1 К.
Газовий термометр постійного об'єму
У § 3.6 говорилося про ідеальну газової шкалою температур. Для визначення температури по цій шкалі використовують газові термометри. Найбільш простим газовим термометром є термометр постійного об'єму. Вимірювання температури за допомогою цього термометра засноване на законі Шарля (3.10.2).
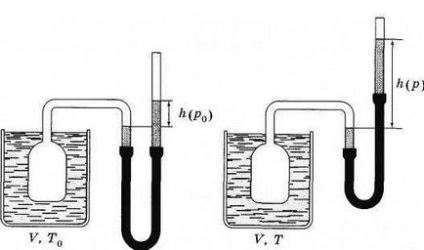
Газовий термометр представляє собою посудину, заповнений тим чи іншим газом: азотом, аргоном або гелієм. Посудина з'єднаний гнучкою трубкою з ртутним манометром, яким вимірюють тиск газу і підтримують його постійний обсяг (рис. 3.15, а, б). Спочатку вимірюють тиск при деякій фіксованій температурі Т0 (див. Рис. 3.15, а) *. Потім вимірюють тиск при температурі Т (див. Рис. 3.15, б). Знаючи тиск р0 при температурі Раз тиск р при температурі Т, температуру Т визначають за формулою
* В якості цієї температури зазвичай вибирається температура потрійної точки води, т. Е. Температура стану, в якому лід, вода і водяна пара знаходяться в тепловій рівновазі.
Газовий термометр для точних вимірювань - дуже складний пристрій. Для вимірювання температури при фізичних дослідженнях він застосовується рідко. Основне його призначення - використання для градуювання простіших, вторинних термометрів. Ця градуювання проводиться в бюро стандартів, в метрологічних інститутах і в окремих фізичних лабораторіях. Для градуювання звичайних, широко застосовуваних термометрів використовуються вторинні термометри.
На законі Шарля заснований пристрій газового термометра для визначення температури по ідеальній газової шкалою.