Проблема лікування важких нозокоміальних інфекцій
резистентність флори
Резистентність збудників нозокоміальних інфекцій до антибіотиків (АБ) є важливою причиною, що впливає на летальність і споживання ресурсів [1]. Швидке зростання і поширення резистентності до АБ госпітальної флори спостерігається в усьому світі, але цей процес відбувається нерівномірно. Грам і грампозитивнімікроорганізми є основними збудниками нозокоміальних інфекцій [2-5]. Найбільш проблемними мікроорганізмами є резистентні до метициліну S.aureus (MRSA) і грамнегативні бактерії - продуценти β-лактамаз розширеного спектру (ESBLs), так як саме вони мають резистентність до багатьох АБ [6-11].
Відділення реанімації та інтенсивної терапії (ВРІТ) виявляються найбільш актуальними відділеннями з точки зору появи резистентності флори до АБ. Це обумовлено декількома причинами: 1) високою частотою неефективною стартової терапії і тривалим застосуванням АБ широкого спектру дії; 2) концентрацією найбільш важких хворих в приміщеннях з відносно невеликою площею; 3) невисокою економічною зацікавленістю середнього медичного персоналу в навчанні і застосуванні на практиці методів обмеження контактного поширення резистентної флори; 4) збільшенням кількості госпіталізованих пацієнтів з гострою та хронічною патологією, які потребують тривалого лікування та є джерелом бактерій, резистентних до АБ [1, 12-13].
Подолання резистентності до АБ
Ідеальна антибактеріальна терапія повинна забезпечувати адекватну (активну щодо виділеного збудника) стартову терапію і обмежувати зростання та поширення резистентності. Порівняно недавно основні ідеї такої програми були представлені у вигляді 12 принципів профілактики резистентності в стаціонарі. Одним з ключових елементів цієї програми є участь у вирішенні цієї проблеми експертів в даній області (інфекціоністів, клінічних епідеміологів, мікробіологів, клінічних фармакологів), особливо при розробці методів оптимізації лікування і обмеження резистентності до АБ.
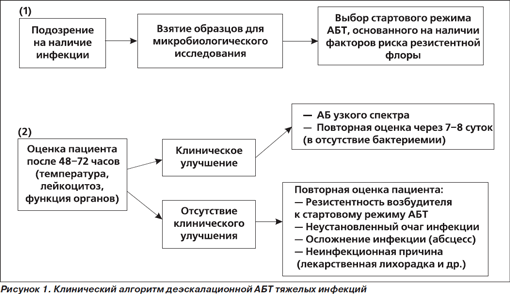
1. Підозра на наявність важкої нозокоміальної інфекції.
2. Оцінка стартового режиму АБТ після отримання мікробіологічних даних.
3. Завершення курсу АБТ - продовження моніторингу.
Резистентність до АБ: фактори ризику та їх вплив на результат
Фактори ризику появи резистентності до АБ
АБ стимулюють появу резистентності, тому заходи, спрямовані на обмеження їх застосування, безпосередньо пов'язані з обмеженням резистентності. У багатьох дослідженнях виявлено тісний зв'язок між застосуванням АБ і появою резистентності бактерій до нього [15-17]. Є інші чинники ризику зростання резистентності до АБ: тривала госпіталізація; застосування інвазивних пристроїв (інтубаційні трубки, судинні катетери), ймовірно, в результаті утворення біоплівки на поверхні цих пристроїв; проживання в будинках інвалідів і людей похилого віку; неефективні заходи інфекційного контролю [13].
Поява нових штамів збудників в позалікарняних умовах призводить до потрапляння цієї резистентної флори в стаціонар. Порівняно недавно доведено поява і поширення позалікарняних штамів S.aureus, резистентних до оксациліну (CA-MRSA) [17-20]. Тривале застосування АБ є найбільш важливим фактором появи резистентності до нього, причому цей вплив може бути істотно ослаблене раціональної АБТ [21-22].
Наслідки неадекватною АБТ
Підвищення летальності. Показано, що емпірична АБТ важких інфекцій препаратами, неактивними відносно збудників, тобто неадекватна стартова АБТ, призводить до достовірного підвищення летальності - приблизно в 2 рази. Нещодавно подібні дані були отримані у хворих сепсисом [23-31]. Зміна режиму АБТ жизнеугрожающих інфекцій після отримання даних мікробіологічного дослідження істотно не покращувало результати лікування через виникнення важких ускладнень: септичного шоку, кровотеч та інших причин [24, 26]. У цих дослідженнях показано, що зростання резистентності госпітальної флори приводив до збільшення летальності через низьку ефективність стандартних режимів емпіричної АБТ. Нещодавно в рекомендаціях Американського торакального суспільства і Товариства інфекціоністів (ATS / IDSA) по лікуванню нозокоміальноїпневмонії була підкреслена важливість неадекватною АБТ як причини зростання госпітальної летальності [32]. Ці рекомендації підкреслюють важливість: 1) моніторингу чутливості до АБ локальної флори (постійного оновлення даних для всієї лікарні та окремих ОРИТ для забезпечення адекватності вибору емпіричних режимів АБТ); 2) правильного дозування АБ (для оптимізації тканинних концентрацій).
Зростання витрат. В основному зростання витрат пов'язаний з нозокоміальної інфекції, які зазвичай бувають викликані флорою, резистентної до АБ [17, 33]. Встановлено, що інфекції, викликані MRSA, в порівнянні з інфекціями, викликаними чутливими до метициліну / оксациліну S.aureus (MSSA), є причиною більш високої летальності. У метааналізу 30 досліджень було показано, що MRSA-бактериемия незалежно від інших причин підвищує ризик смерті [34]. При оцінці атрибутивної летальності MRSA і MSSA різниця склала близько 25% [35]. Причинами цих відмінностей, як вважають, є: 1) тяжкість перебігу інфекції; 2) застосування неадекватної емпіричної АБТ. Зазвичай у пацієнтів з інфекціями, викликаними MRSA, зазначалося більш важкий перебіг захворювання і в момент надходження в стаціонар, і в момент діагностики інфекції. Крім того, хворі потребували більш тривалої госпіталізації.
Фактори, що впливають на вибір стартовою АБТ
Адекватний режим АБТ. При визначенні режиму емпіричної АБТ необхідно враховувати 4 найважливіші чинники: 1) наявність інфекції (встановлений або підозрюваний діагноз інфекційного захворювання); 2) ймовірність етіологічної значущості тих чи інших збудників при певних видах нозокоміальних інфекцій (етіологічна структура нозокоміальних інфекцій); 3) спектр циркулюючих мікробів в даній установі та особливості їх резистентності до антибіотиків (моніторинг локальної флори); 4) наявність у пацієнта факторів ризику інфекції, викликаної резистентної флорою. В ідеальному випадку повинні враховуватися всі зазначені вище фактори.
Наявність інфекції. Багато критичні стани супроводжуються генералізованої запальної реакцією, клінічні і лабораторні ознаки якої істотно не відрізняються від ознак інфекції. У випадках госпіталізації пацієнтів у ВРІТ з неінфекційними захворюваннями поява ознак інфекції (первинний осередок, ознаки генералізованої інфекції, підвищений рівень цитокінів, білків гострої фази, прокальцитоніну), як правило, не викликає діагностичних труднощів. Однак при тяжкій політравмі, опікової токсемії, деструктивному панкреатиті, післяопераційних хірургічних інфекційних ускладненнях, поліорганної недостатності виникає генералізований запалення, яке нерідко створює значні диференційно-діагностичні труднощі у виключенні нозокоміальноїінфекції і призводить до істотного розширення застосування антибактеріальних препаратів, в тому числі широкого спектра.
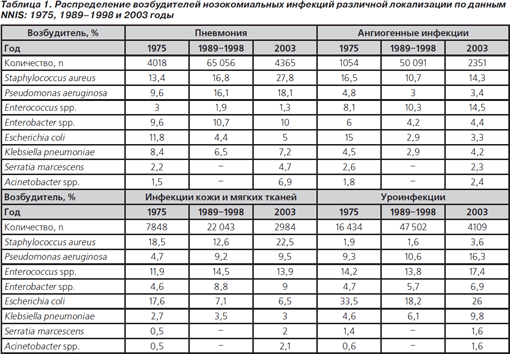
Збільшення кількості і резистентності грамнегативних неферментуючих бактерій. Однією з найбільш важливих тенденцій є зростання актуальності Acinetobacter spp. у хворих з уроінфекціі, пневмонією та раневими хірургічними інфекціями [39-41]. Незважаючи на низький відносний внесок ацінетобактер (
Моніторинг локальної флори і резистентності до АБ
Вплив інших факторів, в тому числі ШВЛ. Поширеність полірезистентною флори суттєво різниться в залежності від патології пацієнтів, типу лікарень і відділень. Полірезистентні збудники найбільш часто виділяються від важких пацієнтів, пацієнтів з хронічними захворюваннями, наприклад з наявністю факторів ризику пневмонії, пов'язаної з наданням медичної допомоги (табл. 2) і пацієнтів з пізньою нозокомиальной пневмонією. Фактори ризику Нпівл, викликаної полірезистентною флорою, були вивчені у 135 пацієнтів, що знаходилися на ШВЛ [17]. Тривалість ШВЛ до початку пневмонії і попереднє призначення АБ (протягом 15 днів, що передують Нпівл) були достовірними факторами ризику Нпівл, викликаної резистентної флорою. Пізня Нпівл (що виникла після 5 діб інтубації трахеї) у пацієнтів, які отримували до цього АБ, викликалася зазвичай полірезистентною флорою: P.aeruginosa. Acinetobacter baumannii, Stenotrophomonas maltophilia. MRSA. Ці дані ще раз вказують на необхідність раціонального застосування АБ у пацієнтів, яким проводиться ШВЛ, і обліку попередньої антибактеріальної терапії як основного фактора ризику Нпівл, викликаних полірезистентною флорою. Цим же визначається необхідність вибору в режимі емпіричної терапії Нпівл (до отримання результатів мікробіологічного дослідження) препаратів широкого спектра дії, здатних долати основні відомі механізми резистентності нозокоміальної флори для підвищення адекватності емпіричного режиму АБТ.

Відмінності госпітальної флори в різних ОРИТ однієї лікарні
Проведено дослідження, присвячене вивченню різних полірезистентних збудників інфекцій в різних ОРИТ однієї лікарні [44]. Виявлено суттєві відмінності в чутливості збудників в хірургічному, травматологічному і загальному ОРИТ. Виявлена низька чутливість Acinetobacter spp. до іміпенем в хірургічному та висока чутливість в травматологічному ОРИТ. Подібні спостереження були зроблені в ОРИТ інших країн [45, 46]. Ці дані підтверджують необхідність узгодження загальних рекомендацій по антимікробної терапії і локальних даних про чутливість (в країні, місті, лікарні і ОРИТ). Це допомагає враховувати особливості грамнегативної флори, наприклад частоту виділення продуцентів β-лактамаз розширеного спектру серед K.pneumoniae або E.coli; резистентних до фторхінолонів P.aeruginosa. резистентних до карбапенемам A.baumannii. При високу ймовірність інфекцій, викликаних цими збудниками, необхідно вносити корективи в режими емпіричної терапії.
Особливості пацієнтів, здатні впливати на резистентність флори до АБ
На додаток до місцевих або регіонарним особливостям флори є багато особливостей пацієнтів, які підвищують ймовірність виділення резистентної флори. Тому вибір емпіричної терапії повинен бути заснований на даних моніторингу локальної флори з урахуванням особливостей пацієнтів. При наявності факторів ризику інфекцій, викликаних госпітальними штамами S.aureus. P.aeruginosa. Acinetobacter spp. через високу ймовірність резистентності істотно зростає летальність [47-51]. Інфекції, викликані резистентної флорою, зазвичай виникають у госпіталізованих пацієнтів з тривалим лікуванням в стаціонарі, тривалої катетеризації судин, застосуванням антибіотиків, при наявності пролежнів, рани хірургічної інфекції, зондовом харчуванні та проведенні гемодіалізу.
Поширеність нозокомиальной флори в стаціонарі
Деякі види медичної допомоги, наприклад гемодіаліз, хіміотерапія, хірургічні стаціонари одного дня, призводять до збільшення кількості пацієнтів, які отримують лікування в умовах стаціонару [52]. Пневмонія і ангіогенние інфекції, пов'язані з наданням медичної допомоги, часто класифікуються як позалікарняних інфекції і спочатку лікуються із застосуванням відповідних рекомендацій. Однак часте спілкування між пацієнтами і медичними працівниками, які працюють в стаціонарах, призводить до того, що колонізують флора таких пацієнтів починає відрізнятися від негоспітальної і стає більш схожою на нозокоміальну. Наприклад, MRSA, виділені від пацієнтів, інфікованих в умовах стаціонару, різко відрізняються від позалікарняних і володіють різною чутливістю до АБ [19].
Крім того, за останнє десятиліття відбувається суттєва зміна в резистентності позалікарняної флори. Streptococcus pneumoniae залишається основним збудником пневмонії, однак ця інфекція викликається і іншими збудниками (Chlamydia pneumoniae. Mycoplasma pneumoniae. Acinetobacter spp. MRSA, Legionella spp.), Поширеність яких істотно відрізняється в різних регіонах і продовжує змінюватися [42, 53, 63, 81 ]. Поширення резистентності до АБ збудників позалікарняних інфекцій істотно ускладнює їх лікування, вимагає внесення змін відповідно до мікробіологічними та епідеміологічними даними [54]. Все це призводить до необхідності відокремити інфекції, пов'язані з наданням медичної допомоги, від інфекцій, які традиційно відносили до позалікарняних [17, 32, 55, 56].
висновок
Зростання резистентності до АБ є найважливішою проблемою на шляху ефективного клінічного застосування АБ. Складність збереження рівноваги між необхідністю проведення адекватної АБТ і обмеженням зростання резистентності флори диктують необхідність пошуку нових підходів до стратегії застосування АБ. Незважаючи на те що нові АБ розширюють можливості лікування, їх створення може не встигати за зростанням резистентності флори. Якщо щодо актуальних грампозитивних збудників в даний час є препарати, здатні вирішувати всі проблеми резистентності, щодо актуальних грамнегативнихбактерій таких препаратів немає. Це ще раз підкреслює важливість стратегічного мислення при застосуванні АБ в клінічних умовах, здатного привести до дотримання балансу між ефективністю їх застосування і обмеженням зростання резистентності збудників.