Окис кальцію при взаємодії з водою гаситься, утворюючи пушонку - гідроокис кальцію:
При цьому відбувається значне збільшення обсягу - в 2-3 рази. Процес гідратації вапна прискорюється в 1,5-2 рази при гасінні слабким розчином (1-5% -ним) NaCl, СаСЬ або інших електролітів 86.
Швидкість гасіння вапна залежить від її складу і темпера-тури випалу і може коливатися в межах від декількох хвилин до декількох годин. Сильно обпалене вапно (при 1200 ° і ви-ше) гідратіруется медленно87'88. Дисперсність вапна також зменшується, якщо для отримання її застосовується вапно, обожнюючи-женная при дуже високій температурі.
Зазвичай при гасінні активної, швидко гасячи вапна тре-буется відводити тепло реакції. При повільному гасінні слід проводити процес без відводу тепла щоб уникнути уповільнення гідратації. Для отримання тонкодисперсної вапна необхідний попередній підігрів води, яка застосовується для гасіння.
Апарат для гасіння вапна представлений на рис. 43581. Іно-гда апарат постачають сорочкою для підтримки необхідної тим-ператури і просушування шару гашеного вапна, що пристала до стінок апарату. Всередину сітчастого барабана подають воду, нагріту до 85-95 °. Вапно гаситься і розсипається в дрібний порошок, просеі-
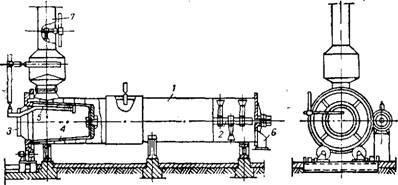
Мал. 435. Апарат для гасіння вапна:
1 -Барабан: 2 - вал з лопатями; 3 -загрузочная воронка; 4 - сітчастий барабан;
5 труба для підведення води; 5 -вигрузочное отвір; 7 труба для відводу водяного
Вающий при обертанні сітчастого барабана через його стінки; вона потрапляє в зовнішній барабан, пересувається до його кінця Лопа-ня обертового вала і вивантажується. Воду дозують так, щоб пушонка на виході з апарату містила 0,5-2% вологи. Гасіння при нестачі води протікає при більш високій тим-пературі і призводить до ускладнення процесу. Підвищений содер-жание вологи в Пушинка (більше 2%) ускладнює її транспорти-ження. Запропоновано прискорювати гасіння шляхом розпушення вапна продуванием неї пара 89.
Для звільнення від шматочків «недопалу» і «перепала» пу-шонку пропускають через обертається сито-БУРАТ. Це сито являє собою сітку з 64 отворами на 1см2, натягнуту на дерев'яну раму. Воно має форму восьмигранної усіченої пі-раміди, розташованої горизонтально і обертається навколо своєї осі. Просіяну пушонка вилежується в бункерах не мен-неї 3 днів. За цей термін гасіння повністю завершується, увели-чивается дисперсність частинок, температура і вологість пушонкц зменшуються, вона набуває однорідний склад і може під-вергнута хлоруванню.
Після вилежування в бункерах пушонка повинна містити не менше 86% Са (ОН) 2, не більше 7% СаСОз, 0,6-1% вільної вологи і менше 6% домішок (Si02, R203, MgO та ін.) При відсутність про-наслідком непогашеної окису кальцію. Зазвичай вона містить 90-92% Са (ОН) 2, 2-4% СаСОз, 0,5-0,9% вологи і до 5,5% інших примі-сей90. її щільність
2,08 г / см3, а об'ємна вага коливається від 0,4 до 1 г / см3 (зазвичай 0,55-0,65).
Хлорування вапна Теорія процесу
Абсолютно сухі гідроокис кальцію і хлор не вступають в реакцію; хлор тільки адсорбується вапном. У виробничих-них умовах хлоруванню піддають пушонку, що містить менше 1% вільної вологи; застосовується для цієї мети раз-додану повітрям хлор також містить невелику кількість вологи. Навіть невелика вологість вихідних речовин забезпечує початок реакції гідролізу хлору з нейтралізацією утворюються кислот вапном. Потім гідроліз триває за рахунок води, ви-ділячи при хлоруванні з гідроксиду кальцію, і все но-ші кількості вапна вступають в процес; утворюється ряд соеди-нений, з яких і складається хлорне вапно (стр. 1431).
У перший період хлорування вапна, мабуть, обра-зуется суміш двуосновних гіпохлориту кальцію і СаС12 • Са (ОН) 2 • Н20 по реакції:
5Са (ОН) 2 + 2С12 = Са (СЮ), • 2Са (ОН) 2 + СаС12 • Са (ОН) 2 • Н20 + Н20
- Звільняється при цьому гідроокис кальцію переходить в рідку фазу і витрачається на взаємодію з хлором: 2Са (ОН) г + 2С1г = Ca (C10) 2 + СаС12 + 2H20
Але так як ця реакція протікає в розчині, насиченому через звісткою, гіпохлоритом і хлоридом, то знову утворюються Са (С10) 2 і СаС12 виділяються в тверду фазу у вигляді основних со-лей СаС12-Са (0Н) 2-Н20 і ЗСА (СЮ) 2-2Са (0Н) 2-2Н20.
Перехід двуосновних гіпохлориту в дветретносновной опору-вождается зменшенням кількості рідкої фази, так як вода входить до складу твердого кристаллогидрата. На цій стадії хло-рірованія виходить вельми сухий, розсипчастий продукт.