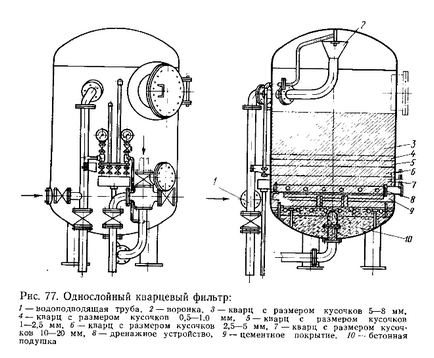
Назва роботи: Методи нейтралізації (вапнування)
Предметна область: Хімія та фармакологія
Опис: Пом'якшення води - це процес видалення з води солей жорсткості. Процеси вилучення з води солей Ca2 + і Mg2 + в водопідготовки називають пом'якшення води. Щодо видалення солей жорсткості з води може проводитися трьома методами: реагентної.
Розмір файлу: 309.98 KB
Роботу скачали: 24 чол.
Пом'якшення води - це процес видалення з води солей жорсткості.
Процеси вилучення з води солей Ca 2+ і Mg 2+ в водопідготовки називають пом'якшення води. Щодо видалення солей жорсткості з води може проводитися трьома методами:
- реагентним пом'якшення води;
- іонним обміном;
- Нанофільтрація.
Жорстка питна вода гіркувата на смак і чинить негативний вплив на органи травлення. За нормами оптимальна жорсткість питної води становить 1,0 # 150; 2,0 мг-екв / л. У побутових умовах надлишок солей жорсткості призводить до заростання поверхонь, що нагріваються в бойлерах, чайниках, трубах, відкладенню солей на сантех арматури і виведення її з ладу, а також залишає наліт на волоссі і шкірі людини, створюючи неприємне відчуття їх «жорсткості». При пранні, взаємодіючи з ПАРами мила або пральних порошків, солі жорсткості пов'язують їх і вимагають більшої витрати.
У харчовій промисловості жорстка вода погіршує якість продуктів, викликаючи випадання солей при зберіганні. Це характерно для бутильованої питної води, пива, соків.
Реагентне пом'якшення води
Пом'якшення води методом осадження містяться в ній розчинних солей полягає в створенні умов, при яких утворюються важкорозчинні сполуки CaCO 3 і Mg (OH) 2. випадають в осад і видаляються з води.
Як осадителей застосовують:
- негашене вапно CaO
- гашене вапно (пушонка) CaOH 2
- їдкий натр (каустична сода) NaOH
- вуглекислий натрій (кальцинована сода) Na 2 CO 3
Ці реагенти застосовують кожен окремо і в різній комбінації. Залежно від цього розрізняють наступні способи обробки:
- вапняний (реагент CaO);
- содоізвестковий (реагент Na 2 CO 3 + CaO)
- едконатровий (реагент NaOH)
- содоедконатровий (реагент Na 2 CO 3 + NaOH)
- вапняно-едконатровий (реагент CaO + NaOH)
Багато солі жорсткості мають низьку розчинність. При введенні в розчин деяких реагентів збільшується концентрація аніонів, які утворюють малорозчинні солі з іонами жорсткості Ca 2+ і Mg 2+. Такий процес називають реагентним пом'якшення води.
Розрізняють пом'якшення води вапнуванням і содо-вапнуванням.
При вапнуванні в розчин додають гашене вапно Ca (OH) 2 до рН близько 10. В результаті протікають реакції:
Ca (HCO 3) 2 + Ca (OH) 2 = 2 CaCO 3 + 2 Н 2 O;
Mg (HCO 3) 2 + 2 Ca (OH) 2 = Mg (OH) 2 + 2 З aCO 3 + 2 Н 2 O.
Даний метод застосовують при високою карбонатною і низькою некарбонатних жорсткості води, коли потрібно одночасне зниження жорсткості та лужності. Залишкова жорсткість на 0,4 # 150; 0,8 мг-екв / л перевищує некарбонатную жорсткість. Зазвичай використовується спільно з іонообмінним пом'якшення води.
Гідроксид кальцію (Ca (OH) 2. гашене вапно або «пушонка») # 151; хімічна речовина, серйозна причина. Являє собою порошок білого кольору. погано розчинний у воді.
гашене вапно # 151; так як її отримують шляхом «гасіння» (тобто взаємодії з водою) «негашеного» вапна оксиду кальцію;
Установка для знезалізнення води вапнуванням складається з змішувача 1, освітлювача 2, фільтра 3, збірки з мішалкою 4 для вапняного молока і дозатора вапняного молока 5.
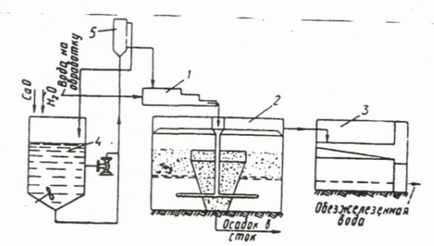
Якщо кількість кисню, що міститься у воді, недостатньо для окислення, одночасно з вапнуванням проводять хлорування або аерація води.
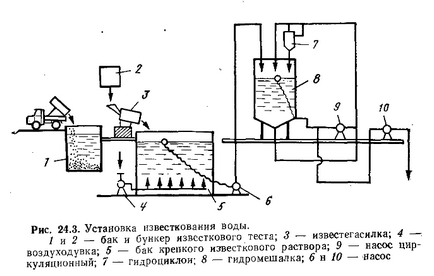
Відстійники малопродуктивні, і отримується в них гідроксидні пульпа має високу вологість # 150; 97 # 150; 99%. Тому вони в даний час практично не застосовуються.
У практиці використовуються різні варіанти освітлювачів зі зваженим шаром осаду. У них очищається розчин подається знизу і проходить через шар осаду. Це збільшує коефіцієнт очищення води. Для зменшення обсягу шламу використовуються додаткові зони і камери шламоуплотненія. Збільшення ступеня освітлення досягається введенням додаткових секцій тонкошарового відстоювання.
При содо-вапнування в воду додають гашене вапно Ca (OH) 2 і соду Na 2 CO 3 до рН близько 10. В результаті протікають реакції:
Ca (HCO 3) 2 + Ca (OH) 2 + Na 2 CO 3 = 2 CaCO 3 + 2 NaOH + Н 2 СО 3;
Mg (HCO 3) 2 + 2NaOH = Mg (OH) 2 + 2NaHCO 3.
Як випливає з рівнянь реакцій, в процесі освіти і осадження осаду з води витягають солі жорсткості. Разом з ними видаляються колоїдні і зважені частинки з асоційованими на них забрудненнями. На пластівцях осаду частково сорбируются органічні забруднення води.
При содо-вапнування за рахунок надлишку іонів HCO 3 досягається більша повнота видалення з води солей жорсткості. Підвищення температури до 70 # 150; 80 ° С дозволяє довести залишкову жорсткість до 0,35 # 150; 1,0 мг-екв / л. Того ж результату можна досягти збільшенням доз реагентів.
Спосіб заснований на реакції вапна з розчиненими у воді вуглекислотою і бікарбонатами кальцію і магнію. Цим методом можна пом'якшити воду тільки до жорсткості 1,4 -1,8 мг - екв / л.
Устаткування найпростішої установки для пом'якшення води даними способом розташовується таким чином, щоб забезпечити самоплив води з напірних збірників 1.
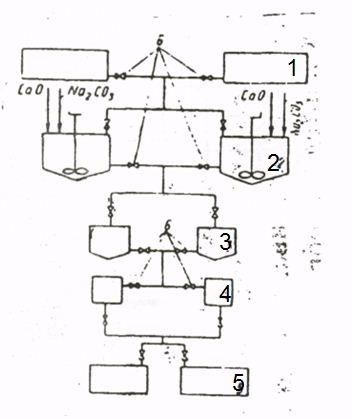
Баки - змішувачі 2 забезпечені мішалками. Дно змішувачів і відстійних резервуарів 3 зазвичай виконується конічним, що полегшує спуск опадів. Установка має парну апаратуру, що дозволяє вести пом'якшення води безперервно. Змішувач зазвичай заповнюють водою до половини, потім в нього вносять необхідну кількість розчинів вапна і соди, після чого додають воду до повного об'єму. Вміст ретельно розмішують мішалкою і спускають в бак - відстійник 3, де витримують протягом 6 ч.
Осветленную воду подають на фільтр 4, після чого вода збирається в збірниках 5. відвідні труби парних баків дозволяють перепускати воду з бака в бак за допомогою вентилів 6, що збільшує маневреність установки.
Бачки для приготування розчинів соди і вапна виготовляють циліндричної форми з конічним днищем. Концентрація розчину соди повинна бути 5 - 6%, а вапна 2 - 3%. Бачки для приготування розчинів повинні бути забезпечені мішалками.
Видалення взвешанной речовин здійснюється відстоюванням і фільтрацією води в фільтрах. Фільтрує служить подрібнений гравій, кварцовий песов, антрацит, мармурова крихта.
Реагентні методи пом'якшення в підготовці питної води не використовуються. Після них вода має сильнолужну реакцію. Вони широко застосовуються в енергетиці і промисловості як перший ступінь очищення до механічних фільтрів. При спільній роботі вони дозволяють пом'якшити воду, видалити зважені речовини, включаючи колоїди, і частково очистити воду від органічних речовин.
Оскільки осадження утворилися пластівців відбувається дуже повільно, продуктивність обладнання низька і воно має великі габарити. В результаті утворюються відходи у вигляді важко утилізованих шламів. Процес вимагає ретельного контролю, причому в основному ручного, оскільки залежить від багатьох факторів: температури води, точності дозування реагентів, вихідної каламутності води і т. П.