Акумулятор -хімічний джерело струму, який має здатність накопичувати і зберігати протягом деякого часу електричну енергію і в міру необхідності віддавати її в зовнішній ланцюг.
Акумулятор сам не виробляє електричну енергію. Він тільки накопичує її при заряді: пропускання струму від стороннього джерела супроводжується перетворенням електричної енергії в хімічну, в результаті, акумулятор сам стає джерелом струму.
При розряді акумулятора накопичена електрична енергія витрачається в підключеної до нього зовнішньої ланцюга (хімічна енергія перетворюється в електричну).
При правильній експлуатації акумулятор витримує кілька сотень циклів заряду і розряду.
Залежно від складу електроліту розрізняють:
· Та лужні акумулятори.
Найпростіший кислотний акумулятор складається з двох свинцевих електродів, занурених у розчин сірчаної кислоти.
Процеси, які відбуваються в кислотному акумуляторі, можна представити таким рівнянням:
PbSO4 - сірчанокислий свинець (сульфат свинцю).
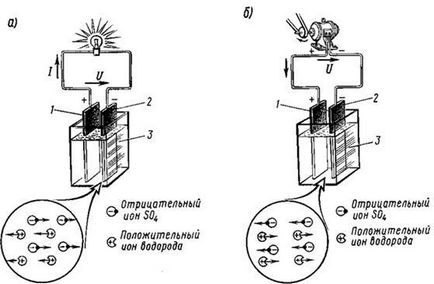
Малюнок 4.2. Проходження через електроліт позитивних і негативних іонів при а) розряді і б) заряді кислотного акумулятора
На локомотивах та електропоїздах найбільшого поширення набули лужні акумулятори (значно більший термін служби, ніж у кислотних).
Повністю заряджений акумулятор має е.р.с. близько 2,2 В, приблизно таке ж напруга на його затискачах, так як внутрішній опір дуже мало.
При розряді напруга швидко падає до 1,8-1,7 В, при цьому напрузі розряд припиняється, щоб уникнути пошкодження.
Найбільш поширені нікель-залізні (НЖ) і нікель-кадмієві (НК) лужні акумулятори. У тих і інших активна маса позитивного електрода в зарядженому стані складається з гідрату окису нікелю NiOOH, до якого додають графіт і окис барію.
Графіт збільшує електропровідність активної маси, а окис барію - термін служби. Активна маса негативних пластин нікель-залізного акумулятора складається з порошкового заліза з добавками, а нікель-кадмиевого акумулятора з суміші порошкового кадмію і заліза. Електролітом служить розчин їдкого калію з домішкою моногідрату літію, яка збільшує термін служби акумулятора.
Електрохімічні реакції, що протікають при заряді і розряді лужного акумулятора, можна представити наступними рівняннями:
2Ni (OOH) + 2KOH + Fe 2Ni (OH) 2 + 2KOH + Fe (OH) 2
2Ni (OOH) + 2KOH + Cd 2Ni (OH) 2 + 2KOH + Cd (OH) 2
Ni (OОH) - гідрат окис нікелю;
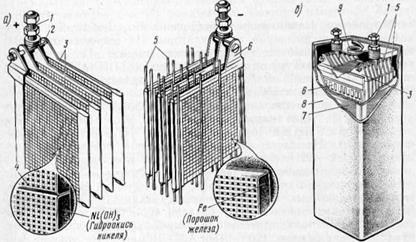
Малюнок 4.3. Напівблоки негативних і позитивних пластин (а) і загальний вид (б)
нікель-залізного акумулятора ТПНЖ, що застосовується на тепловозах:
1 - вивідний штир; 2 - шпилька; 3 - позитивні пластини; 4 - сталеві нікелерованние рамки (ламелі); 5 - сепаратори; 6 - негативні пластини; 7 - корпус;
8 - гумовий чохол; 9 - отвір з пробкою для заливки електроліту
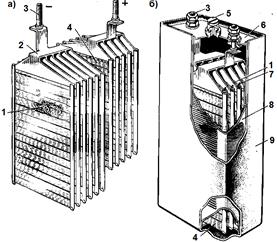
Малюнок 4.4. Напівблоки негативних і позитивних пластин (а) і загальний вид (б) нікель-кадмиевого акумулятора НКН-100 для е.п.с. 1 - негативні пластини; 2 - з'єднувальний місток; 3 - вивідний штир; 4 - позитивні пластини; 5 - отвір з пробкою для заливки електроліту; 6 - кришка; 7 - сепаратор; 8 - корпус; 9 - гумовий чохол
Повністю заряджений акумулятор має е.р.с. приблизно 1,45 В. Внаслідок великого внутрішнього опору його напруга при розряді значно менше цього значення. При розряді напруга швидко падає до 1,3 В, потім повільно до 1 В. Розряджати нижче цього напруги забороняється.
Переваги лужних акумуляторів:
· При їх виготовленні не використовується дефіцитний свинець;
· Вони мають більшу витривалістю і механічною міцністю, не бояться сильних струмів розряду, тряски, ударів і навіть коротких замикань;
· При тривалому бездіяльності несуть малі втрати на саморазряд і не псуються, мають великий термін служби;
· При роботі виділяють меншу кількість шкідливих газів і випарів;
· Мають меншу вагу;
· Менш вимогливі щодо постійного кваліфікованого догляду.
· Нижчий ККД
· Більш висока вартість.
1. Яке призначення акумулятора?
2. Принцип роботи кислотного акумулятора.
3. Принцип роботи лужного акумулятора.
4. Переваги лужних акумуляторів.
5. Недоліки лужних акумуляторів.
6. Чому дорівнює е.р.с. повністю зарядженого акумулятора?
7. З чого складається найпростіший кислотний акумулятор?
8. Як називаються пристрої, що перетворюють хімічну енергію в електричну?
9. Що таке електроліт?
10. Що таке електроліз?
11. На які складові розпадається молекула сірчаної кислоти?
12. З чого складається гальванічний елемент Вольта?
13. Як відбувається поляризація елемента?
14. Який вплив надають іони водню на роботу акумуляторної батареї?
15. Що таке сухий гальванічний елемент?
16. Як проходить електричний струм в рідких провідниках?
17. Яка конструкція кислотних акумуляторів?
19. Яким чином заряджають акумулятори?
20. Що є ознакою кінця заряду у кислотного акумулятора?
21. Що є ознакою кінця заряду у лужного акумулятора?
22. Як з'єднують акумулятори в батарею?
4.3. Способи з'єднання акумуляторів в батарею
Послідовне. коли мінус кожного попереднього джерела з'єднаний з плюсом наступного. За другим законом Кірхгофа результуюча ЕРС дорівнює сумі е.р.с. окремих акумуляторів. Чим більше акумуляторів в ланцюзі, тим більша напруга на приймачах.
Якщо батарея буде замкнута на зовнішній опір R, то
Послідовно з'єднують акумулятори, коли напруга споживача вище напруги одного акумулятора.
Паралельне. коли позитивні затискачі кількох акумуляторів з'єднують між собою і виводять на загальний плюс, і негативні затискачі з'єднують між собою і виводять на загальний мінус.
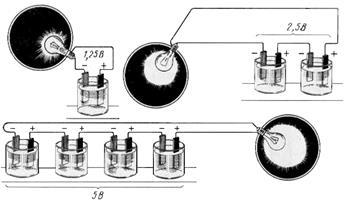
Малюнок 4.5. Напруга, прикладена до приймача, при різній кількості послідовно з'єднаних акумуляторів
Паралельне з'єднання застосовують, коли напруга споживача дорівнює напрузі одного акумулятора, а струм, необхідний споживачеві, більше розрядного струму одного акумулятора.
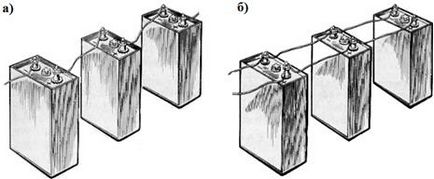
Малюнок 4.6. Послідовне (а) і паралельне (б) з'єднання акумуляторів
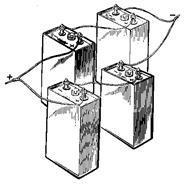
Змішане з'єднання застосовується, коли акумулятори не забезпечують можливості отримання необхідного струму і напруги. На рис. 4.7 в кожній з двох паралельних груп акумуляторної батареї є по два послідовно з'єднаних акумулятора.
Малюнок 4.7. Змішане з'єднання акумуляторів
Акумуляторні батареї в більшості випадків складаються з послідовно з'єднаних акумуляторів. Змішане і паралельне з'єднання акумуляторів застосовують рідко, тому що важко забезпечити рівномірний розподіл струму між паралельними гілками.
1. Які види з'єднання акумуляторів Ви знаєте?
2. У чому суть послідовного з'єднання акумуляторів?
3. Яке з'єднання акумуляторів називається паралельним?
4. Яке з'єднання акумуляторів називається змішаним?