Визначення і формула пропіонової кислоти
Пропіонова (пропановая) кислота - це складна органічна сполука, що відноситься до класу граничних одноосновних карбонових кислот.
У звичайних умовах являє собою безбарвну їдку рідину з різким запахом. Самозаймається при температурі 440 o C. Змішується з водою і органічними розчинниками.
Хімічна формула пропіонової кислоти
Хімічна формула пропіонової кислоти може записуватися двояко: C2 H5 COOH або C3 H6 O2. Вона показує, що до складу даної молекули входять три атома вуглецю (Ar = 12 а.е.м.), шість атомів водню (Ar = 1 а.е.м.) і два атоми кисню (Ar = 16 а.о. м.). За хімічною формулою можна обчислити молекулярну масу пропіонової кислоти:
Mr (C3 H6 O2) = 3 × 12 + 6 × 1 + 2 × 16 = 36 + 6 + 32 = 74.
Структурна (графічна) формула пропіонової кислоти
Структурна (графічна) формула пропіонової кислоти є більш наочною. Вона показує те, як пов'язані атоми між собою всередині молекули (рис. 1).
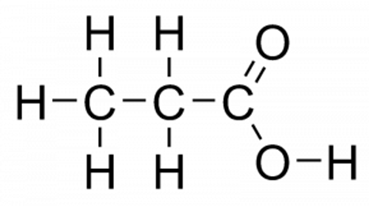
Мал. 1. Пропіонова кислота. Графічна формула.
Приклади розв'язання задач
Одноосновная карбонова кислота містить 26,1% вуглецю і 4,3% водню. На підставі даних умови завдання зробіть необхідні обчислення і встановіть молекулярну формулу органічної речовини.
Запишемо молекулярну формулу одноосновної карбонової кислоти в загальному вигляді як Cx Hy Ow.
ω (С) - ω (H) - ω (O) = 100%.
Тоді, масова частка кисню в складі граничної одноосновної карбонової кислоти буде розраховуватися як:
ω (O) = 100% - ω (С) - ω (H);
ω (O) = 100% - 26,1 - 4,3 = 69,6%.
x: y: w = ω (С) / Ar (С). ω (H) / Ar (H). ω (O) / Ar (O);
x: y: w = 26,1 / 12. 4,3 / 1. 69,6 / 16;
x: y: w: = 2,18. 4,3. 4,35 = 1: 2. 2.
Значить найпростіша формула одноосновної карбонової кислоти матиме вигляд CH2 O2 або HCOOH. Це мурашина кислота.
При повному згорянні певної кількості вуглеводню утворилося 14,08 г оксиду вуглецю (IV) і 3,6 г води. Знайдіть молекулярну формулу речовини, якщо відносна щільність його парів за воднем дорівнює 39.
Складемо схему реакції згоряння амінокислоти позначивши кількість атомів вуглецю, водню, кисню та азоту за «x», «у», «z» і «k» відповідно:
Визначимо маси елементів, що входять до складу цієї речовини. Значення відносних атомних мас, взяті з Періодичної таблиці Д.І. Менделєєва, округлимо до цілих чисел: Ar (C) = 12 а.е.м. Ar (H) = 1 а.е.м. Ar (O) = 16 а.е.м.
Розрахуємо молярні маси вуглекислого газу і води. Як відомо, молярна маса молекули дорівнює сумі відносних атомних мас атомів, що входять до складу молекули (M = Mr):
M (CO2) = Ar (C) + 2 × Ar (O) = 12 + 2 × 16 = 12 + 32 = 44 г / моль;
M (H2 O) = 2 × Ar (H) + Ar (O) = 2 × 1 + 16 = 2 + 16 = 18 г / моль.
m (C) = [14,8 / 44] × 12 = 4,04 г;
m (H) = 2 × 3,6 / 18 × 1 = 0,4 м
Визначимо хімічну формулу вуглеводню:
x: y = m (C) / Ar (C). m (H) / Ar (H);
Значить його найпростіша формула CH, а молярна маса 13 г / моль [M (CH) = Ar (C) + Ar (H) = 12 + 1 = 13 / моль].
Значення молярної маси органічної речовини можна визначити за допомогою його щільності за воднем:
Msubstance = 2 × 39 = 78 г / моль.
Щоб знайти справжню формулу органічної сполуки знайдемо відношення отриманих молярних мас:
Msubstance / M (CH) = 78/13 = 6.
Значить індекси атомів вуглецю і водню повинні бути в 6 разів вище, тобто формула речовини матиме вид C6 H6 .Це бензол.