Загальні відомості про будову атома калію
Калій - перший елемент четвертого періоду. Він розташований в I групі головною (А) підгрупі Періодичної таблиці.
Відноситься до елементів s - сімейства. Метал. Елементи-метали, що входять в цю групу, носять загальна назва лужних. Позначення - K. Порядковий номер - 19. Відносна атомна маса - 39,102 а.е.м.
Електронна будова атома калію
Атом калію складається з позитивно зарядженого ядра (+19), всередині якого є 19 протонів і 20 нейтронів, а навколо, по 4-м орбітах рухаються 19 електронів.
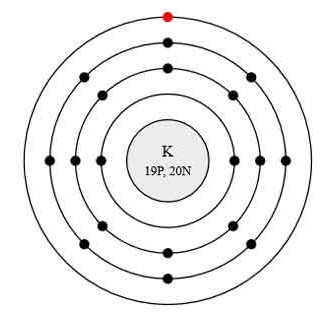
Рис.1. Схематична будова атома калію.
Розподіл електронів по орбіталях виглядає наступним чином:
Зовнішній енергетичний рівень атома калію містить 1 електрон, який є валентним. Ступінь окислювання калію дорівнює +1. Енергетична діаграма основного стану приймає наступний вигляд:
Збудженого стану, незважаючи на наявність вакантних 3p - і 3d орбіталей немає.
Приклади розв'язання задач
Атом елемента має наступну електронну конфігурацію 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 3. Вкажіть: а) заряд ядра; б) число завершених енергетичних рівнів в електронній оболонці цього атома; в) максимально можливу ступінь окислення; г) валентність атома в поєднанні з воднем.
Для того, щоб відповісти на поставлені питання, спочатку потрібно визначити загальне число електронів в атомі хімічного елемента. Це можна зробити, склавши всі електрони, наявні в атомі, не враховуючи їх розподілу по енергетичним рівням:
Це миш'як (As). Тепер відповімо на питання:
а) заряд ядра дорівнює +33;
б) атом має чотири рівні, з яких завершеними є три;
в) запишемо енергетичну діаграму для валентних електронів атома миш'яку в основному стані.
Миш'як здатний переходить в збуджений стан: електрони s -подуровня розпарюються і один з них переходить на вакантну d орбіталь.
П'ять неспарених електронів свідчать про те, що максимально можливий ступінь окислення миш'яку дорівнює +5;
г) Валентність миш'яку в поєднанні з воднем дорівнює III (AsH3).