Загальні відомості про будову атома азоту
Азот - сьомий за рахунком елемент Періодичної таблиці. Відноситься до неметалів. Розташований у другому періоді V групи A підгрупи.
Порядковий номер дорівнює 7. Заряд ядра дорівнює +7. Атомний вагу - 14,007а.е.м. У природі зустрічаються два ізотопу азоту: 14 N - 99,635% і 15 N - 0,365% (в дужках вказано їх процентне співвідношення).
Електронна будова атома азоту
Атом азоту має дві оболонки, як і всі елементи, розташовані в другому періоді. Номер групи -V - свідчить про те, що на зовнішньому електронному рівні атома азоту знаходиться 5 валентних електронів.
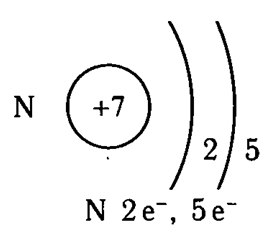
Мал. 1. Схематичне будова атома азоту.
Електронна конфігурація основного стану записується в такий спосіб:
Азот - елемент p-сімейства. Енергетична діаграма для валентних електронів в збудженому стані виглядає наступним чином:
Збудженого стану немає. За кількістю неспарених електронів можна сказати, що азот в з'єднаннях проявляє валентність III. Однак, валентність так само визначається за номером групи (V), отже, азот може проявляти дві валентності - III і V.
Мал. 2. Просторове зображення будови атома азоту.