- Чи бували ви взимку на березі швидкої гірської річки? Подивіться на малюнок нижче (рис. 2.23). Навколо лежить сніг, завмерли на березі дерева, покриті інеєм, який сяє в сонячних променях, а реч-ка не замерзає. Надзвичайно чиста, прозора вода розбиває-ся про обмерзлі камені. Чому з'явився іній? У чому відмінність води і льоду? Чи є між ними подібність? У цьому параграфі ви орга-тельно знайдете відповіді на ці питання.
1. Спостерігаємо різні агрегатні стани речовини
Ви вже знаєте, що вода і лід (сніг, іній) - це два різних агрегатних стану води. рідке і тверде. Поява інею на де-ревьях пояснюється просто: вода з поверхні річки випаровується, перетворюючись на водяну пару. Водяна пара, в свою чергу, конденсується і осідає у вигляді інею. Водяна пара - це тре-тє стан води - газоподібний.
Наведемо ще один приклад. Ви, безуслов-но, знаєте про небезпеку розбити медичний термометр: в ньому міститься ртуть - густа рідина сріблястого кольору, яка, випаровуючись-Ясь, утворює дуже отруйний пар. А ось при температурі нижче -39 ° С ртуть перетворюється в твердий метал. Таким чином, ртуть, як і вода, може перебувати в твердому, рідкому і газоподібному станах.
Практично будь-яка речовина в залежне ти від фізичних умов може перебувати в трьох агрегатних станах: твердому, рідкому і газоподібному.

Мал. 2.23 Різні агрегатні стани води
У нашому прикладі з гірською річкою (рис. 2.23) присутні всі три агре-Гатне стану води.
Існує ще одне агрегатний стан речовини - плазма. Напри-заходів, ртуть в плазмовому стані міститься у включених ртутних лампах (так звані лампи денного світла). У мегамире плазма є-ється поширеним станом речовини, так як саме в цьому відбутися у-янии знаходиться речовина в надрах зірок.
Водяна пара, вода, лід - це три агрегатних стани одного і того ж речовини, утвореного однаковими молекулами - молекулами води. Чому ж фізичні властивості речовин, утворених однаковими мо-лекул, але знаходяться в різних агрегатних станах, відрізняються один від одного? Ймовірно, причина такої відмінності полягає в тому, що молекули по-різному рухаються і взаємодіють.
Які ж властивості мають речовини в різних агрегатних станах? Як при цьому рухаються і взаємодіють молекули?
2. Спостерігаємо і пояснюємо фізичні властивості твердих тіл
Подивіться уважно на рис. 2.24. Всі зображені на ньому твер-Диє тіла відрізняються один від одного: кольором, видом і т. П. Вони виготовлені з різних речовин. Разом з тим вони мають і загальні властивості, притаманні всім твердих тіл.
Тверді тіла зберігають об'єм і форму. Це пояснюється тим, що ато-ми і молекули твердих тіл розташовані в позиціях рівноваги. Сили тяжіння і відштовхування між молекулами (атомами) в цих позиціях рівні один одному. У разі спроби збільшити або зменшити відстань між частинками (т. Е. Збільшити або зменшити розмір тіла) виникає відповідно межмолекулярное тяжіння або відштовхування (див. § 14).
Ви знаєте, що відповідно до атомно-молекулярної теорії атоми (молекули) завжди знаходяться в русі. Частинки твердих тіл практичес-но не пересуваються з місця на місце - вони постійно рухаються біля певної точки, т. Е. Коливаються. Тому тверді тіла зберігають не тільки обсяг. але і форму.

Мал. 2.24. Незважаючи на зовнішні відмінності, будь-які тверді тіла зберігають форму і об'єм
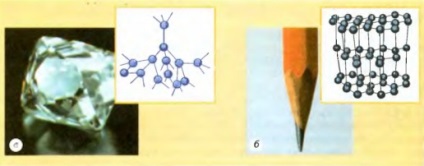
Мал. 2.25 Моделі кристалічних решіток: про - алмазу, 6 - графіту. Кульками зображені центри атомів; ліній, що з'єднують атоми, насправді не існує, вони проведені тільки для того, щоб пояснити характер просторового розташування атомів
3. Розрізняємо кристалічні і аморфні речовини
В ході вивчення будови твердих тіл за допомогою сучасних мето-дів вдалося з'ясувати, що молекули й атоми більшості речовин в тведого стані розташовані в строго визначеному порядку, фізики го-ворят: утворюють кристалічну решітку. Такі речовини називаються кристалічними. Прикладами кристалічних речовин можуть бути ал-маз, графіт (рис. 2.25), лід, сіль (рис. 2.26), метали і т. П.
Порядок розташування атомів в кристалічній решітці речовини оп-ределяет його фізичні властивості. Так, наприклад, алмаз і графіт складаються з одних і тих самих атомів - атомів вуглецю, однак ці речовини дуже відрізняються один від одного, так як атоми в них розташовані по-різному (див. Рис. 2.25).
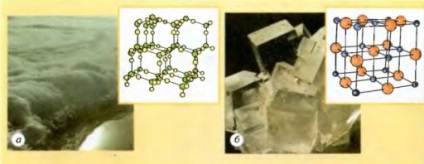
Мал. 2.26. Моделі кристалічних решіток: а - льоду б - кухонної солі (маленькі кульки - атоми натрію, великі - атоми Хлору)

Мал. 2.27. У рідкому стані речовина зберігає об'єм, але набуває форму судини, в якому знаходиться
Мал. 2.28. Молекули рідини розташовані майже впритул один до одного. У невеликому обсязі рідини спостерігається взаємна орієнтація сусідніх молекул (існує ближній порядок). В цілому ж молекули рідини розташовані хаотично
Існує група твердих речовин (скло, віск, смола, бурштин і т. П.), Молекули (атоми) яких не утворюють кристалічної решітки і в це-лом розташовані безладно. Такі речовини називають аморфними.
При певних умовах тверді тіла плавляться, т. Е. Переходять в жид-кое стан. Кристалічні речовини плавляться при певній температурі. Наприклад, лід зазвичай переходить в рідкий стан, якщо тим-пература дорівнює О ° С, нафталін - якщо досягає 80 ° С, ртуть - якщо падає до -39 ° С. На відміну від кристалічних, аморфні речовини не мають визначенні температури плавлення. У разі збільшення температури вони переходять в рідкий стан поступово (танення воскової свічки).
4. Спостерігаємо і пояснюємо фізичні властивості рідин
Рідини легко змінюють свою форму і набувають форму того судини, в якому вони містяться, проте обсяг рідини при цьому є незмінним (рис. 2.27). Більш того, якщо ми спробуємо стиснути рідину, нам це не вдасться. Щоб довести нестисливі рідин, вчені провели експеримент: воду налили в свинцева куля, який запаяли, а потім сжа-ли потужним пресом. Вода не стиснулася, а просочилася крізь стінки кулі.
Здатність рідин зберігати свій обсяг пояснюється тим, що, як і в твердих тілах, молекули в рідинах розташовані близько один від дру-га (рис. 2.28). Молекули рідини досить щільно упаковані, однак вони не тільки коливаються на одному і тому ж місці в оточенні найближчих «сусідів», а й досить легко можуть переміщатися за обсягом, зайнятого рідиною. Тому рідини зберігають обсяг, але не зберігають фор-ми - вони є текучими.
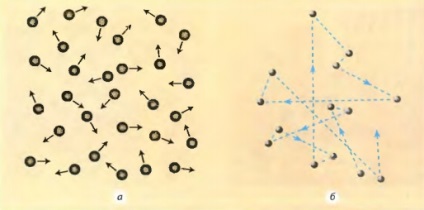
Мал. 2.29 Рух і розташування молекул в газах: а - напрям руху молекул через змінюється в результаті їх зіткнення з іншими молекулами; б - приблизна траєкторія руху молекули повітря при нормальному тиску (збільшення в мільйон разів)
5. Пояснюємо фізичні властивості газів
Слово «газ» походить від грецького chaos ( «хаос», «безлад») І справді, для газоподібного стану речовини характерний повний безлад у взаємному розташуванні і русі молекул.
Молекули газу розташовані на відстанях, які в десятки і со-тни разів перевищують розміри молекул. На таких відстанях молекули практично не взаємодіють один з одним, тому молекули газу розлітаються і газ займає весь наданий об'єм. Великими расстоя-нями між молекулами пояснюється і той факт, що гази легко стиснути.
Щоб зрозуміти, як рухаються молекули газу, уявімо собі рух однієї молекули. Ось вона рухається в якомусь напрямку, на своєму шляху стикається з іншою молекулою, змінює напрямок і швидкість своє-го руху і летить далі, до наступного удару (рис. 2.29). Чим більше кількість молекул в посудині, тим частіше вони стикаються. Наприклад, каж-дая молекула, що входить до складу повітря в класній кімнаті, стикається з іншими молекулами і змінює швидкість свого руху пріблізітель- але п'ять мільярдів раз в секунду.
Практично будь-яка речовина в залежності від фізичних умов може існувати в трьох агрегатних станах: твердому, рідкому і га-зообразном.
Коли речовина переходить з одного стану в інший, змінюється вза-імное розташування молекул і характер їх руху, однак склад молекул залишається незмінним.
1. Назвіть речовину, яка часто можна спостерігати в трьох різних агрегатних станах.
2. Чи можна стверджувати, що ртуть - завжди рідина, а кисень - завжди газ?
3. Чи відрізняються один від одного молекули водяної пари і льоду?
4. Чому тверді тіла з-яке береже обсяг і форму?
5. У чому подібність і в чому відмінність кристал-вої і аморфних речовин?
6. Як рухаються молекули в рідко-стях?
7. Чому гази займають весь наданий об'ем?
1. Виберіть правильну відповідь.
Якщо перелити рідину з однієї судини в іншій, вона:
а) змінює і форму, і обсяг;
б) зберігає і форму, і обсяг;
в) зберігає обсяг, але змінює форму;
г) зберігає форму, але змінює обсяг.
2. Вода випарувалася і перетворилася на пару. Чи змінилися при цьому мо-лекул води? Як змінилися розташування молекул і характер їх руху?
3. Чи може алюміній перебувати в газоподібному стані?
4. Чи може газ заповнити банку наполовину?
5. Чи легко стиснути воду? Відповідь обґрунтуйте.
6. Чи можна стверджувати, що в закритій посудині, частково заповнений-ном водою, над поверхнею води води немає?
7. У чайнику кипить вода. Чи справді ми бачимо водяна пара, що виходить з носика?

1. Використовуючи стакан з водою, доведіть, що в гумовій груші є повітря.
2. Аморфні тіла називають дуже в'язкими рідинами. Використовуючи свічку і, наприклад, маркер, доведіть, що віск, нехай дуже мед-повільно, але тече. Для цього покладіть маркер на підвіконня, свер-ху - перпендикулярно до маркера - покладіть свічку і залиште так на кілька днів. Поясніть результати свого експерименту.
Якщо у вас є виправлення або пропозиції до даного уроку, напишіть нам.
Якщо ви хочете побачити інші коригування та побажання до уроків, дивіться тут - Освітній форум.