Робота №8 (віртуальна)
визначення ставлення теплоємності при постійному тиску до теплоємності при постійному обсязі для повітря методом адіабатичного розширення
Мета роботи - вивчити закони ідеального газу і основні положення класичної теорії теплоємності; визначити коефіцієнт Пуассона - відношення теплоємності при постійному тиску Ср до теплоємності при постійному обсязі CV методом адіабатичного розширення (методом Клемана - Дезорма).
Кількість тепла, яке необхідно повідомити одному молю речовини, щоб підвищити його температуру на 1 К, називають молярної теплоємністю.
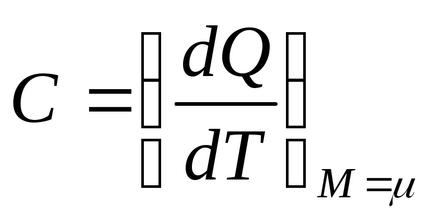
де Q - кількість тепла, що підводиться до системи, Т - абсолютна температура, M - маса газу, - маса одного моля газу.
Як показують теорія і досвід, теплоємність залежить від умов, при яких нагрівається газ, тобто від характеру термодинамічного процесу.
Теплоємність газу при постійному тиску (Сp) більше теплоємності при постійному об'ємі (Cv). Це легко показати якісно на підставі першого закону термодинаміки: кількість теплаQ. підводиться до системи, йде на збільшення внутрішньої енергії сістемиU і на вчинення цією системою работиA над зовнішніми тілами.
Якщо газ нагрівається при постійному обсязі, то робота не відбувається і все підводиться тепло йде на збільшення запасу його внутрішньої енергії U, тобто тільки на підвищення температури газу. Якщо ж газ нагрівається при постійному тиску, він розширюється і виробляє роботу, що вимагає додаткової витрати тепла. Таким чином, для підвищення температури газу на певну величину в изобарном процесі потрібна більша кількість теплоти, ніж при Ізохоричний.
Як випливає з теорії
де R- універсальна газова стала.
Ставлення = Ср / CV входить в рівняння Пуассона, що описує адіабатичний процес, тобто процес, що йде без теплообміну з навколишнім середовищем (Q = 0):
Тут іV1 - тиск і об'єм газу в першому стані; p2 и- тиск і об'єм газу в другому стані.
Повну теплоізоляцію газу від зовнішнього середовища здійснити неможливо. Однак, якщо параметри стану газу змінюються дуже швидко, процес можна наближено вважати адіабатичним. На практиці адіабатичний процес відбувається в деяких теплових двигунах (наприклад, в двигуні Дизеля); поширення звуку в газах (швидке періодична зміна тиску в малих областях простору) також протікає адіабатично.
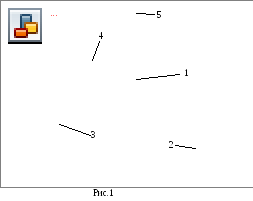
Схема установки показана на малюнку 1. Установка складається з скляної посудини 1, балона 2 зі стисненим повітрям і U- образного рідинного манометра 3. Є також два крана - впускний кран 4, службовець для напуску газу в посудину 1 з балона 2, і випускний кран 5 для з'єднання посудин з атмосферою.
Висновок робочої формули.
Розглянемо метод Клемана - Дезорма. Напустимо повітря в скляну посудину 1 (див. Малюнок) і закриємо кран 4. При швидкому стискуванні температура повітря підвищується. Тому після припинення напуску різниця рівнів рідини в манометрі буде поступово зменшуватися, поки температура повітря всередині посудин не зрівняється з температурою навколишнього повітря. Назвемо стан повітря в посудині після вирівнювання температур станом 1. Параметри стану 1: V1 - обсяг одиниці маси повітря; t1 - температура повітря; р1 - тиск в посудині.
Про ткроем кран5 і, як тільки тиск в посудині зрівняється з атмосферним, закриємо його. Так як розширення відбувається дуже швидко, то процес близький до адіабатичного і, отже, температура знизиться до t2. Обсяг одиниці маси повітря стане рівним V2. Повітря, що залишився в посудині, перейде в стан 2 з параметрами V2. t2. р2 (р2 -атмосферні тиск). Так як температура t2 менше зовнішньої, то повітря в посудині буде поступово нагріватися (слідом-ствие теплообміну з навколишнім середовищем) до температури навколишнього повітря t1. Це нагрівання відбувається изохорический, так як кран закритий. Тиск повітря в посудині збільшується в порівнянні з атмосферним, і в манометрі виникає різниця рівнів h2. тобто повітря переходить в стан 3 з параметрами V2. t1. р3.
Таким чином, ми маємо три стану газу з наступними параметрами:
6) обчислити для кожного вимірювання за формулою (7); знайти середнє значення

7) похибка вимірювання в цьому випадку (величина визначається багаторазово) допускається розрахувати як середню квадратичну для серії n вимірювань:
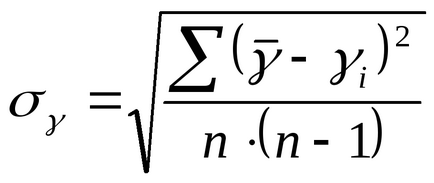
8) привести остаточний результат.
1. Що таке теплоємність, молярна теплоємність, питома теплоємність? Як вони пов'язані? Яка розмірність теплоємності? Від чого залежить молярна теплоємність?
2. Чому Cp> CV з точки зору першого початку термодинаміки?
3. Який процес називають адіабатичним? Яким рівнянням описується адіабатичний процес? Зобразіть АДІАБАТА в координатах p-V.
4. Які термодинамічні процеси відбуваються в даній роботі? Покажіть ці процеси в координатах p-T, V-T, р-V.
5. Чому вимірювання тиску слід проводити не відразу після напуску (випускання) повітря, а через деякий час?