1. Як розташовані електрони по енергетичним рівням і подуровням в атомі вуглецю? Чому в атомі вуглецю можливо розпарювання 2s-електронів і яка у них форма електронних хмар?
Будова електронної оболонки атома вуглецю 1s22s22р2. У атома вуглецю 4 валентних електрони, з них тільки 2 неспарених електрона на 2р-орбіталях.
на другий електронній оболонці є ще вільна 2р-орбіталь, на яку може перейти один з електронів з 2s-орбіталі. При цьому у атома вуглецю стає чотири неспарених електрона:
Так, атом вуглецю може утворювати 4 ковалентні зв'язки, причому відбувається гібридизація орбіталей: утворюються 4 однакові орбіталі, кожна з яких має форму витягнутої вісімки, спрямованої до вершин тетраедра.
2. Зобразіть електронні формули метану і етану. Поясніть, як утворюються хімічні зв'язки в молекулах цих речовин при перекривання відповідних електронних хмар.
Електронні формули метану і етану:
метан
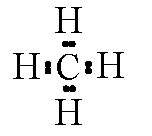
У молекулі метану утворюється чотири хімічні зв'язки при перекривання чотирьох гібридних sр3-орбіталей атома вуглецю з 1 s -орбіталямі чотирьох атомів водню.
У молекулі етану зв'язок між атомами вуглецю утворюється при перекривання гібридних sр3-орбіталей двох атомів вуглецю. У кожного атома залишається ще по три гібридних орбіталі, і при перекривання цих орбіталей з 1 s -орбіталямі шести атомів водню утворюється шість зв'язків С-Н.
3. Дослідним шляхом доведено, що у метану тетраедричних форма будови молекул. Як цей експериментальний факт пояснює вчення про форми електронних хмар і їх гібридизації?
При гібридизації електронних хмар в атомі вуглецю з однієї s-орбіталі і трьох р-орбіталей утворюються чотири однакові гібридні sp3-орбіталі. Гібридні орбіталі спрямовані до вершин тетраедра, і при утворенні ковалентних зв'язків ці зв'язки також виявляються спрямовані до вершин тетраедра. Тому молекула метану має тетраедричних форму.
4. Які сполуки називаються граничними вуглеводнями? Наведіть приклади.
Граничними називаються вуглеводні із загальною формулою с2н2n + 2. приклади: метан СН4, етан С2Н6, гексан С6Н14.
5. Алкана, молекула якого містить сім атомів вуглецю, має формулу:
А. С7Н16
6. Формули тільки алканів записані в ряду:
2) С2Н6, С3Н8, С4Н10
7. Які речовини називаються гомологами? Наведіть приклади
Гомологи - це органічні сполуки, що відрізняються один від одного на одну або кілька груп-СН2. Гомологами є алкани: метан, етан, пропан і т.д.
8. Напишіть формули і назви радикалів, які можна вивести з перших шести граничних вуглеводнів.
метил
9. Складіть скорочені структурні формули і підпишіть назви всіх можливих ізомерів гексану.
гексан
10. Наведіть назви граничних вуглеводнів, які мають такі формули:
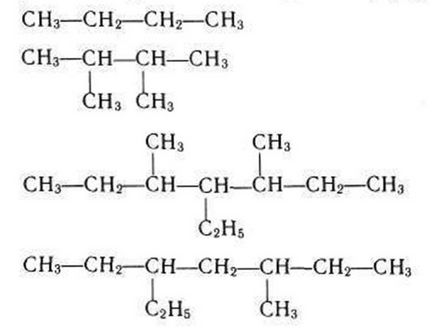
а) бутан
б) 2,3-діметілбутан
в) 3,5-диметил-4-етілгептан
г) з-метил-5-етілгептан
11. Зобразіть структурну формулу 2,2,4-триметилпентана
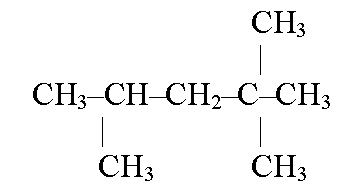
12. Де і в якому вигляді граничні вуглеводні зустрічаються в природі?
Метан - основна частина природного газу, також утворюється при розкладанні рослинних залишків. Др. алкани також входять до складу природного газу, вуглеводні з великим числом атомів вуглецю входять до складу нафти.
13. При нагріванні ацетату натрію з гідроксидом натрію утворюється:
2) метан
14. При взаємодії хлорметана з натрієм утворюється:
2) етан
15. Для алканів характерні реакції:
2) заміщення
16. Як дослідним шляхом можна відрізнити метан від водню?
При горінні метану утворюється крім води СО2:
якщо пропустити що утворюється при згоранні метану газ через вапняну воду, випадає осад:
17. За яких умов відбувається дегидрирование етану? Напишіть рівняння реакції:
Дегидрирование етану відбувається при нагріванні в присутності каталізатора, при цьому утворюється етилен:
18. На прикладі хлоретану на основі сучасних уявлень розкрийте сутність взаємовпливу атомів в молекулі.
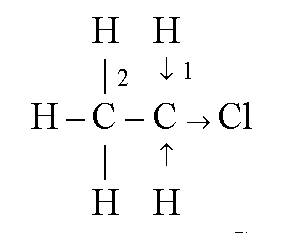
У молекулі хлоретану електронна щільність зміщена до хлору. За рахунок нерівномірного розподілу електронної щільності йде різниця потенціалів, що впливає на фізико-хімічні властивості молекули. Вона стає полярною. Наприклад, хлоретан, на відміну від етану, розчинний в спиртах і ефірах.
19. Як в промисловості з вугілля і метану отримують так званий синтез-газ? Складіть рівняння відповідних хімічних реакцій.
20. Складіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення:
1.
2. на світлі утворюється хлорметан:
(Прим. Замість = ставимо →)
21. Складіть конспект відповіді, що характеризує метан і етан, заповнивши таблицю.


