Токсичні елементи (зокрема, деякі важкі метали) складають велику і дуже небезпечну в токсикологічному відношенні групу речовин. Зазвичай розглядають 14 елементів: Hg (ртуть), Pb (свинець), Cd (кадмій), As (миш'як), Sb (сурма), Sn (олово), Zn (цинк), Al (алюміній), Be (берилій), Fe (залізо), Cu (мідь), Ba (барій), Cr (хром), Tl (талій). Зрозуміло, не всі перераховані елементи є отруйними, деякі з них необхідні для нормальної життєдіяльності людини і тварин. Тому часто важко провести чітку межу між біологічно необхідними і шкідливими для здоров'я людини речовинами.
У більшості випадків реалізація того чи іншого ефекту залежить від концентрації. При підвищенні оптимальної фізіологічної концентрації елементу в організмі може наступити інтоксикація. а дефіцит багатьох елементів в їжі і воді може привести до досить важким і важко розпізнаваним явищ недостатності.
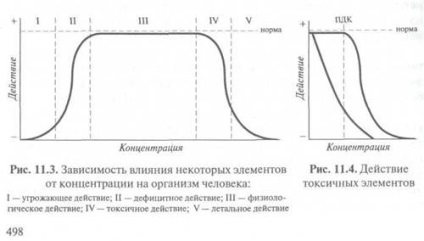
Залежність шкідливого або корисної дії деяких елементів від концентрації показана на рис. 11.3.
Для речовин, що відносяться до так званим супертоксикантів, плато, що характеризує норму, відсутній (або дуже короткий), а крутизна низхідній гілці характеризує токсичність речовини (рис. 11.4).
Забруднення водойм, атмосфери, грунту, сільськогосподарських рослин і харчових продуктів токсичними металами відбувається за рахунок:
- викидів промислових підприємств (особливо вугільної, металургійної та хімічної промисловості);
- викидів міського транспорту (мається на увазі забруднення свинцем від згоряння етилованого бензину);
- застосування в консервному виробництві неякісних внутрішніх покриттів і при порушенні технології припоев;
- контакту з обладнанням (для харчових цілей дозволяється вельми обмежене число сталей та інших сплавів).
Для більшості продуктів встановлені гранично-допустимі концентрації (ГДК) токсичних елементів, до дитячих і дієтичних продуктів пред'являються більш жорсткі вимоги.
Найбільшу небезпеку з вищеназваних елементів представляють ртуть (Hg), свинець (РЬ), кадмій (Cd).
Ртуть - один з найнебезпечніших і високотоксичних елементів, що володіє здатністю накопичуватися в рослинах і в організмі тварин і людини, т. Е. Є отрутою кумулятивної дії.
Токсичність ртуті залежить від виду її сполук, які по-різному всмоктуються, метаболізуються і виводяться з організму. Найбільш токсичні алкілртутние з'єднання з коротким ланцюгом - метилртуть, етілртуть, диметилртуть. Механізм токсичної дії ртуті пов'язаний з її взаємодією з сульфгідрильними групами білків. Блокуючи їх, ртуть змінює властивості або інактивує ряд життєво важливих ферментів. Неорганічні сполуки ртуті порушують обмін аскорбінової кислоти, піридоксину, кальцію, міді, цинку, селену; органічні - обмін білків, цистеїну, аскорбінової кислоти, токоферолів, заліза, міді, марганцю, селену.
Захисним ефектом при впливі ртуті на організм людини мають цинк і, особливо, селен. Припускають, що захисну дію селену обумовлено деметилюванню ртуті і утворенням нетоксичного з'єднання - селено-ртутного комплексу.
Про високу токсичність ртуті свідчать і дуже низькі значення ГДК: 0,0003 мг / м 3 в повітрі і 0,0005 мг / л у воді. Безпечним рівнем вмісту ртуті в крові вважають 50-100 мкг / л. Людина отримує з добовим раціоном близько 0,05 мг ртуті, що відповідає рекомендаціям ФАО / ВООЗ.
Свинець - один з найпоширеніших і небезпечних токсикантів. Історія його застосування дуже давня, що пов'язано з відносною простотою його отримання і великий поширеністю в земній корі (1,6х10 -3%). Сполуки свинцю - Рb3 О4 і PbSO4 - основа широко застосовуваних пігментів: сурику і свинцевого білила. Глазурі, які використовуються для покриття керамічного посуду, також містять сполуки Рb.
Металевий свинець з часів Стародавнього Риму застосовують при прокладці водопроводів. В даний час перелік областей його застосування дуже широкий: виробництво акумуляторів, електричних кабелів, хімічне машинобудування, атомна промисловість, виробництво емалей, замазок, лаків, кришталю, піротехнічних виробів, сірників, пластмас і т. П.
Світове виробництво свинцю становить більше 3,5х10 6 т на рік. В результаті виробничої діяльності людини в природні води щорічно потрапляє 500-600 тис. Т, а в атмосферу в переробленому і дрібнодисперсному стані викидається близько 450 тис. Т, переважна більшість якого осідає на поверхні Землі. Основним джерелом забруднення атмосфери свинцем є вихлопні гази автотранспорту (260 тис. Т) і спалювання кам'яного вугілля (близько 30 тис. Т).
Механізм токсичної дії свинцю має подвійну спрямованість. По-перше, блокада функціональних SH-груп білків і, як наслідок, - інактивація ферментів, по-друге, проникнення свинцю в нервові і м'язові клітини, освіту лактату свинцю, потім фосфату свинцю, які створюють клітинний бар'єр для проникнення іонів Са 2+. Основними мішенями при впливі свинцю є кровотворна, нервова і травна системи, а також нирки.
Свинцева інтоксикація може призводити до серйозних порушень здоров'я, що виявляється в частих головних болях, запамороченнях, підвищеної стомлюваності, дратівливості, погіршенні сну, м'язової гіпотонії. а в найбільш важких випадках до паралічів і парезів, розумової відсталості. Неповноцінне харчування, дефіцит в раціоні кальцію, фосфору, заліза, пектинів, білків (або підвищене надходження кальциферол) збільшують засвоєння свинцю, а отже - його токсичність. Допустима добова доза (ДСД) свинцю становить 0,007 мг / кг; величина ГДК у питній воді - 0,05 мг / л.
Заходи щодо профілактики забруднення свинцем сировини і харчових продуктів повинні включати державний і відомчий контроль за промисловими викидами свинцю в атмосферу, водойми і грунт. Необхідно істотно знизити або повністю виключити застосування тетраетилсвинцю в бензині, свинцевих стабілізаторах, виробах з полівінілхлориду, барвниках, пакувальних матеріалах і т. П.
Кадмій широко застосовується в різних галузях промисловості. У повітря кадмій надходить разом зі свинцем при спалюванні палива на ТЕЦ, з газовими викидами підприємств, що виробляють або використовують кадмій. Забруднення грунту кадмієм відбувається при осіданні кадмій-аерозолів з повітря і доповнюється внесенням мінеральних добрив: суперфосфату (7,2 мг / кг), фосфату калію (4,7 мг / кг), селітри (0,7 мг / кг).
В одній сигареті міститься 1,5-2,0 мкг Cd. Подібно ртуті і свинцю, кадмій не є життєво необхідним металом. Потрапляючи в організм, кадмій проявляє сильне токсичну дію, головною мішенню якого є нирки. Механізм токсичної дії кадмію пов'язаний з блокадою сульфгідрильних груп білків; крім того, він є антагоністом цинку, кобальту, селену, пригнічує активність ферментів, що містять зазначені метали. Відома здатність кадмію порушувати обмін заліза і кальцію.
Все це може призвести до широкого спектру захворювань: гіпертонічна хвороба, анемія, ішемічна хвороба серця, ниркова недостатність та інші. Відзначено канцерогенний, мутагенний та тератогенні ефекти кадмію. За рекомендаціями ВООЗ допустима добова доза (ДСД) кадмію - 1 мкг / кг маси тіла.
Алюміній. Перші дані про токсичність алюмінію були отримані в 70-х рр. XX ст. і це стало несподіванкою для людства. Будучи третім за поширеністю елементом земної кори (8,8% маси земної кори складає А1) і володіючи цінними якостями, металевий алюміній знайшов широке застосування в техніці і побуті. Постачальниками алюмінію в організм людини є алюмінієвий посуд, якщо вона контактує з кислим або лужним середовищем, вода, яка збагачується іонами А1 3+ при обробці її сульфатом алюмінію на водоочисних станціях.
Істотну роль в забрудненні навколишнього середовища іонами А1 3+ грають і кислотні дощі. Не слід зловживати містять гідроксид алюмінію ліками: протигемороїдальний, протівоартрітнимі, що знижують кислотність шлункового соку. Як буферну добавку вводять гідроксид алюмінію і в деякі препарати аспірину і в губну помаду. Серед харчових продуктів найвищою концентрацією алюмінію (до 20 мг / г) володіє чай.
Вступники в організм людини іони А1 3+ в формі нерозчинного фосфату виводяться з фекаліями, частково всмоктуються в кров і виводяться нирками. При порушенні діяльності нирок відбувається накопичення алюмінію, яке призводить до порушення метаболізму Са, Mg, P, F, що супроводжується зростанням крихкості кісток, розвитком різних форм анемії. Крім того, були виявлені і більш грізні прояви токсичності алюмінію: порушення мови, провали в пам'яті, порушення орієнтації і т. П. Все це дозволяє наблизити «нешкідливий», що вважався нетоксичним до недавнього часу алюміній до «похмурої трійці» супертоксикантов: Hg, Pb , Cd.
Миш'як як елемент в чистому вигляді отруйний тільки в високих концентраціях. Він належить до тих мікроелементів, необхідність яких для життєдіяльності організму людини не доведена, а його сполуки, такі як миш'яковистий ангідрид, арсеніти і арсенати, сильно токсичні. Миш'як утримується в усіх об'єктах біосфери (в земній корі - 2 мг / кг, в морській воді - 5 мкг / кг). Відомими джерелами забруднення навколишнього середовища миш'яком є електростанції, що використовують буре вугілля, мідеплавильні заводи; він використовується при виробництві напівпровідників, скла, барвників, інсектицидів, фунгіцидів і ін.
Залежно від дози миш'як може викликати гостре і хронічне отруєння, разова доза миш'яку 30 мг - смертельна для людини. Механізм токсичної дії миш'яку пов'язаний з блокуванням SH-груп білків і ферментів, що виконують в організмі найрізноманітніші функції.