Швидкість хімічної реакції = зміни кількості речовини в одиницю часу в одиниці реакційного простору-ства
Середня швидкість реакції дорівнює:
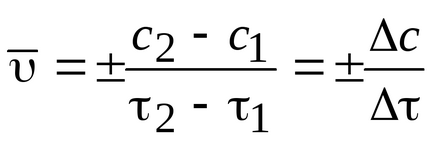
Фактори, що впливають на швидкість хімічної реакції. Швидкість хімічної реакції визначається наступними ос-основними факторами:
природою реагуючих речовин (енергія активації);
концентрацією реагуючих речовин (закон дію-чих мас);
температурою (правило Вант-Гоффа);
наявністю каталізаторів (енергія активації);
тиском (реакції за участю газів);
ступенем подрібнення (реакції, що протікають за участю твердих речовин);
видом випромінювання (видиме, УФ, ІК, рентгенівське).
Зав-ть швидкості хімічної реакції від концентрації виражається основним законом хімічної кінетики - законом діючих мас.
18.Сформуліруйте основний закон хімічної кінетики - закон діючих мас. Що таке константа швидкості реакції?
У 1865 р професор Н. Н. Беке-тов вперше висловив гіпотезу про кількісну взаємозв'язку між масами реагентів і часом перебігу реакції: «. при-тяжіння пропорційно добутку діючих мас ». Ця гіпотеза знайшла підтвердження в законі дії мас, який був встановлений в 1867 р двома норвезькими хі-ками К. М. Гульдбергом і П. Вааге. Сучасна формулює-ка закону дії мас така: при постійній температурі швидкість хімічної реакції прямо пропорційна произве-ня концентрацій реагуючих речовин, взятих у ступенях, рівних стехиометрическим коефіцієнтам в уравненш реакції.
Для реакції АА + ВВ = ТМ + nN кінетичне рівняння за-кону дії мас має вигляд:
де

k - коефіцієнт пропорційності, званий кон-константи швидкості хімічної реакції (при
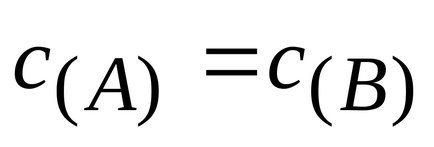

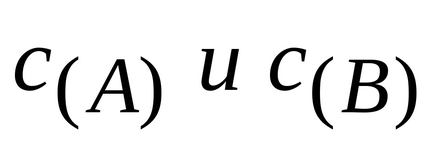
Константа швидкості хімічної реакції не залежить від кон-центрації реагентів, а визначається природою реагуючих речовин і умовами протікання реакцій (температурою, нали-Чієм каталізатора). Для конкретної реакції, що протікає при даних умовах, константа швидкості є величина постійна.
19.Правіло Вант-Гоффа. Температурний коефіцієнт швидкості реакції.
Залежність швидкості реакції від температури приблизно визначається емпіричним правилом Вант-Гоф-фа: при зміні температури на кожні 10 градусів ско-кість більшості реакцій змінюється в 2-4 рази.
Математично правило Вант-Гоффа виражається так:
γ-температурний коефіцієнт швидкості реакції.
Значення γ для ендотермічної реакції вище, ніж для екзо- термічної. Для багатьох реакцій γ лежить в межах 2-4.
Фізичний сенс величини γ полягає в тому, що він показує, у скільки разів змінюється швидкість реакції при зміні температури на кожні 10 градусів.
Оскільки швидкість реакції і константа швидкості хімічної реакції прямопропорційні, то вираз (3.6) часто записують в наступному вигляді:
γ-температурний коефіцієнт швидкості реакції.