ВЗАЄМОДІЯ ПОВЕРХОНЬ ТВЕРДИХ ТІЛ з навколишнім середовищем
Молекули навколишнього середовища в процесі безладного теплового руху стикаються з поверхнею твердого тіла і вступають з нею у взаємодію, висаджуючи переважно на активних центрах поверхні, тобто на ділянках, де виходять на поверхню ребра і грані кристаллитов, дефекти атомної решітки - дислокації, сторонні атоми і т.д. що забезпечує підвищену надлишкову (вільну) поверхневу енергію, і де тому взаємодія з висадилися молекулами протікає більш активно. В результаті концентрація молекул навколишнього середовища (званої в цьому випадку адсорбатом) у поверхні твердого тіла (в даному випадку адсорбенту) стає більше, ніж в обсязі рідкої або газоподібної фази. Такий процес називається позитивною адсорбцией (або просто адсорбцией). Проходить він мимовільно, так як забезпечує зниження енергії Гіббса поверхні, зменшуючи її поверхневий натяг, а отже, зменшуючи небезпеку адгезії поверхонь в вузлі тертя. При цьому в поверхневий шар краще потрапляють молекули того компонента середовища, який більш знижує міжфазну поверхневий натяг. Тоді про цю речовину кажуть, що воно більш поверхнево-активно.
Найбільшу поверхневу активність проявляють полярні молекули середовища, тобто молекули, що мають жорсткий дипольний момент. В мастильних матеріалах міститься певна кількість молекул, які представляють собою полярну групу (або кілька таких груп), з'єднану з вуглеводневим радикалом. Ці молекули висаджуються на поверхні металу полярної групою до поверхні. Слід мати на увазі, що в результаті емісії електронів з поверхні металів приповерхневих шари збіднені електронами. Це обумовлює існування подвійного електричного шару. У вільній поверхні утворюється область негативного заряду, а в поверхневому обсязі металу - позитивного. В результаті взаємодії цього подвійного електричного шару з полярної групою адсорбирующихся молекул на поверхні утворюється орієнтований мономолекулярний (товщиною в одну молекулу) шар адсорбованих молекул. Вуглеводневий радикал у кожної з таких молекул при повністю заповненому (насиченому) адсорбционном шарі спрямований по нормалі від поверхні розділу фаз, так що утворюється своєрідний частокіл, що покриває цю поверхню, причому адсорбція має місце на активних центрах поверхні. Адсорбовані молекули пов'язані між собою міжмолекулярними силами когезії, які такі великі, що дозволяють говорити про орієнтованому шарі як про двовимірному кристалі.
Потім поверх мономолекулярного шару адсорбуються наступні орієнтовані шари молекул до тих пір, поки загальна товщина шару не буде перевищувати радіус дії поверхневих сил (рис. 1, а). Передбачається, що ці сили достатні, щоб утримати шар товщиною в десятки і сотні нанометрів. Оскільки поверхневі сили слабшають пропорційно третього або четвертого ступеня відстані, то кожен поверхневий шар пов'язаний з металом менше, ніж попередній. За межами граничного шару виникають перехідні шари, що утворюються завдяки слабким взаємодіям між адсорбованими молекулами (тобто їх кінцевими вуглеводневими групами) і молекулами середовища або агрегатами молекул, так як в мастильних матеріалах -рідку або пластичних - молекули, як правило, знаходяться в агрегованому стані. Якщо сили взаємодії з поверхнею більше, ніж сили, що зв'язують молекули в агрегати, то ці агрегати руйнуються і молекули адсорбуються на поверхні розділу або на вже утворилися адсорбційних шарах. В іншому випадку, як показав Г.І. Шор, такі агрегати (міцели) можуть утворювати граничний шар (мицеллярная адсорбція) (рис. 1, б). На думку Блюма, міцели утворюють граничний шар поверх адсорбованого (рис. 1, в). Нижче розглядається модель молекулярної адсорбції як найбільш розроблена.
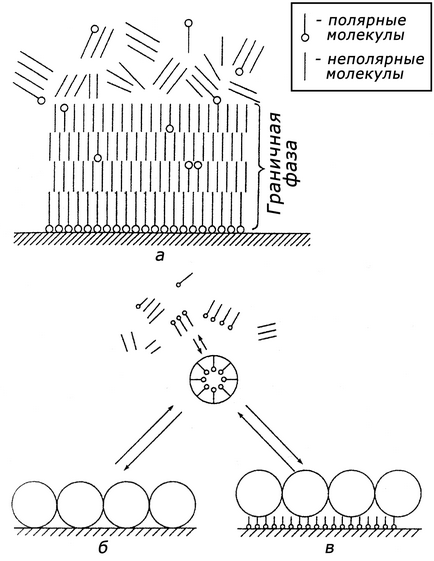
Мал. 1. Будова граничного адсорбційного шару: а - по Дерягин; б - по Шору; в - по Блюму.
Полярні молекули також можуть утворювати граничний шар, оскільки поверхня металу індукує в них дипольний момент. Однак зв'язок їх з поверхнею істотно менш міцна. Якщо до складу середовища входять як полярні, так і неполярні компоненти, то полярні молекули, утворюючи адсорбований орієнтований шар, повідомляють ту ж орієнтацію неполярних молекул (див. Рис. 1, а).
Граничні шари на поверхні твердого тіла за своїми властивостями різко відрізняються від властивостей середовища в обсязі. Згідно А.С. Ахматову, вони подібні до твердому кристалічному тілу (орієнтація частинок), а також мають істинної пружністю форми (підкоряються закону Гука). Граничні шари мають високим опором стисненню і багато меншим - зрушення. Як показав Б.В. Дерягин, в'язкість граничних шарів істотно вище, ніж об'ємна, причому при переході до граничного шару в'язкість підвищується стрибкоподібно.
У науковій літературі розглядають два види адсорбції:
- фізична (оборотна) адсорбція виникає під дією сил Ван-дер-Ваальса і розглянута вище. Енергія зв'язку молекул з поверхнею невелика (від 5-10 кДж / моль для простих молекул і до 40-80 кДж / моль для складних молекул);
- хімічна адсорбція (хемосорбцня) виникає під дією хімічного зв'язку між поверхневими частками твердого тіла і молекулами середовища. Енергія зв'язку хемосорбірованной молекули з поверхнею вище, ніж при фізичній адсорбції і її можна порівняти з енергією хімічної реакції (40-400 кДж / моль). Хемосорбція зазвичай вимагає певної енергії активації і тому протікає при температурах, що перевищують деяку мінімальну температуру.
Фізична адсорбція, навпаки, зменшується з ростом температури. Інша відмінність хемосорбції від фізичної адсорбції полягає в тому, що перша утворює двовимірну фазу і припиняється після заповнення мономолекулярного шару. Поверх хемосорбірованного шару молекул можлива багатошарова фізична адсорбція молекул середовища.
Слід мати на увазі, що адсорбція, пов'язана з хімічним взаємодією, не обов'язково має наслідком зниження поверхневої енергії твердої фази.
Подальшої стадією взаємодії поверхні твердого тіла з активними компонентами середовища є хімічна реакція з утворенням хімічно модифікованого шару на поверхні розділу. На відміну від хемосорбції, хімічна реакція призводить до утворення шару продукту цієї реакції, інакше кажучи - тривимірної фази.
Характерним прикладом взаємодії поверхонь твердих тіл із середовищем є їх окислення.
Практично всі поверхні твердих тіл, зокрема металів, починаючи з моменту свого утворення, контактують з повітрям. Активний компонент повітря - кисень - хемосорбіруется на поверхні металу. Тут його двухатомная молекула дисоціює, так як енергія взаємодії з поверхнею більше енергії зв'язку атомів в молекулі. Потім кисень реагує з поверхнею, утворюючи плівки оксидів, як правило, кристалічної будови. Швидкість освіти оксидів достатня висока. На таких металах, як Fe, Cu, Al, менш ніж через 5 хв після обробки різанням вже при кімнатній температурі утворюється плівка товщиною до 10 нм, причому при зростанні температури швидкість утворення оксидної плівки збільшується. Покриваючи поверхні металу шаром, товщина якого більше радіусу дії сил тяжіння, що діють між твердими тілами, оксиди покращують фрикционно-ізносние характеристики сполучення, оскільки адгезія оксидних плівок набагато менше адгезії між атомарному чистими поверхнями металів.
Необхідно відзначити один важливий наслідок адсорбції поверхнево-активних середовищ на поверхнях твердих тіл. Академік П.А. Ребиндер встановив, що при цьому відбувається пластіфіцірованія найтоншого (глибиною близько 0,1 мкм) поверхневого шару твердих тіл (як металів, так і неметалів), полегшення його деформируемости, зниження його міцності (виникнення крихкого руйнування, при малих напругах аж до мимовільного диспергування) і твердості. Цей ефект (званий в науковій літературі «ефектом Ребіндера») значно впливає як на обробку різанням і тиском, полегшуючи ці технологічні процеси, так і на процес тертя. Термодинамічно ефект Ребіндера може бути пояснений зниженням вільної поверхневої енергії твердих тіл в результаті адсорбционного впливу поверхнево-активних середовищ.
Пластифицирующее дію адсорбционно-активних середовищ проявляється в полегшенні виходу дислокацій на поверхню і зародження поверхневих джерел дислокацій. Крім зовнішньої форми прояву ефекту Ребіндера виділяють його внутрішню форму, яка визначається адсорбцією поверхнево-активних речовин на внутрішніх поверхнях розділу зародкових мікротріщин, що утворюються в результаті деформування твердих тіл. Це полегшує розвиток мікротріщин ( «розклинюючий» ефект) і призводить до крихкого руйнування твердого тіла. Ефект Ребіндера проявляється при спільному впливі поверхнево-активного середовища і напруженого стану. Так, за даними Г.І. Фукса, в поверхнево-активних середовищах зменшується твердість на вдавлення найтонших поверхневих шарів металу. Адсорбційну активність проявляють, зокрема, вуглеводні з різними полярними групами (в порядку убування адсорбційної здатності): -OH, -COOH, -NH2. -COOR. При цьому більше зниження поверхневої міцності забезпечують речовини з короткою вуглеводневої ланцюгом, що, мабуть, дозволяє їм легше проникати в мікротріщини. Значну адсорбционную активність проявляють розплави легкоплавких металів по відношенню до більш тугоплавким.
Пластична деформація в процесі обробки металів тиском і різанням значно збільшує фізико-хімічну активність поверхневих шарів. Це в значній мірі визначає будову і властивості утворених на поверхні деталей шарів, кінетику фізичної та хімічної адсорбції і хімічної взаємодії. При деформації металів (пружною або пластичної), згідно з Ван-Бюрен, практично вся збережена в цьому процесі енергія витрачається на освіту або на збільшення енергії взаємодії дефектів решітки. Так, концентрація дефектів, що характеризує нерівноважний стан металу при 10% -ної деформації, досягає 10 18 -10 19 см -3. Дослідження показують, що структура поверхневого шару металу вже після технологічної обробки є ряд шарів (рис. 2), розташованих в наступному порядку (від поверхні в глиб металу): 1 - шар, що складається з забруднень (адсорбованих з мастильно-охолоджувальної рідини і т . Д.); 2 - шар адсорбованого газу; 3 шар оксиду; 4 - зміцнений під час механічної обробки шар, що складається з сильно деформованих під дією нормальних і тангенціальних зусиль зерен; 5 - метал з вихідною структурою.
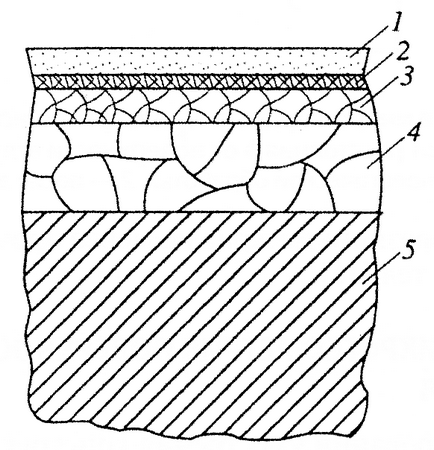
Мал. 2. Структура поверхневого шару шліфованої сталевої деталі.
Фізико-хімічні властивості поверхневих шарів металів визначаються процесами, що мають місце при механічній обробці (зміцнення внаслідок пластичних деформацій - наклеп, разупрочнение внаслідок впливу температур, що генеруються при обробці, - відпустка); фізичної адсорбції і хемосорбції з урахуванням адсорбционного зниження міцності (найбільш інтенсивно проявляється при розтягуючих напруг, створюваних в матеріалі, що характерно при терті ковзання). У найзагальнішому випадку зміни твердості найтонших поверхневих шарів по глибині в умовах технологічної обробки і в умовах зовнішнього тертя мають вигляд, наведений на рис. 3.
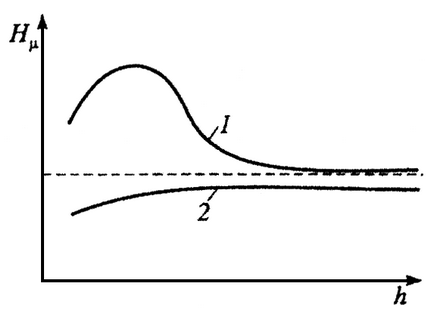
Мал. 3. Зміна мікротвердості Нμ поверхневого шару металу в залежності від відстані h від поверхні вглиб металу: 1 - після технологічної обробки; 2 - після експлуатації.
Відповідно до сформульованого І.В. Крагельська правилом позитивного градієнта механічних властивостей металів за глибиною, зовнішнє тертя (на відміну від внутрішнього тертя, при якому має місце руйнування поверхневих і більш глибоко лежачих шарів тертьових тіл) має місце в тому випадку, коли dHμ / dH> 0. Забезпечення позитивного градієнта механічних шарів по глибині може бути здійснено в процесі технологічної обробки (наприклад, шляхом нанесення тонких плівок металу або полімеру, більш м'якого, ніж основний метал), або шляхом адсорбції або хемосорбції молекул активних компонентів мастильних матеріалів, або шляхом введення між труться тілами твердого, рідкого або газоподібного матеріалу, менш міцного на зрушення, ніж матеріал, що труться тел.
Сайт створено в системі uCoz