Магній - дванадцятий за рахунком елемент Періодичної системи. Метал. Розташований в третьому періоді, II группеA підгрупі.
Порядковий номер дорівнює 12. Заряд ядра дорівнює +12. Атомний вагу - 24,132 а.е.м.
Електронна будова атома магнію
Магній розташований в третьому періоді, значить, він має три оболонки, одна з яких зовнішня, яка містить валентні електрони. Атом магнію має позитивно заряджене ядро (+12), в якому є 12 протонів і 12 нейтронів (різниця між атомною вагою і порядковим номером). По орбітах навколо ядра рухаються 12 електронів.
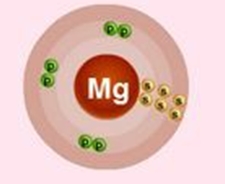
Мал. 1. Схематичне зображення будови атома магнію.
Електронну конфігурацію атома магнію можна записати двояко:
1s 2 2s 2 2p 6 3s 2.
Магній відноситься до сімейства s-елементів. Енергетична діаграма атома магнію (на ній зображуються тільки валентні електрони) має вигляд:
В результаті хімічної взаємодії магній втрачає свої валентні електрони, тобто є їх донором, і перетворюється в позитивно заряджений іон (Mg 2+):
Mg 0 -2e → Mg 2+;
У з'єднаннях магній проявляє ступінь окислення +2.
Приклади розв'язання задач
Хімічному елементу головної підгрупи відповідає вищий оксид складу RO3. Яка електронна конфігурація зовнішнього енергетичного рівня атома цього елемента?
Необхідно визначити до якої групи Періодичної системи відноситься елемент, який утворює вищий оксид складу RO3. Оскільки в оксидах кисень проявляє постійну валентність рівну II, то вища валентність елемента в оксиді R VI O II 3 дорівнює VI.
Звідси випливає, що це елемент VIA групи, в його атомі 6 валентних електронів. Цій вимозі відповідає елемент з електронною формулою ns 2 np 4.