- 10 найвпливовіших психологів
- Як провести час з дітьми? Ось вам 100 ідей!
- Ід, Его і Суперего
- Вчені піддали критиці піраміду Маслоу
- Ефект Струпа: як створити ваш власний експеримент?
- 10 речей, які необхідно знати про психологію
div> .uk-panel '> "data-uk-grid-margin>
амінокислоти
Дещо з хімії про амінокислоти (раптом хто не знає), які є всім і вся для наших з вами організмів. З курсу біології ми ще знаємо що амінокислоти є мономерами, т. Е можуть в слідстві полімеризації утворювати полімери, ніж та є білки. Звичайно всі амінокислоти мають органічну структуру.
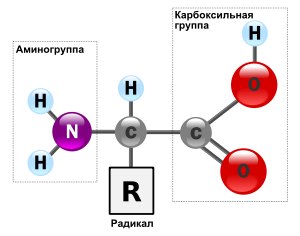
Що стосується будови амінокислот, то кожна амінокислота складається з карбоксильної (-COOH) і аминной (-NH2) групи, які пов'язані одним атомом вуглецю. До цього вуглецю приєднується бічний ланцюг - радикал, який є як раз таки определителям властивості амінокислоти.
У більшій частині амінок існує тільки одна аминная і карбоксильная група, такі амінокислоти називаються «нейтральними». Однак, існують амінокислоти більш ніж з однієї аміно Іллі карбоксильною групою, вони називаються «основними».
Науці відомо лише близько 200 амінокислот, які можуть зустрінеться в організмах, проте, тільки 20 з них входять до складу білків. Ці 20 амінокислот називають белокобразующіе або Протеїногенні амінокислоти.
Залежно від радикала, про який було написано вище, основні аміноксилот ділять на три групи:
1) неполярні (аланін, метіонін, валін, про-лін, лейцин, ізолейцин, триптофан, фенілаланін)
2) полярні незаряджені (аспарагін, глутамін, серії, гліцин, тирозин, треонін, цистеїн)
3) полярні заряджені (аргінін, гістидин, лізин - позитивно; аспарагінова і глутамінова кислоти - негативно).
Для зовсім хіміків:
Бічні ланцюга амінокислот (радикал) можуть бути гідрофобними або гідрофільними, що надає білків відповідні властивості, які проявляються при утворенні вторинної, третинної і четвертинної структур білка.
У розчині амінокислоти можуть виступати в ролі як кислот, так і основ, т. Е. Вони є амфотерними сполуками. Карбоксильная група -СООН здатна віддавати протон, функціонуючи як кислота, а аминная - NH2 - приймати протон, виявляючи таким чином властивості підстави.
Примітки: На фотографії представлена загальна формула амінокислот.
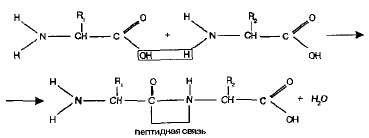
У продовженні курсу про амінокислоти я хочу додати дещо про пептидах. Зараз вони широко продаються і використовуються в спорті, косметології, хірургії і так далі ... Але ми поговоримо про хімії, а точніше про органічної хімії, адже пептиди мають органічну структуру. І так, що таке пептіди- це органічні речовини, що утворюються, коли аминогруппа однієї амінокислоти здатна вступати в реакцію з карбоксильної групою іншої амінокислоти. (Про групах дивіться мою попередню статтю). Молекула, що утворюється при цьому називається дипептид, а зв'язок -CO-NH- називається пептидного зв'язком.
На утворився дипептидами з одного боку знаходиться вільна аміногрупа, а з іншого карбоксильная. Завдяки цьому, дипептид може приєднувати до себе інші амінокислоти, і тоді утворюються олигопептид, якщо таким чином приєднується більше 10 амінокислот, то утворюється полепептід. Сподіваюся зрозуміло)
Багато гормони (інсулін, адренокортикотропний гормон та ін.), Антибіотики (наприклад, граміцидин А), токсини (наприклад, дифтерійний токсин) є поліпептидами.
Білки являють собою поліпептиди, в молекулу яких входить від п'ятдесяти до декількох тисяч амінокислот з відносною молекулярною масою понад 10 000.
Ось така ось коротенька статейка, сподіваюся кожен засвоїв щось нове, або повторив пройдене, спасибі за увагу.