Московська медична академія ім. И.М.Сеченова
Фактори ризику розвитку АТ
За сучасними уявленнями, АТ - багатофакторне захворювання, розвиток якого тісно пов'язане з генетичними дефектами імунної відповіді і негативними впливами несприятливих факторів зовнішнього середовища. Встановлено, що дія цих чинників визначає темпи розвитку АТ, особливо у дітей раннього віку, причому чим раніше починається вплив цих факторів, тим більш ранньої є маніфестація АД [4, 6].
Спадкова схильність до алергії, виявлена нами в 82% спостережень, є провідним фактором і визначається особливостями генетично запрограмованого системного імунної відповіді на антиген, а також порушеннями генетичного контролю продукції цитокінів, особливо інтерлейкіну-4 (ІЛ-4), що супроводжується підвищенням продукції IgЕ і генералізованої гіперчутливістю [7]. Спадково обумовлені також місцеві механізми формування АТ, які характеризуються великою накопиченням клітин Лангерганса в шкірі хворих дітей, змінами будови і розподілу в епідермісі цих клітин, збільшенням числа високоаффінних рецепторів на їх мембранах і зниженням ролі в підтримці мітотичної активності кератиноцитів, що підсилює гіперпроліферативних процеси в епідермісі . Генетично обумовлене також наявність значного числа еозінофілов- "довгожителів", стійких до апоптозу, що сприяє збільшенню їх циркуляції в крові до 3 міс (хоча в нормі вони живуть не більше 1 міс); одночасно виявляється також спадково детермінована патологія синтезу ліпідів, що призводить до дефіциту церамидов і підвищеної сухості шкіри, що порушує її бар'єрну функцію [7, 8].
У реалізації спадкової схильності до розвитку АТ беруть участь також численні фактори зовнішнього середовища: висока антигенна навантаження на плід під час вагітності, куріння матері, раннє штучне вигодовування, а також раннє введення прикорму і продуктів, які не відповідають віку дитини [4].
Значущим чинником ризику АТ є патологія органів шлунково-кишкового тракту (ШКТ), особливо дисбіоз кишечнику (89%), так як нормальна мікрофлора кишечника відіграє найважливішу роль в становленні імунної системи дитини і має протективний дією у формуванні атопії. Мають значення також порушення екології довкілля та мікрооточення дитини. Дія цих факторів проявляється в певні вікові періоди, і їх несприятливе поєднання супроводжується формуванням різних форм АД у дітей.
Причинно-значущими алергенами при АД є перш за все харчові алергени, які особливо часто визначаються у дітей раннього віку (за нашими даними, в 94-100% випадків). По суті харчова алергія є стартовою сенсибілізацією, на тлі якої шляхом перехресних реакцій формується гіперчутливість до інших алергенів. Домінуюча роль харчової алергії поступово зменшується з віком дитини і збільшується значимість аероаллергенов, перш за все побутових (38%), епідермальних (35%), пилкових (32%), бактеріальних алергенів (20%), постійне дію яких сприяє рецидивуючого перебігу АД [3 , 4].
Серед бактеріальних алергенів при АД встановлена значна роль золотистого стафілокока, який в 80-90% випадків є основним мікроорганізмом, колонізує уражені ділянки шкіри і виділяє екзотоксини з властивостями суперантігенов, які інгібують апоптоз і стимулюють проліферацію Т-лімфоцитів, що прискорює хронізації алергічного запалення шкіри [ 8, 9].
патогенез АД
В основі патогенезу АД лежать імунні механізми з провідною роллю Т-лімфоцитів і клітин Лангерганса. В даний час встановлено, що в механізмах формування АТ провідним є двофазний імунну відповідь, обумовлений певною поляризацією Т-лімфоцитів [7]. Крім того, встановлено, що клітини Лангерганса є основними клітинами імунної системи шкіри, відповідальними за IgE-опосередкований накопичення алергенів в шкірі, а також їх презентацію Т-лімфоцитам, і їх число у хворих АД значно вище, ніж у здорових [10]. У цьому вбачають одну з причин переважного ураження шкіри у дітей при АД. В останні роки клітини Лангерганса розглядаються як спеціалізовані високопотентних антігенпрезентірующіх клітини шкіри, відповідальні за розвиток гострої фази алергічного запалення в шкірі і перемикання імунної відповіді на Th2. При першому контакті антиген зв'язується з високоаффіннимі рецепторами IgE (FceRI), які розташовані на поверхні клітин Лангерганса, в них алергени піддаються ферментативному розщепленню і зв'язуються з HLA-антигенами II класу. Утворений при цьому поліпептид специфічно розпізнається Т-клітинним рецептором CD4 + -лімфоцитів. Отримавши інформацію, клітини Лангерганса переміщаються в лімфатичні вузли, де вступають у взаємодію з Th0-лімфоцитами, що збільшує активацію Т-хелперів, сприяє переключенню їх в сторону Th2 і супроводжується підвищенням продукції цитокінів. При цьому Th2-хелпери виділяють переважно ІЛ (ІЛ-4, ІЛ-5, ІЛ-10, ІЛ-13) і активують В-лімфоцити з локальної гиперпродукцией специфічних IgE. При повторному надходженні алергену відбувається його зв'язування зі специфічними рецепторами на мембрані огрядних клітин, що індукує процес їх дегрануляції з виділенням медіаторів запалення і хемокінів, які запускають ранню фазу алергічної реакції, клінічно виявляється вираженим свербінням, гіперемією, висипаннями на шкірі.
Під дією медіаторів гострої фази АД в епідерміс залучаються запальні дендритні епітеліальні клітини, які також є антигенпрезентуючими, відповідальними за формування хронічної фази АД, яка характеризується перемиканням імунної відповіді з Th2- на Th1-лімфоцити з підвищеною продукцією ними інтерферону g (ІФН- g), ІЛ -2 і ІЛ-12, що сприяє хронізації алергічного процесу в шкірі [10]. Поряд з цим цитокіни ІЛ-5, ІЛ-6, ІЛ-8 підсилюють міграцію еозинофілів і макрофагів у вогнище запалення, що визначає темпи хронізації алергічного запалення шкіри. Причому в хронізації АТ особливе значення мають еозинофіли "довгожителі", які менш схильні до апоптозу і продукують високі рівні основного білка еозинофілів.
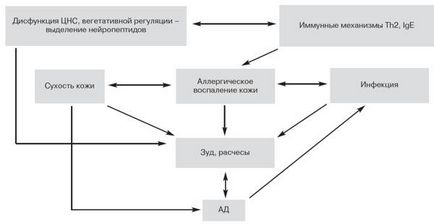
Поряд з імунними механізмами в патогенезі АД мають значення пошкодження рогового шару епідермісу і водно-ліпідної плівки в результаті алергічного запалення. Причому при пошкодженні цієї водно-ліпідної плівки значно збільшуються трансепідермальних втрати води, що призводить до вираженої сухості шкіри, її високу чутливість до іррітанти, розмноженню бактерій і накопичення антигенів. Підвищена сухість шкіри сприяє підтримці сверблячки, а свербіж і расчеси супроводжуються додатковим пошкодженням кератиноцитів і огрядних клітин, що посилює алергічне запалення шкіри при АД. При расчесах підвищується інфікування шкіри патогенною флорою, переважно золотистим стафілококом, який пригнічує апоптоз і підсилює проліферацію Т-лімфоцитів, що також сприяє хронізації алергічного запалення в шкірі [10, 11]. Крім того, в останні роки встановлено значення аутоаллергенов, що вивільняються з запально змінених тканин, особливо при розчісуванні, які підтримують імунну відповідь, первинно викликаний алергенами навколишнього середовища [10]. Певну роль відіграє також дисфункція центральної і вегетативної нервової системи хворих, яка за допомогою нейропептидів контролює активність імунокомпетентних клітин і безпосередньо бере участь в механізмах формування сверблячки при АТ у дітей (рис. 1).
Патофізіологічні зміни при АД полягають в тому, що при алергічному запалення шкіра у хворих має ряд особливостей і характеризується неспецифічної гіперреактивністю до різних подразників і антигенів, підвищеною сухістю, порушеннями фізіологічної десквамації епітелію, потовщенням рогового шару з розвитком гіперкератозу і вираженого лущення.
Рис.1. Схема патогенезу АД.
Таблиця 1. Протизапальні засоби для зовнішньої терапії АД
Мал. 2. Діагностичні критерії АД.
• Сверблячка шкіри
• Вікова морфологія висипів
• Вікова стадийность
• Типова локалізація
• Ранній початок
• Хронічне рецидивуючий перебіг
• Спадкова обтяженість
• Неспецифічна гіперреактивність шкіри
Мал. 3. Динаміка симптомів АД (за шкалою SCORAD) на тлі лікування Еліделом.