1. Яку будову мають атоми хімічних елементів?
У центрі атома знаходиться позитивно-заряджене ядро, яке складається з протонів і нейтронів, а навколо ядра переміщаються електрони відповідно до визначених законами.
2. Вкажіть порядковий номер, заряд ядра і розрахуйте число протонів, нейтронів і електронів в атомах бору (масове число 11), міді (масове число 63) і олова (масове число 118).
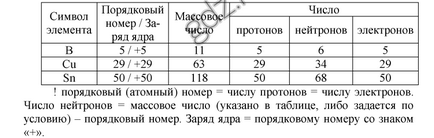
3. Напишіть електронні формули атомів азоту і алюмінію.
4. Напишіть не менше трьох символів хімічних елементів, у яких не зовнішньому енергетичному рівні знаходиться чотири електрона. Зобразіть схему будови атома і електронну формулу одного з них.
1. Вкажіть відмінності в будові атомів типових металів і типових неметалів.
Атоми типових металів мають на валентном рівні 1-2 електрона (елементи I і II А груп, крім H і He), а типових неметалів - більше 4 електронів.
2. Вкажіть порядковий номер, заряд ядра і розрахуйте число протонів, нейтронів і електронів в атомах кальцію (масове число 40), кисню (масове число 16) і срібла (масове число 107).

3. Напишіть електронні формули атомів фтору і кремнію.
4. Електронна формула атома елемента 1s2 2s2 2p6 3s1. Який це елемент? Напишіть формули оксиду і гідроксиду даного елемента.
Na. Na2O - оксид натрію, NaOH - гідроксид натрію.
1. Що спільного в будові атомів хімічних елементів, розташованих в одній А-групі?
Однакова кількість електронів на зовнішньому енергетичному рівні.
2. Вкажіть порядковий номер, заряд ядра і розрахуйте число протонів, нейтронів і електронів в атомах вуглецю (масове число 12), цинку (масове число 64) і брому (масове число 79).
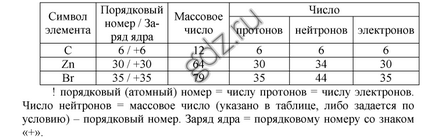
3. Напишіть електронні формули атомів літію і хлору.
4. Напишіть не менше трьох символів хімічних елементів, у яких на зовнішньому енергетичному рівні знаходяться п'ять електронів. Зобразіть схему будови атома і електронну формулу одного з них.
1. Що спільного в будові атомів хімічних елементів, розташованих в одному періоді?
У атомів, розташованих в одному періоді однакове число енергетичних рівнів.
2. Вкажіть порядковий номер, заряд ядра і розрахуйте число протонів, нейтронів і електронів в атомах фтору (масове число 19), калію (масове число 39) і золота (масове число 197).
3. Напишіть електронні формули атомів магнію і кисню.
4. Електронна формула атома елемента 1s2 2s2 2p6 3s2 3p4. Який це елемент? Напишіть для даного елементи формули вищого оксиду і летючого з'єднання з воднем.
S. SO3 - оксид сірки (VI), H₂S - сірководень.